美 ASCO서 고형암 대상 중간연구 결과 발표
루닛과 협업한 AI 활용 바이오마커 분석 결과도 공개
이뮨온시아(대표 김흥태)는 지난 6월 1일(현지시간) 미국 시카고에서 개최된 미국임상종양학회(ASCO)에서 CD47 단클론항체 'IMC-002'의 고형암 1a상 임상시험 중간결과를 발표했다고 밝혔다.
이번에 소개된 1상 연구 데이터는 용량 증량(dose escalation) 관련 부분으로, 2022년 5월부터 총 4개의 용량 코호트에 등록된 12명 환자에게 각각 IMC-002을 5, 10, 20, 또는 30 mg/kg을 2주 간격으로 투여했다.
회사 관계자는 "연구 결과, 측정 가능한 병변이 있는 환자 12명중 6명에서 안정반응(SD)이 확인돼 50%의 질병조절율(DCR)을 보였다. 이 중 5명은 간세포암 환자, 1명은 유방암 환자였다"며 "아울러, 환자 4명에서 6개월 이상 안정반응이 지속돼 33.3%의 임상적 이득율(CBR)을 확인했다"고 소개했다.
이날 회사는 루닛과 협업해 진행한 AI 활용 바이오마커 분석(Lunit SCOPE IO) 결과 또한 발표했다. 임상 효능이 확인된 CBR 그룹의 CD47 양성 대식세포 밀도는 71.0/mm 로, 비 CBR 그룹 44.3/mm²에 비해 더 높은 것으로 나타났으나, CD47 양성 종양 세포의 밀도는 두 그룹 간에 큰 차이를 보이지 않았다. CD47 양성 대식세포의 밀도와 치료 반응의 연관성을 시사하고, 향후 CD47을 표적으로 한 치료 전략 개발에 중요한 역할을 할 것으로 기대된다는 것이 회사 측 설명이다.
임상시험 책임자인 임호영 삼성서울병원 교수는 "모든 코호트에서 용량제한독성(DLT)은 관찰되지 않았고, 항 CD47 치료제에서 주로 나타나는 주입관련반응, 용혈성 빈혈, 혈소판감소증 및 호중구감소증도 보고되지 않아 IMC-002의 높은 안전성이 확인됐다"며 "특히, IMC-002의 단독 투여에도 불구하고 15개월째 투약을 유지 중인 간암 환자의 경우, 장기독성이 없을 뿐만 아니라 종양 크기도 20% 감소를 보여 예후가 매우 좋을 것으로 기대된다"고 말했다.
이뮨온시아 김흥태 대표는 "지난 2023년 10월 유럽종양학회(ESMO)에서 발표된 중간 결과를 통해 IMC-002의 안전성과 내약성을 1차 공개했고, 임상 2상 권장 용량 또한 20 mg/kg 3주 간격 투약으로 확인한 바 있다"며 "작년 11월부터 개시한 IMC-002 임상 1b상을 통해 미충족 수요가 높은 특정 고형암에 대한 IMC-002의 효능을 추가할 수 있을 것으로 기대한다"고 전했다.
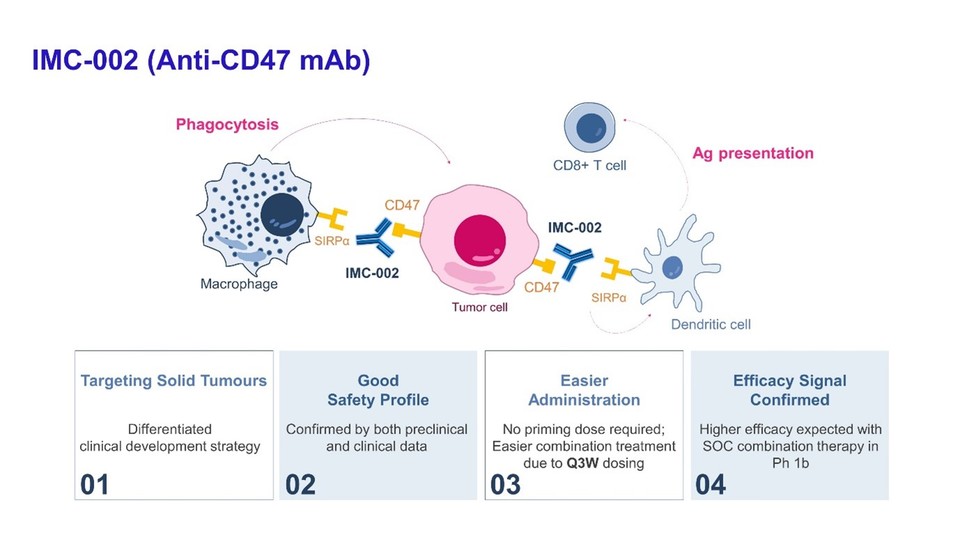
한편, IMC-002는 대식세포에 대한 면역관문억제제로, 암세포의 CD47과 대식세포의 SIRPα 간의 'don’t eat me' 신호를 차단해 대식세포가 암세포를 공격할 수 있도록 돕는 약물이다.

