특별기고
배진건 박사(이노큐어 테라퓨틱스, 수석부사장)

베타-아밀로이드(Aβ)는 어떻게 형성되는가? Aβ는 β- 및 γ-세크레타제(secretase)에 의한 순차적 절단을 통해 β-아밀로이드 전구체 단백질(APP)로부터 유래된다. γ-세크레타제는 프레세닐린(PS), 니카스트린(NCT), 전인두 결함 1(APH-1) 및 프레세닐린 인핸서 2(PEN-2)의 4가지 성분으로 구성된 고분자량(230 kDa, 19 TMs) 복합체이다. Aβ 생산에 중요한 효소인 γ-세크레타제는 사이즈가 큰 단백질이지만 매력적인 AD 치료 표적이다.
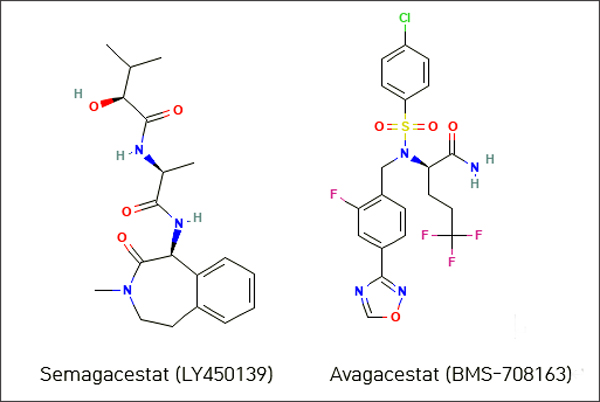
먼저 semagacestat 및 avagacestat와 같은 γ-세크레타제 억제제가 존재하였다. 하지만 연구자들이 100개 이상의 막횡단 단백질을 처리하는 프로테아제를 잘라내면 인지 기능을 방해할 수 있다는 염려때문에 이 억제제는 슬금슬금 사라졌다(2012년 12월 뉴스, 2010년 8월 뉴스).
이 분야는 어떻게 되살아났는가? γ-Secretase가 아밀로이드 생성 Aβ42 및 Aβ43을 Aβ37 및 Aβ38과 같은 더 작고 무해한 펩타이드로 처리하도록 조정한다는 아이디어를 바탕으로 γ-세크레타제를 조절하는 데 중점을 두었다. 2001년에 일부 비스테로이드성 항염증제는 효능이 낮더라도 그렇게 작용하는 것으로 보고되었다(Weggen et al., 2001). 2010년대에는 Chiesi, Forum Therapeutics, Neurogenetics 등의 여러 후보물질이 보고되고 임상1상에 진입하였다. 임상 2상에는 아무 회사도 진출하지 못했다.
그런 다음 과학자들은 Eisai의 E2212, Bristol Myers Squibb의 BMS-932481 및 임상 1단계에서 테스트된 Pfizer의 PF-06648671을 포함하여 대부분 아릴-이미다졸 그룹을 포함하는 화합물인 2세대 GSM을 발견했다. BMS의 화합물은 간에 독성이 있었다. 그러기에 임상 2상에 진출한 회사는 아직도 없었다(Nordvall et al., 2023 리뷰 참조).
γ-세크레타제 조절제가 다시 돌아올 수 있을까? 시간도 흐르고 불가능해 보였다. 그러나 지난 10월 24~27일 보스턴에서 열린 올해 알츠하이머병 임상 시험(Clinical Trials on Alzheimer's Disease(CTAD) 컨퍼런스에서 기대가 되살아났다. 스위스 바젤의 F. Hoffmann-La Roche의 Irene Gerlach가 이끄는 과학자들은 2세대 GSM인 RG6289가 1상 시험에서 안전한 것으로 나타났으며 Aβ 생산을 더 작고 덜 끈적이는 펩타이드로 전환했다고 보고했다.
보스턴 브리검 여성병원의 AD 전문가인 데니스 셀코(Dennis Selkoe)는 이 데이터가 설득력이 있다고 말했다. "AD 분야에서는 아밀로이드를 낮추고 충분히 조기에 사용하면 AD 진행을 예방할 수 있는 경구용 소분자 치료제가 절실히 필요하기 때문에 Roche의 분자 및 기타 잘 검증된 γ-Secretase Modulator(GSM) 후보 물질의 지속적인 개발을 기대한다."라고 Selkoe는 말했다. 로슈는 2024년에 임상 2상을 시작할 계획이다. 이번 임상은 극심한 좌절을 겪었던 분야에 다시 활력을 불어넣을 것이다.
이 모든 실패와 좌절이 있은 후 무엇이 GSM에 다시 관심을 불러일으켰을까? 염려하던 더 짧은 Aβ 펩타이드가 Aβ42보다 독성이 낮을 뿐만 아니라 아밀로이드 감소 면역요법에서 볼 수 있는 임상적 이점과 결합하여 보호적이라는 인식이 나타났다(Cullen et al., 2022; 2022년 1월 뉴스, 2023년 7월 뉴스). 뮌헨 대학의 Harald Steiner는 "이제 우리는 Aβ 면역요법이 효과가 있다는 것을 알고 있기 때문에 다음 단계는 Aβ 생성에 대항하는 작은 분자를 만들어 결국 면역요법 이후 유지 요법에 사용하는 것이라고 생각한다."라고 말했다. “GSM을 이용한 예방 치료법도 생각할 수 있다.”라고 그는 덧붙였다.
Irene Gerlach의 말을 믿고 Roche는 결코 GSM을 포기하지 않았다. "BACE 억제제가 등장했기 때문에 현장에서는 BACE 억제제가 필요하지 않다고 믿었던 때가 있었지만 우리는 그런 견해를 결코 받아들이지 않았다."라고 그녀는 Alzforum 인터뷰에 대답했다.
2020년에 Gerlach와 동료들은 트리아졸로-아제핀 구조를 가진 GSM의 새로운 종류인 RO7185876이 시험관 내 및 생쥐 모두에서 Aβ42 및 Aβ40을 희생하여 Aβ의 단백질 분해를 Aβ37 및 Aβ38로 이동시켰다고 보고했다(Ratni et al., 2020). 이 구조는 일부 초기 GSM의 독성을 유발할 수 있는 이미다졸 그룹을 피하지만 Gerlach는 Alzforum에 RG6289가 구조가 전혀 다른 분자라고 말했다.
실제로 Roche는 RG6289에 대해 거의 공개하지 않았지만 CTAD에서 Agnes Portron은 최근 보고된 바와 같이 기질-분비효소 상호작용을 안정화하고 아마도 기질이 막 밖으로 미끄러지는 것을 방지함으로써 절단을 연장한다고 말했다(2023년 11월 뉴스). 시험관 내에서, RG6289는 M 미만 농도에서 Aβ37 및 Aβ38을 약 6배 증가시켰다. 이는 전체 Aβ 생산에 영향을 주지 않고 Aβ40 및 Aβ42를 거의 제거했다. 이 화합물은 신경 발생 및 기타 세포 증식 경로를 조절하는 γ-분비효소 기질인 Notch의 처리를 방해하지 않았다.
로슈는 2021년 1상 시험을 시작했고, Portron은 일부 결과를 발표했다. 이 연구에는 127명의 건강한 지원자가 등록되었다. 이는 시험 과정에서 나타나는 약동학 및 약력학 데이터에 따라 용량을 증가시키는 적응형 설계를 사용하고 있다. Roche는 임상시험을 6개 부분으로 나누었다. Portron은 4가지 데이터를 보여주었다. 18세에서 45세 사이의 단일 상승 용량; 18~64세의 경우 2주에 걸쳐 용량을 여러 번 증량한다. 64~85세의 사람들에게는 2주에 걸쳐 여러 번 투여한다. 음식 섭취가 약동학에 미치는 영향에 대한 연구도 포함되었다. 전반적으로 이 약은 두통, 메스꺼움, 설사와 같은 경미한 부작용을 나타냈으며, 그 중 상당수는 위약군에서 더 흔했다. 부작용 발생률은 복용량에 따라 증가하지 않았다.
경구로 투여된 RG6289는 사람들의 혈장에 빠르게 진입했으며, 음식과 함께 복용하든 관계없이 약의 농도는 약 5일 동안 꾸준히 떨어졌다. 약동학에서는 반감기가 13~21시간으로 제안되었으며, 이는 하루에 한 번 투여하는 것이 좋다. 이 일일 요법을 통해 RG6289는 항정 상태 농도에 도달했다. 그 중 약 3%가 CSF에 도달했는데 이는 혈액을 통해 흐르는 유리 화합물의 양과 동일하다고 Portron은 말했다. 뇌척수액 샘플은 혈액 내 화합물 농도가 정상 상태에 도달한 후 젊은 다중 용량 증가 그룹의 사람들로부터 한 번 수집되었다.
혈장 및 CSF Aβ42 분석에 따르면 화합물이 목표에 도달한 것으로 나타났다. 혈장 Aβ42는 용량 의존적으로 떨어졌지만 Porton은 그 용량이 무엇인지 밝히지 않았다. 뇌 외부의 분비효소 활동도 APP에서 Aβ를 방출하므로 측정된 혈장 감소는 말초 γ-분비효소의 조절과 일치할 수 있다.
다중 상승 용량(multiple-ascending-dose) 요법에서 Roche는 CSF에서 Aβ42 및 Aβ40의 용량 의존적 감소를 기록했으며, 겉보기 최고 용량에서는 80% 감소했다. 이번에도 Porton은 복용량 정보를 공개하지 않았으며 Gerlach도 공개하지 않았다. 이러한 Aβ42 및 Aβ40 감소와 함께 CSF Aβ37 및 Aβ38이 동시에 증가하여 γ-세크레타제 진행성의 조절을 시사한다.
로슈는 내년에 2상 시험을 시작할 계획이며, 1상 시험의 약동학을 기반으로 용량을 선택한다. Gerlach는 이것이 손상되지 않았거나 AD로 인한 경미한 인지 장애가 있든 상관없이 아밀로이드 양성 반응을 보이는 사람들에게 있을 것이라고 말했다. 그녀는 연구 설계에 대한 세부 사항이 내년 초 회의에서 발표될 것이라고 말했다. CTAD의 포스터에서 과학자들은 임상 2상 용량이 혈장 Aβ42를 27~66% 낮추는 것을 목표로 할 것이라고 암시했다. 저자들은 이 범위가 긍정적인 이익 대 위험 비율을 정의한다고 믿는다.
업계 사람들이 걱정하는 위험 요소 중 하나는 Notch 및 기타 기질의 처리가 변경되는 것이다. 최근 벨기에 KU Leuven에 있는 Bart de Strooper 연구실의 과학자들은 소교세포(microglia)에서만 이러한 기질 중 85개를 발견했다. 실제로, γ-세크레타제 억제제(GSI)는 아밀로이드증과 관련된 소교세포 반응을 근본적으로 제한했다. 이러한 막횡단 단백질 중 다수는 세포내 도메인(ICD)을 통해 신호를 전달하며, γ-세크레타제는 GSI에 의해 차단되는 내부 단백질 분해 단계에서 ICD를 잘라낸다. 반면에 조절제는 ICD가 출시되면 카르복시펩티다제 처리를 가속화하도록 설계되었다.
Steiner는 "GSI처럼 γ-세크레타제의 신호 기능에 부정적인 영향을 미칠 염려가 없다. 왜냐하면 GSM은 ICD를 생성하는 절단에 영향을 주지 않기 때문이다."라고 Steiner는 설명했다.
그럼에도 불구하고 Gerlach와 동료들은 더 넓은 γ-세크레타제 프로테옴에 대한 효과를 테스트하고 있다. "내인성으로 기질을 발현하는 세포주를 사용한 단백질체학 연구에서 우리는 GSI가 서벌 기질의 처리를 차단했지만 일련의 GSM을 사용하여 조사된 하위 상태에 그러한 영향을 미치지 않았다는 것을 확인했다."라고 Gerlach는 Alzforum 인터뷰에 말했다. "물론, 우리가 모든 기질을 조사하지는 않았지만, 우리의 데이터는 조절제에 대해 예상되는 것처럼 다른 γ-세크레타제 기질(비APP)에 아무런 영향을 미치지 않는다는 것을 매우 일관되게 보여준다.”
프레세닐린 절단 기능의 감마-분비효소 알로스테릭 조절제(즉, GSM)는 AD에 대한 매력적인 치료 접근법을 제공한다. 이는 질병을 유발할 수 있는 더 길고 더 자기 응집적인 Aβ-펩티드의 프레세닐린 매개 생산에 대한 외과적 제거를 나타낸다.
이러한 접근법은 오랫동안 알려져 왔지만, 필자의 생각에는 의약화학, 화합물 개발, 임상시험과 관련하여 충분한 관심을 받지 못했다. 최근 CTAD에서 Agnes Portron과 동료들이 새로운 GSM에 대한 Roche의 임상 1상 데이터에 대해 발표한 내용은 설득력이 있었고 저자가 다가오는 2단계 실험에서 기계적으로 계획한 대로 이 화합물이 추가 개발 가치가 있음을 보여준다.
AD 분야에서는 아밀로이드를 낮추고 충분히 조기에 사용하면 AD 진행을 예방할 수 있는 경구용 소분자 치료제가 너무나도 절실히 필요하기 때문에 Roche의 분자 및 기타 잘 검증된 GSM 후보 물질의 지속적인 개발에 기대를 건다.
관련기사
- 효소 이름은 '-ase'가 끝에 붙는데 왜 Autotaxin인가?
- 알츠하이머 뉴런 사멸 뒤에 숨은 미스터리를 해독하다
- 치매 걸릴 확률 현저히 낮추려면 덜 앉고, 더 움직여라
- PLCγ2 M28L 변형, 기억상실 악화…P522R은 신경 보호 촉진
- 달콤한 '빵의 단백질 글루텐'은 사람의 뇌에도 영향 미칠까
- 'RNA 결합 단백질'이 타우(Tau) 응집을 방지한다면?
- "아밀로이드-타우 연결 푸는 작업이 알츠하이머 신약개발의 열쇠"
- 기억 형성의 미스터리: 뇌는 정보를 어디에 어떻게 저장하나
- "희귀질환 유발 '융합 단백질을 삭제하는 치료제' 필요"
- C-Met-ADC와 C-Met-TPD… 어느 약물이 더 경쟁력 있을까

