특별기고 |
배진건(이노큐어 테라퓨틱스, 수석부사장)

역학 연구에 따르면 제2형 당뇨병 환자(T2DM)의 알츠하이머병(Alzheimer Disease, AD) 발병 위험이 2~4배 높다는 것은 잘 알려져 있다. 하지만 그 이유는 아직도 현재 진행형 연구 분야이다.
연구자들에게 "제2형 당뇨병과 AD가 밀접한 관련이 있다고 믿는 이유가 무엇이냐?" 물으면 대부분 '염증' 다음으로 '인슐린 저항성' 때문이라고 답한다. 인슐린 저항성으로 인해 세포가 인슐린을 비효율적으로 이용해 혈액 속 당이 쌓이고 뇌가 당으로부터 영양분을 제때 공급받지 못해 인지기능이 저하되기 때문이라고 설명한다. '염증'과 '인슐린 저항성'만이 답일까?
Wake Forest University School of Medicine의 과학자들은 증가된 설탕 섭취와 그로인한 혈당 상승이 AD의 위험을 증가시키는 뇌의 아밀로이드-베타(Aβ) 플라크 축적을 유발하기에 충분하다는 새로운 메커니즘을 발견했다. 연구 결과는 'Journal of Clinical Investigation(JCI) Insight'에 "KATP channels are necessary for glucose-dependent increases in amyloid-β and Alzheimer’s disease–related pathology"라는 제목으로 5월 21일 온라인(online)에 먼저 실렸다.
Wake Forest 연구자들은 AD 위험에 빠질 가능성이 높거나 미래에 AD 진단을 받게 될 개인의 뇌에서 이미 진행되고 있는 당뇨병의 대사 변화를 더 잘 이해하기 위하여 연구를 진행했다. 연구팀은 먼저 생쥐 모델을 이용해 간단한 비교 실험을 진행하였다.
일반 식수를 제공한 생쥐보다 설탕물을 준 생쥐의 뇌에서 Aβ 플라크가 더 많이 형성된다는 사실을 먼저 관찰했다. 간단한 비교 실험을 통해 설탕 섭취 증가가 혈관의 혈당 상승뿐만 아니라 AD의 특징적인 징후인 뇌의 Aβ 플라크 증식으로 이어지고 있음을 발견했다. "이 발견은 너무 많은 설탕을 섭취하는 것이 Aβ 플라크 증식을 일으키고 AD의 위험을 증가시키기에 충분하다는 것을 보여주기 때문에 이 연구 결과가 중요하다."라고 연구를 주도한 Macauley 교수는 설명한다.

이 현상은 분홍색 설탕(pink sugar)으로 만든 뇌를 보여준다(핑크 브레인). 분홍색 설탕의 분자 동인(the molecular drivers)을 더 잘 이해하기 위해 연구팀은 신경 발화(neuronal firing) 및 Aβ 생성과 신진 대사 변화를 연결하는 신경세포의 대사 센서를 식별했다.
ATP-민감성 칼륨 채널(ATP-sensitive potassium channels, KATP 채널)은 Aβ 및 AD 관련 병리학에서 포도당 의존성 증가에 필요하다. 상승된 혈당 수치 또는 고혈당증은 뇌의 흥분성(brain excitability)과 Aβ 방출을 증가시켜 제2형 당뇨병과 AD 사이의 기계적인 연결을 제공할 수 있다. 이 관계를 지배하는 세포 메커니즘이 제대로 이해되지 않기 때문에 연구자들은 에너지 가용성의 변화와 세포 흥분성을 결합시키는 ‘ATP 민감성 칼륨(KATP) 채널’이 AD 병인에서 역할을 하는지 여부를 조사했다.
이 식별 과정에서 뉴런 KATP 채널의 구체적인 역할을 밝혔다. 이 채널은 건강한 정상적인 기능을 위해 얼마나 많은 에너지를 사용할 수 있는지 감지한다. 이러한 감지 센서를 방해하면 뇌가 정상적으로 작동하는 방식부터 변경된다.
연구팀은 유전자 조작 기술을 사용하여 생쥐의 뇌에서 이러한 센서를 제거하면 혈당 상승이 더 이상 Aβ 생성이나 Aβ 플라크 형성을 증가시키지 않는다는 것을 먼저 보여주었다. 다음으로 연구진은 인간 AD 뇌에서 이러한 대사 센서의 발현을 조사하고 확인하였다.
KATP 채널 소단위 Kir6.2/KCNJ11 및 SUR1/ABCC8이 인간 뇌의 흥분성 및 억제성 뉴런에서 발현되었고 KCNJ11 및 ABCC8의 대뇌 피질 발현이 인간 및 마우스에서 AD 병리학에 따라 이러한 채널의 발현이 증가한다는 사실을 다시 확인했다.
다음으로 뇌 아밀로이드증 및 신경 KATP 채널 제거(즉 아밀로이드 전구체 단백질[APP]/PS1 Kir6.2 -/- 생쥐)한 모델에서 급성 및 만성 패러다임을 모두 사용하여 Kir6.2-KATP 채널이 Aβ의 간질 액 수준의 고혈당 의존성 증가, APP의 아밀로이드 생성 처리 및 젖산 염(lactic acid) 방출에 의존할 수 있는 Aβ 플라크 형성을 조절하는 대사 센서임을 입증하였다(Graphic Abstract).
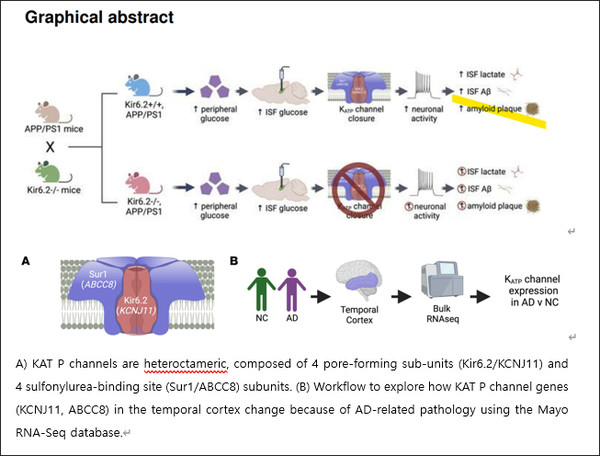
그렇기에 이번 연구는 Kir6.2-KATP 채널의 AD 발병에 잠재적인 새로운 역할을 확인하고 Kir6.2-KATP 채널의 약리학적 조작이 당뇨병 또는 당뇨병 전단계(prediabetic) 환자에서 Aβ 병리를 감소시키는 데 치료적 가능성을 가지고 있음을 시사한다.
당신은 얼마나 많은 양의 설탕을 섭취하시나요? 너무 많은 설탕을 섭취하면 Aβ 플라크 증식을 유도하고 AD의 위험을 증가시키기에 충분하기에 설탕 섭취를 유의 깊게 짚어보아야 한다. 'Sweet'은 달콤하지만 위험에 빠뜨리게 한다.
관련기사
- 아밀로이드 플라크를 제거한 뒤 롱텀 결과는 무엇일까?
- 신경독성 높은 타우(tau) 조절 물질 Numb '베일 벗어'
- 여성은 왜, 남성보다 알츠하이머 환자가 많은가
- 좋은 콜레스테롤(HDL)은 알츠하이머 친구인가, 적인가
- "PLD가 세포막에서 영역 넓혀 알츠하이머 치매(AD)로 이동한다"
- 타우린 부족은 노화를 촉진시키는 주범인가
- 간-뇌 연결축(Liver-Brain Axis)을 아시나요?
- "AI, CRISPR의 RNA-타깃팅 효과 예측하고 유전자치료에 혁명을..."
- K바이오! 당신은 '강제혁신' 할 것인가, 당할 것인가
- "아밀로이드-타우 연결 푸는 작업이 알츠하이머 신약개발의 열쇠"
- 24살 더 오래 살 수 있게 만드는 '8가지 습관'
- PLCγ2 M28L 변형, 기억상실 악화…P522R은 신경 보호 촉진

