13개 제약 자누메트엑스알서방정 후발약 허가, 수탁사 대화제약
대화제약이 수탁 생산하는 한국MSD '자누메트엑스알서방정' 후발약 허가가 줄을 이었다.
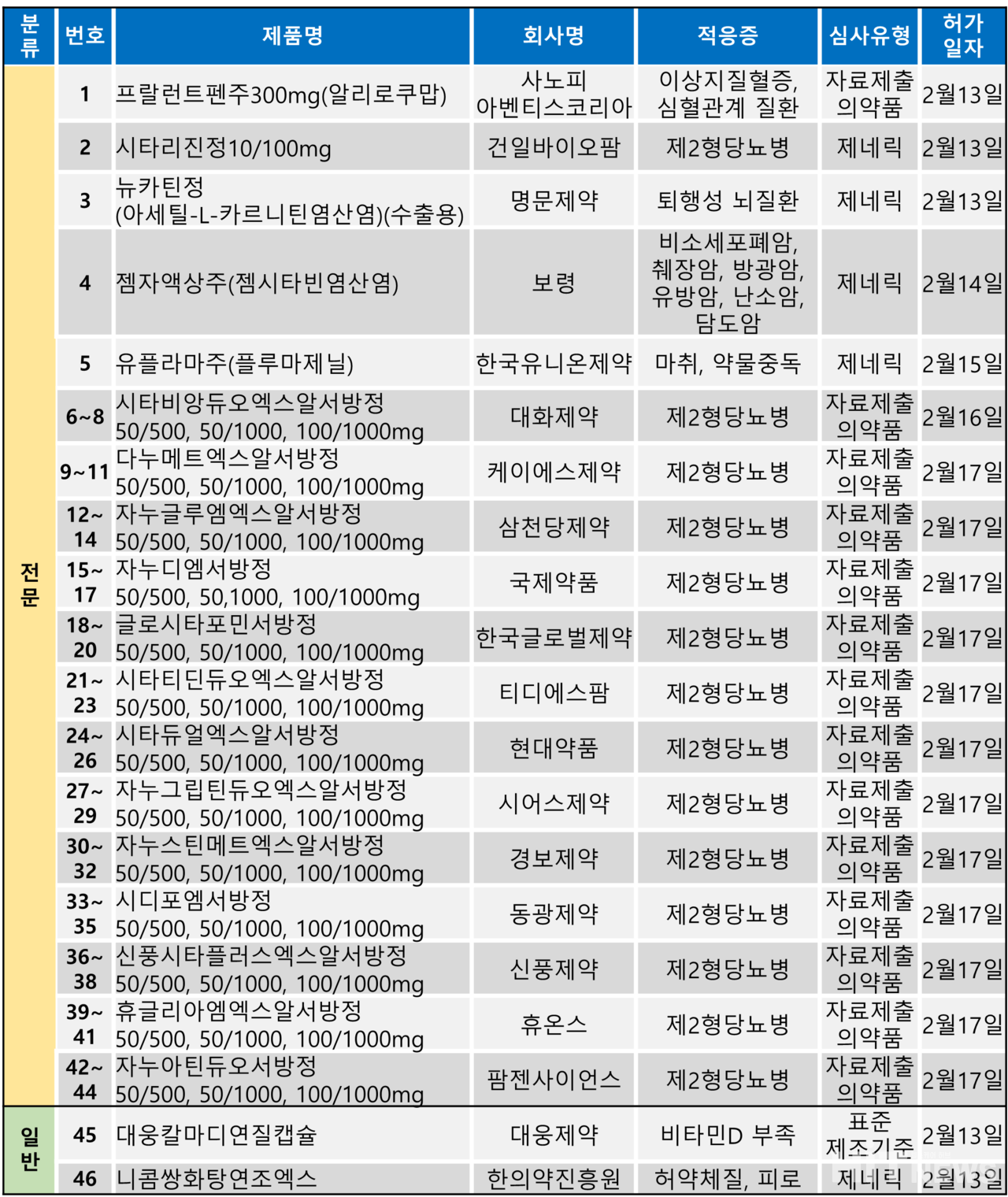
지난 주(2월 13~17일)에는 총 46개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 44건, 일반의약품은 2건이었다.
대화제약은 지난 16일 DPP-4 억제제 성분 제2형당뇨병 치료제인 시타글립틴, 메트포르민 복합제 '시타비앙듀오엑스알서방정'을 허가 받았다. 이 의약품은 오리지날인 자누메트엑스알서방정의 염변경 제제다.
뒤이어 17일 △케이에스제약 △삼천당제약 △국제약품 △한국글로벌제약 △티디에스팜 △현대약품 △시어스제약 △경보제약 △동광제약 △신풍제약 △휴온스 △팜젠사이언스 등 12개 제약사의 허가 또한 이어졌다.
이 제제들은 모두 대화제약 횡성 제1공장에서 생산되는 위·수탁 품목이다.
각 제약사들은 50/500mg(시타글립틴/메트포르민), 50/1000mg, 100/1000mg 등 3개 용량의 허가를 받았다.
작년 5월 일차적으로 '자누메트엑스알서방정'의 염변경 후발약이 꼬리를 물고 허가됐었다. 당시 지엘팜텍 '지누메트엑스알서방정'과 신일제약 '자누메티아엑스알서방정', 일동제약 '시타콤비엑스알서방정', 한국휴텍스제약 '나누메트엑스알서방정' 등이 허가를 받은 바 있다.
또한 신일제약은 △동구바이오제약(글리시타메트엑스알서방정) △하나제약(시타원플러스엑스알서방정) △동국제약(시타칸메트서방정) △동화약품(시트디엠메트서방정) △유영제약(유시타메트엑스알서방정) △비보존제약(이글립틴엑스알서방정) △대웅바이오(자누다움엑스알서방정) △대원제약(자누리틴콤비서방정) △아주약품(프로메트엑스알서방정) △삼진제약(하누비엠엑스알서방정) 등의 제품도 수탁생산한다. 이들 역시 작년 5월 10일과 11일에 걸쳐 모두 허가됐다.
이들은 2016년 시타글립틴과 메트포르민복합제 우판판매품목허가권(이하 우판권)을 지정받은 종근당 '시타폴민엑스알서방정' 및 한미약품 '시타메폴엑스알서방정'과는 다른 염 성분 제제다. 즉, 2024년 6월 1월까지로 확보한 우판권 영향에서 벗어나 시타글립틴 특허존속기간만료 일인 2023년 9월 1일 이후부터 바로 발매 가능하다.
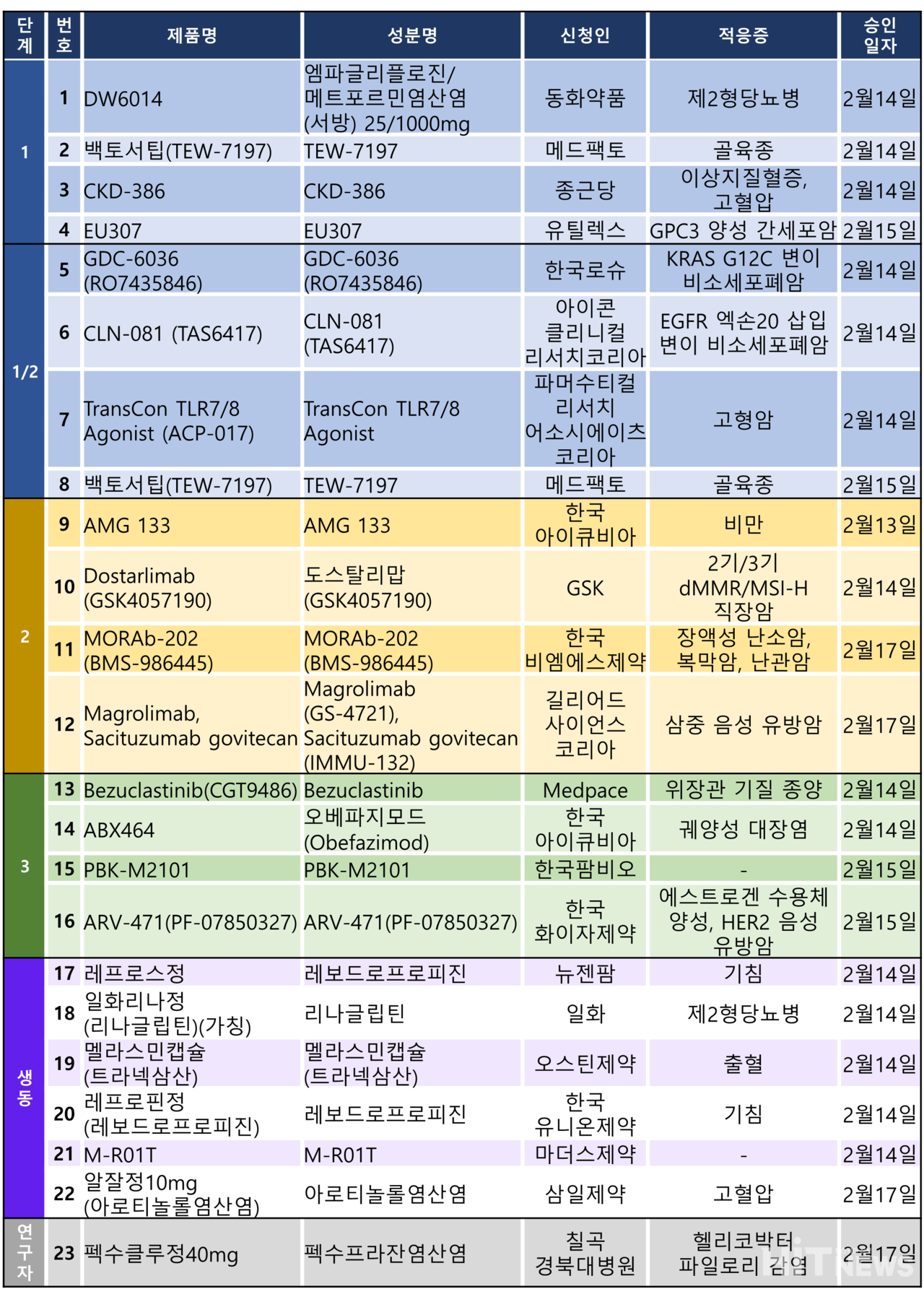
지난주 임상시험계획은 총 23건이 승인 완료됐다. 세부적으로 △1상 4건 △1/2상 4건 △2상 4건 △3상 4건 △생동 6건 △연구자임상 1건 등이다.
이 임상시험들은 제2형당뇨병, 고혈압, 이상지질혈증, 비만, 궤양성 대장염 등 다양한 질환과 골육종, GPC3 양성 간암, KRAS G12C 변이·EGFR 엑손 20삽입 변이 비소세포폐암, 고형암, 삼중 음성 유방암 등 다양한 암종을 대상으로 승인됐다.
화이자와 미국 바이오기업 아르비나스(Arvinas)가 공동개발중인 경구용 PROTAC(표적 단백질 분해 기술) 제제인 ARV-471의 3상 임상시험계획이 승인됐다.
양사는 이 치료제 개발을 위해 2021년 7월부터 개발 및 판매 계약을 체결했다. 당시 아르비나스 존 휴스턴 CEO는 ARV-471 개발에 있어 자사의 PROTAC 기술을 활용할 것이라고 말한 바 있다.
이번 임상시험은 '진행성 질환에 대해 이전에 내분비 기반 치료를 받은 후 질환이 진행된 에스트로겐 수용체(HR) 양성, HER2(사람 상피세포 성장인자수용체2) 음성 진행성 유방암' 환자를 대상으로 한다. 대조약은 선택적 에스트로겐 수용체 분해제(SERD, Selective Estrogen Receptor Degrader)인 한국아스트라제네카의 파슬로덱스(성분 풀베스트란트)다.
시험 기관은 △가톨릭대 서울성모병원 △국립암센터 △분당서울대병원 △이대 목동병원 △길병원 △연세대 강남세브란스병원 △연세대의대 세브란스병원 △아주대병원 △서울아산병원 △서울대병원 △삼성서울병원 △고려대의대부속병원 등 12개 병원이다.
한편 유방암은 HR과 HER2의 여부에 따라 4가지 유형으로 구분할 수 있다. 그 중 HR+/HER2- 환자는 전체 유방암 환자의 73%를 차지할 정도로 많은 비중을 차지한다.

