허가후 변경 심사, 약효동등성과→의약품규격과 등으로 변경

원료의약품과 완제의약품 연계 허가심사가 시행되면서 식품의약품안전처 업무조정이 이뤄지고 있다. 전문성 확보를 위한 조치다.
16일 식품의약품안전평가원 의약품심사부에 따르면 제조방법 변경이 없는 주성분 제조원 변경(추가)의 동등성 시험자료 심사를 내달 1일부터 의약품규격(제네릭)과와 첨단의약품품질심사과(신약, 자료제출약)에서 맡는다.
또한 시험약의 제조공정에 대한 상세자료 대신 제조방법 변경이 없다는 확인서를 제출하도록 업무가 개선된다.
허가 후 변경은 약효동등성과에서 심사를 담당했으나, 주성분과 완제약의 연계심사 전문성 확보를 위해 의약품규격과와 첨단의약품품질심사과에서 담당하기로 했다. 내달 1일 접수 민원부터다.
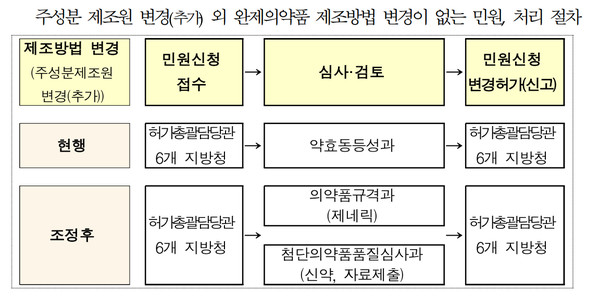
즉, 현행은 변경 전·후 제조원의 주성분으로 완제약을 제조해 각각 대조약과 시험약의 비교용출시험 자료(기시조건 또는 3조건)를 제출하면, 대조약(변경전)과 시험약(변경후)의 제조방법을 제조지시기록서 또는 CTD 자료로 확인·비교 후 제조방법 변경 시 관련규정에 따라 검토하고 있다.
하지만 개선안에 따라 대조약과 시험약의 적절성 여부를 판단하기 위해 허가사항에 따른 제조방법을 검토하되, CTD 자료를 통해 확인한다.
다만, 주성분제조원 추가외 완제약 제조방법 변경이 없는 경우 제조공정에 변경이 없다는 확인서를 제출해야 한다.
이와 함께 소화기관용약의 안전성·유효성 심사는 종양항생약품과에서 담당했으나 약효동등성과로 변경된다. 15일부터 적용되면서 기접수 민원은 이관된다.
관련기사
이현주 기자
hjlee@hitnews.co.kr
폭 넓은 취재력을 바탕으로 제약산업과 건강보험정책 사이 퍼즐찾기에 주력하고 있습니다.

