식약처, 민원설명회 통해 밝혀..."자사제품 품질관리 의무 업체에"
원료의약품 불순물 안전관리 책임이 업체에게 돌아간다.
모든 합성 원료 및 완제의약품 제조·수입업체는 자체 NDMA(N-니트로소디메틸아민), NDEA(N-니트로소디에틸아민), NMBA(N-니트로소엔메칠아미노부틸산) 등 니트로소아민류 불순물 발생 가능성에 대한 평가 및 시험을 진행해야 한다.
구체적으로 발생가능성 평가결과는 2020년 5월까지, 시험결과는 2021년 5월까지 식약처에 보고해야 한다. 검출되지 않았거나 즉시 시험이 불필요하다는 걸 확인하기 위한 품목 결과를 보고해야 한다.
합성 원료의약품 안전관리 문제는 발사르탄과 라니티딘, 니자티딘까지 이어지면서 정부 당국의 관리범위와 속도를 벗어났다. 앞으로 제조물 책임의 관점에서 업체별 자체평가 및 시험을 지시하는 것으로 식약처가 결론 낸 것으로 보인다. 국제적으로도 전체 원료의약품의 자체 조사를 규제기관이 업체에게 지시했다는 설명이다.
식약처 의약품연구과 김영주 사무관은 서울 삼정호텔에서 개최한 '의약품 등 제조·수입자 민원설명회에서 이같이 설명했다.

김 사무관은 "이번 대책의 큰 요점은 '즉시보고'다. 발사르탄, 라니티딘, 니자티딘 모두 기관이 주도했다. 우리 나름대로 조사했지만, 사실 현재 업계가 제일 잘 알고 자기 제품에 대한 품질관리 의무도 있다. 필드에 있는 분들이 평가도, 조사도 해달라는 뜻"이라고 했다. 발생가능성을 평가하다가 이상 결과가 나오면 즉시 보고해달라는 의미다. GMP와 기시법(기준및시험법) 자료에 불순물 규정을 넣을 수도 있다고 했다.
업체는 발생가능성 평가 중 NDMA 등 불순물 발생 가능성이 있는 '주성분' 원료가 있다면 즉시 시험을 실시해 정량한계 이상 검출 시 식약처에 즉시 보고해야 한다. 화학 합성하는 원료로 DMF 등록, 품목허가 신고, 자사제조용 수입품목 주성분 원료면 된다. 모든 주성분에 대해 시험하는 것이 아니라 발생가능성 평가 결과 가능성이 있는 원료만 시험하면 된다.
단, 생산·수입 실적이 없는 원료도 평가 대상인데 이참에 실적없는 원료를 자진취하한다면 대상에서 제외된다. 잠정관리기준이 있는 5개의 원료에 대해서는 불순불 발생가능성을 평가한다.
시험검사는 자사 시험실 실시 또는 위탁(국내 GMP업체, 시도보건환경연구원, 식약처 지정 시험검사기관)하라는 게 식약처의 설명이다. 해외 제조원이 발행한 성적서는 인정되지 않는다. 시험법은 식약처 및 해외 규제기관 공개 시험법을 활용해야 한다.

원료약의 경우 공정개선 시 제조공정, 사용물질 등 변경 시 등록 및 허가신고사항 변경을, 완제약의 경우 주성분 제조원 변경 등을 할 때 품목허가신고사항을 2022년 5월까지 식약처에 보고해야 한다.
김 사무관은 "원료 발생가능성 평가표는 6가지, 완제 발생가능성은 원료 평가자료로 갈음해 완제는 2가지를 더 해 8가지를 내면 된다"고 했다.
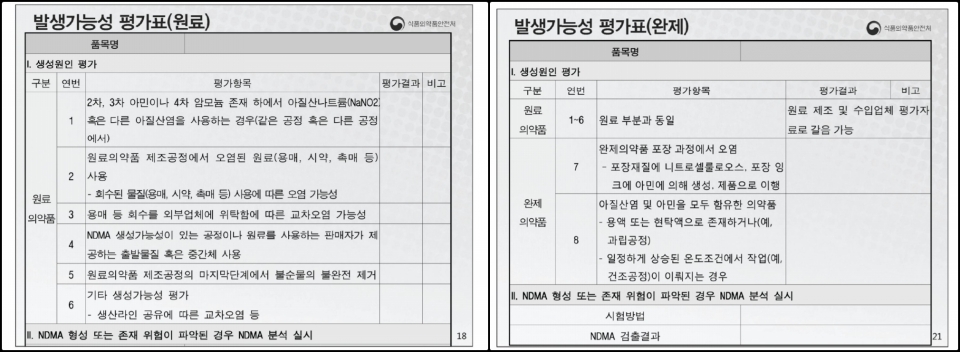
원료는 ▶ 2·3차 아민이나 4차 암모늄 존재 하에 (같은 공정 혹은 타 공정에서) 아질산나트륨(NaNO2) 혹은 다른 아질산염을 사용하는 경우 ▶ 원료약 제조공정에서 오염된 원료(용매, 시약, 촉매 등)를 사용하거나 회수된 물질(용매, 시약, 촉매 등) 사용에 따른 오염 가능성 ▶ 용매 등 회수를 외부업체에 위탁해 발생할 교차오염 가능성 ▶ NDMA 생성가능성이 있는 공정이나 원료를 사용하는 판매자가 제공하는 출발물질 혹은 중간체 사용 ▶ 원료약 제조공정의 마지막단계에서 불순물 불완전 제거 ▶ 생산라인 공유 등 기타 생성가능성을 평가해야 한다. 이를 내년 5월 31일까지 내야하는데, 요약된 평가결과만 내면 된다는 게 김 사무관의 설명.
완제의 경우 원료 평가항목은 원료 제조 · 수입업체 평가자료로 갈음 가능하다. 단 주성분들 중 합성 원료가 하나라도 있으면 대상이 된다. 세부적으로는 완제약 포장 재질에 니트로셀룰로오스, 포장 잉크에 아민에 의해 생성되는지, 과립공정이나 건조공정 등 아질산염 및 아민을 모두 함유한 의약품을 평가해야 한다.
식약처는 업체들이 국내외 규제기관 홈페이지, 언론정보, 관련 문헌 검색 등을 통해 취급하는 원료 및 완제약에 대한 불순물 정보 등을 검색하도록 권유했다. 유럽과 캐나다도 내년 3월과 4월까지 업체들에게 전체 원료약 자체 조사를 지시한 바 있고, NDMA 등 불순물이 불검출을 목표로 한다고 공표했다.
식약처는 라니티딘이 자체 분해돼 NDMA가 생길 줄 몰랐던 게 사실이라며 원료 제조업체들이 자사 원료에 대해 연구해야 한다고 했다. 또 NDMA 등 불순물 발생가능 물질을 지속적으로 연구 중이라는 설명이다.
외국은 민간 약국체인 연구소, 분석기기 제조판매업체들도 등 발생 가능 물질에 대해 시험하고 있는 상황이다. 김 사무관은 국내에선 먹는 물에도 NDMA, NDEA 기준이 있는데 관련 논문을 찾아보는 것도 추천한다고 했다.
김 사무관은 "환자들의 안전을 위해 식약처가 불순물을 어디까지 안전할 것인가 기준을 잡아야 한다. 특히 이런 물질이 의약품에선 나와서 안 된다는 게 추세"라며 "의약품에 NDMA가 일정함량 나오는 것 자체를 제한하겠다. 이 방향성을 업계도 알아달라"고 했다.
관련기사
- 원료약 불순물 관리 돌고돌아 결국 업체 몫으로...
- "수입약 해외제조소 실사 거부하면 수입중단"
- "니자티딘 시험법, 범용성·적용 가능성 최우선적 고려"
- 티딘 계열 NDMA 조사는 니자티딘으로 “끝”
- NDMA 잡겠다는 식약처 대안이 ‘투망식’ 전수조사라니
- "NDMA 니자티틴 발암?...고속터미널서 2시간 있는 게 더 위험"
- 순간랭킹 1위 "니자티딘 NDMA"...빈대잡다 외양간 태울라
- 니자티딘에서도 NDMA 검출, 회수포함 대응조치 곧 발표
- "NDMA 검출 즉시, 보고...제품은 업체가 잘 안다"
- 미·EU, 메트포르민 'NDMA' 조사… 식약처도 '예의주시'
- "식약처 메트포르민 불순물 직접 조사… 시험법 마련 중"
- 불순물 자체조사 할 제약업계 "식약처에 질문 쏟아"
- EMA, NDMA 조사보고 10월까지 연장...식약처는?
- 회수 '라니티딘' 국내사 간 법정 다툼으로 번지나
- 불순물 발생가능성 평가 보고서 제출 5월→12월로 연장
- 재판부가 물었다… 발사르탄 불순물 검출로 보험자가 피해봤나?

