전문의약품 915개 품목, 일반의약품 426개 품목 허가
전문의약품은 자료제출의약품 435개, 제네릭 399개 순으로 많아
자체 개발 국산신약은 '0개'로 이쉬움 남겨

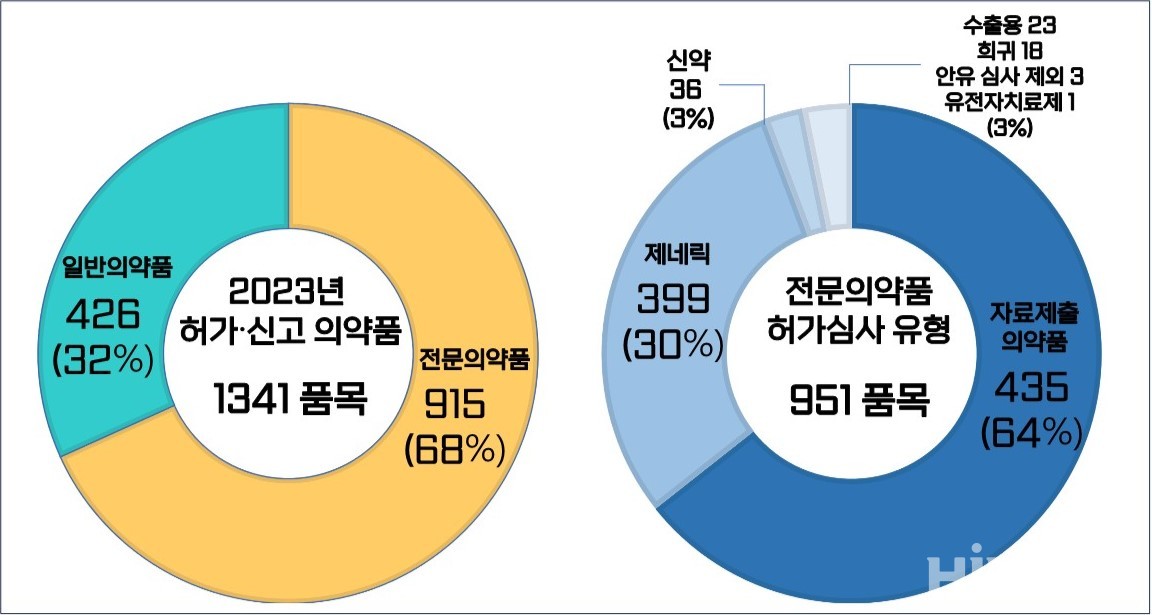
식품의약품안전처 '의약품안전나라' 데이터를 분석한 결과, 작년 식약처를 통해 허가ㆍ신고(이하 허가)된 의약품 품목 수(수출용 의약품 포함, 한약재 미포함)는 총 1341개로 집계됐다. 작년 허가된 1565개 의약품 품목 수의 약 86%에 해당하는 기록이다.
전체 허가 품목 중 전문의약품은 915개(68%), 일반의약품은 426개(32%) 품목이었다. 전문의약품을 허가 심사 유형에 따라 살펴보면 △신약 36개 △자료제출의약품 435개 △희귀 18개 △유전자치료제 1개 △제네릭 399개 △안유(안전성ㆍ유효성) 심사 제외 3개 △수출용 23개 등이었다.
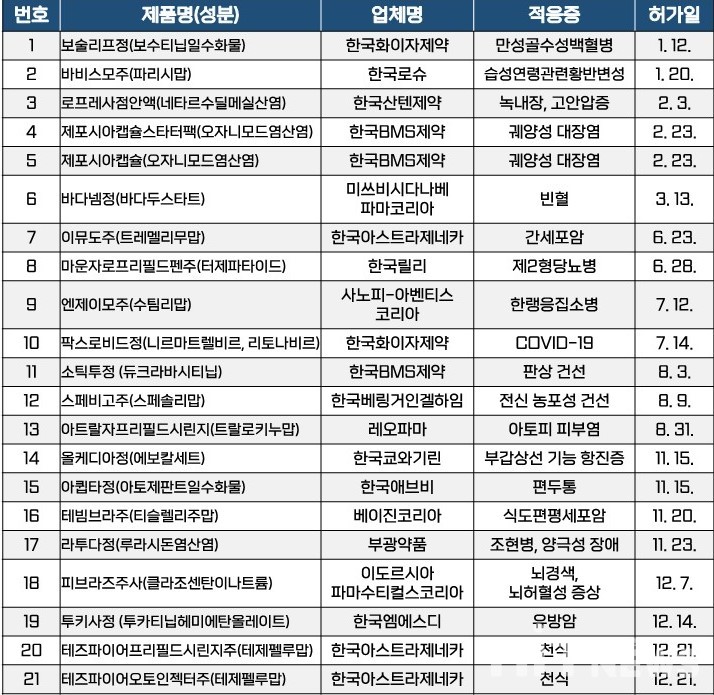
작년 허가된 신약은 총 36개 품목으로, 2022년 23개 품목에 비해 약 57% 증가했다. 제품으로 구분해 보면 △보술리프정(한국화이자제약, 1월 12일) △바비스모주(한국로슈, 1월 20일) △로프레사점안액(한국산텐제약, 2월 3일) △제포시아캡슐스타터팩(한국BMS제약, 2월 23일) △제포시아캡슐(한국BMS제약, 2월 23일) △바다넴정(미쓰비시다나베파마코리아, 3월 13일) △이뮤도주(한국아스트라제네카, 6월 23일) △마운자로프리필드펜주(한국릴리, 6월 28일) △엔제이모주(사노피-아벤티스코리아, 7월 12일) △팍스로비드정(한국화이자제약, 7월 14일) △소틱투정(한국BMS제약, 8월 3일) △스페비고주(한국베링거인겔하임, 8월 9일) △아트랄자프리필드시린지(레오파마, 8월 31일) △올케디아정(한국쿄와기린, 11월 15일) △아큅타정(한국애브비, 11월 15일) △테빔브라주(베이진코리아, 11월 20일) △라투다정(부광약품, 11월 23일) △피브라즈주사(이도르시아파마수티컬스코리아, 12월 7일) △투키사정(한국엠에스디, 12월 14일) △테즈파이어프리필드시린지주(한국아스트라제네카, 12월 21일) △테츠파이어오토인젝터주(한국아스트라제네카, 12월 21일) 등 21개 제품이다.
다만, 라이선스 인(L/I) 계약 등을 통해 허가 받은 것이 아닌 고유 국산 기술로 개발한 신약은 0건에 그쳤다. 2022년에는 △스카이코비원멀티주(SK바이오사이언스, 국산신약 35호) △엔블로정(대웅제약, 국산신약 36호) 등 2개 제품이 국산신약으로 허가된 바 있다.
작년 자료제출의약품 허가 품목 수는 예년에 비해 상당 부분 감소를 보였다. 자료제출의약품은 기존 허가 의약품의 염기ㆍ제형 등을 변화시킨 제제로, 안전성 및 유효성 자료를 제출해야 하는 의약품을 말한다.
2023년 자료제출의약품 유형으로 허가된 품목은 435개로, 2022년 595개와 비교할 때 약 73%에 그쳤다. 다양한 허가 자료제출의약품 중에서도 제2형 당뇨병과 고혈압 치료제의 비중이 컸다. 보령의 카나브(성분 피마사르탄), 한국아스트라제네카의 포시가(성분 다파글리플로진) 등 기존 오리지널 약들의 특허가 만료됨에 따라, 해당 성분을 포함한 복합제들이 줄지어 허가되기도 했으며, TZD(티아졸리딘디온)ㆍDPP-4 억제제ㆍSGLT-2 억제제 등 제2형 당뇨병 치료 성분의 새로운 조합 복합제가 다수 출시되기도 했다.
한편, 유전자치료제로 허가된 품목은 한국얀센이 개발한 '카빅티주(성분 실타캅타젠오토류셀)' 1개 품목뿐이었다. 식약처는 카빅티를 이전에 △프로테아좀 억제제 △면역조절제제 △항-CD38 항체를 포함해 적어도 4가지 치료를 받은 재발 또는 불응성 다발골수종 환자를 대상으로 허가했다.
카빅티는 환자의 면역세포인 T세포에 B세포 성숙항원(BCMA)을 인지할 수 있는 유전정보를 넣어준 후 다시 이 T세포를 환자의 몸에 주입하는 항암제다. BCMA는 항원과 T세포의 자극에 의해 대량의 항체를 분비하는 B세포의 형질 세포 분화 중에 선택적으로 발현된다. 이 항원은 다른 주요 기관에서는 발현하지 않아 형질 세포암인 다발골수종에 대한 이상적인 표적으로 알려져 있다.
관련기사
- [허가/임상]부광, 조현병 신약 '라투다' 허가…베링거, 비만약 3상승인
- [허가/임상]릴리, 2형 당뇨 '마운자로' 허가…당뇨·비만 치료제 3상
- [허가/임상] 간암신약 '이뮤도주' 허가, '올루미언트' 소아 탈모 3상
- [허가/임상] 다발골수종 CAR-T 카빅티, 빈혈 바다넴 허가
- [허가/임상] 포시가·직듀오 후발약 강세... 황반변성 '바비스모' 허가
- [허가/임상] 4월출시 막차 탄 '포시가' 후발, 11년 기다린 '보술리프'
- 식약처, 한·미 AI 규제 심포지엄 준비 착착...준비기획단 출범
- 올해 6월부터 마약류 복용하면, 병의원에서 다 안다
- 히트뉴스 선정, 2024년을 뜨겁게 달굴 제네릭의약품들
- 지난해 국산신약 0건… "K-제약바이오, 조바심 내지마 잘하고 있어"
- 애브비, '아큅타' 삽화성 편두통 대상 3상 결과 '란셋 뉴롤로지' 게재
- 테빔브라, 식도편평세포암 2차 치료제로 FDA 허가
- 한독, 넥세라파마 '피브라즈' 국내 독점 유통 계약
- 애브비 '아큅타', 편두통 일수와 급성 약물 사용 감소시켜

