3월 중 美 FDA에도 IND 신청 예정
한미약품(대표 박재현)은 지난달 29일 식품의약품안전처에 국내 성인 건강인 및 비만 환자를 대상으로 'HM15275(개발코드명)'의 안전성과 내약성, 약동학, 약력학 특성 등을 평가하는 임상시험계획(IND)을 제출했다고 8일 밝혔다. 한미약품은 식약처에 이어 3월 중 미국 식품의약국(FDA)에도 IND를 제출할 계획이다.
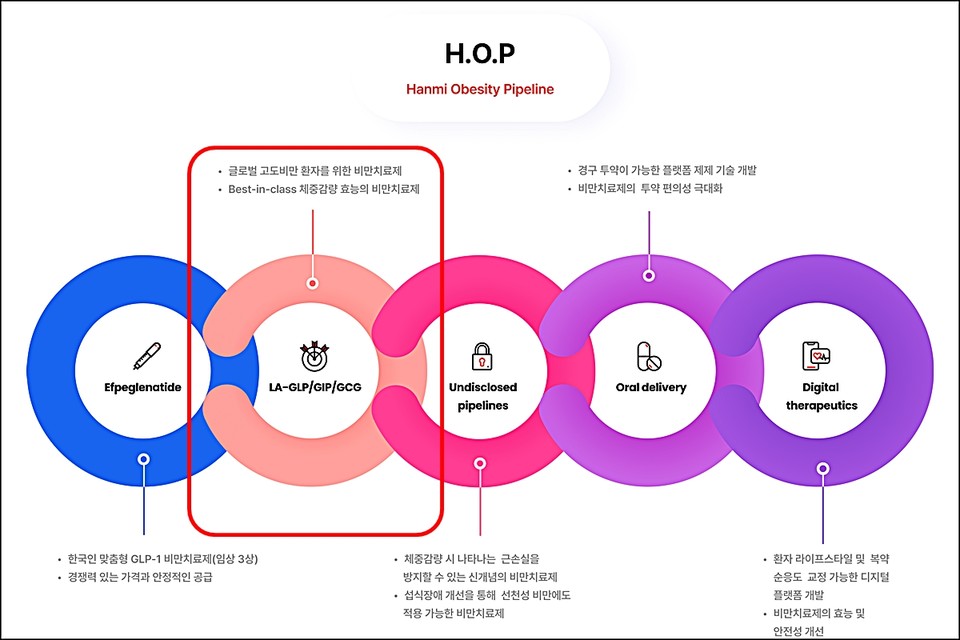
HM15275는 한미약품의 전주기적 비만 치료 신약 프로젝트인 'H.O.P(Hanmi Obesity Pipeline)'에 포함된 혁신신약 후보물질이다. 현재 임상 3상 개발이 진행 중인 '에페글레나타이드'를 이어나갈 신약이다.
회사 측에 따르면 HM15275는 한미약품의 기존 바이오신약 플랫폼인 '랩스커버리'가 아닌 '아실레이션(Acylation)' 기술이 적용된 비만 신약이다. 글루카곤 유사 펩타이드(GLP-1)와 위 억제 펩타이드(GIP), 글루카곤(GlucagonㆍGCG) 등 각각의 수용체 작용을 최적화해 비만 치료에 특화되며, 부수적으로 다양한 대사성 질환에 효력을 볼 수 있도록 설계된 것이 특징이다.
GLP-1 수용체 작용제는 포만감을 증가시켜 체중을 감소시키고, 인슐린 분비와 감수성을 개선해 혈당 조절을 원활하게 한다. GIP는 GLP-1 수용체 작용제의 약리학적 이점을 향상시키는 한편, 메스꺼움과 구토ㆍ설사 등 이 작용제의 일반적인 위장관 부작용을 완화할 수 있다. GCG는 포만감 조절과 함께 에너지 소비 및 지질 대사 조절에도 관여한다.
이 3가지 약리작용을 적절히 활용하면 비만뿐만 아니라 제2형 당뇨병 및 심혈관 질환에 대한 치료 잠재력을 극대화할 수 있다는 게 한미약품 측 설명이다. HM15275가 우수한 체중 감량 효능은 물론, 심혈관 및 신장 질환에 대한 개선 효과를 나타내는 '차세대 비만치료제'가 될 것으로 기대하고 있다고 회사 측은 덧붙였다.
앞선 비임상 연구에서 HM15275는 근 손실은 최소화하면서도 수술적 요법에 따른 체중 감량 효과에 효능은 물론 다양한 대사질환 모델에서 기존 비만 치료제 대비 우수한 치료 효능을 입증했다고 회사 측은 설명했다.
한미약품 관계자는 "HM15275에는 회사가 인크레틴 분야에서 20년 이상 연구를 지속하면서 축적한 연구 지식과 노하우들이 집약돼 있다"며 "기존 치료제의 한계를 극복하고 효과를 혁신적으로 높이는 차세대 비만 치료제 개발을 완수할 수 있도록 최선을 다하겠다"고 말했다.
한편 한미약품은 오는 6월 미국에서 열리는 2024 미국당뇨병학회(ADA)에서 HM15275에 대한 여러 건의 주요 연구 결과를 발표할 예정이다.
관련기사
- 한미약품 제10회 빛의 소리 나눔 콘서트 성황리 마쳐
- 한미그룹은 연구원만 28%…인적자원 업계 '최고'
- 한미그룹, '디지털 헬스케어' TF 통해 본격 비즈니스 나서
- 한미약품 "'펜탐바디' 적용 차세대 면역항암제 1상 환자 투약 시작"
- 한미그룹 "경영권 매각 없는데 프리미엄? 악의적인 통합 왜곡 유감"
- 한미약품 고지혈증 복합제 '로수젯', 1월 원외처방액 '챔피언' 등극
- "비만 유병률↑… 경제적 손실·계층 양극화 막는 방안 필요"
- 한미그룹, 국내 특허 등록 수·의약품 등재 특허 수 제약업계 1위 등극
- 한미약품, 대한비만학회서 자사 당뇨병 치료제 유용성 소개
- "멈추지 않는 한미 R&D 혁신"… AACR서 업계 '최다' 연구과제 발표
- 한미약품 ‘아모잘탄패밀리’ 4상 결과 국제학술지 ‘AHJ’ 등재
- Hanmi Pharma Unveils 10 New Research Projects at AACR 2024
- 한미약품, 차세대 비만 치료 삼중작용제, FDA에 임상 1상 승인 신청

