식약처 승인 후 2개월 반 만에 순항… 한국서 420명 모집
한미약품(회장 송영숙)은 국내 성인 비만 환자를 대상으로 이달 초 '에페글레나타이드'의 유효성 및 안전성을 평가하는 3상 임상시험에 참가할 첫 환자를 등록했다고 15일 밝혔다.
한미약품이 작년 10월 23일 식품의약품안전처로부터 3상 임상시험계획을 승인받은 후 약 2개월 반 만에 속도감 있게 최초 임상시험 대상자 등록을 이뤄낸 것이라는 게 회사 측 설명이다. 향후 임상시험 대상자 모집에 더욱 탄력이 붙을 것으로 전망된다고 회사 측은 덧붙였다.
3상 임상시험은 국내 대학병원에서 당뇨병을 동반하지 않은 성인 비만 환자 420명을 대상으로 무작위 배정, 이중 눈가림, 위약 대조, 평행 비교 방식으로 진행된다. 임상 종료는 2026년 상반기로 예상되며, 앞으로 3년 내 국내에서 상용화될 것으로 기대된다.
에페글레나타이드는 한미약품의 독자 플랫폼 기술 '랩스커버리'가 적용된 장기 지속형 GLP-1 제제다. 과거 파트너사였던 사노피가 진행한 다수의 글로벌 임상을 통해 약물의 혁신성을 입증받은 바 있다. 특히 대규모 글로벌 임상 3상에서는 체중 감소와 혈당 조절 효력을 확인했을 뿐만 아니라 주요 심혈관계 및 신장 질환 발생률을 유의미하게 감소시켜 세계적인 학술지 '뉴잉글랜드 저널 오브 메디슨(NEJM)' 등 다수의 학술지에 결과가 등재됐다.
에페글레나타이드는 한미약품의 최첨단 바이오의약품 전용공장인 '평택 스마트플랜트'에서 생산될 예정이어서 국내 비만 환자들에게 보다 경제적 비용의 안정적 공급을 통해 약물 접근성과 지속성을 대폭 높일 것으로 기대된다. 한미약품 관계자는 "국내 비만 유병률이 매년 꾸준하게 증가하고 있어 국민들의 건강이 더욱 위협받고 있다"며 "한국 제약회사가 처음부터 끝까지 독자 기술로 개발하는 최초의 GLP-1 비만신약 탄생이 신속하고 성공적으로 이뤄질 수 있도록 최선을 다하겠다"고 말했다.
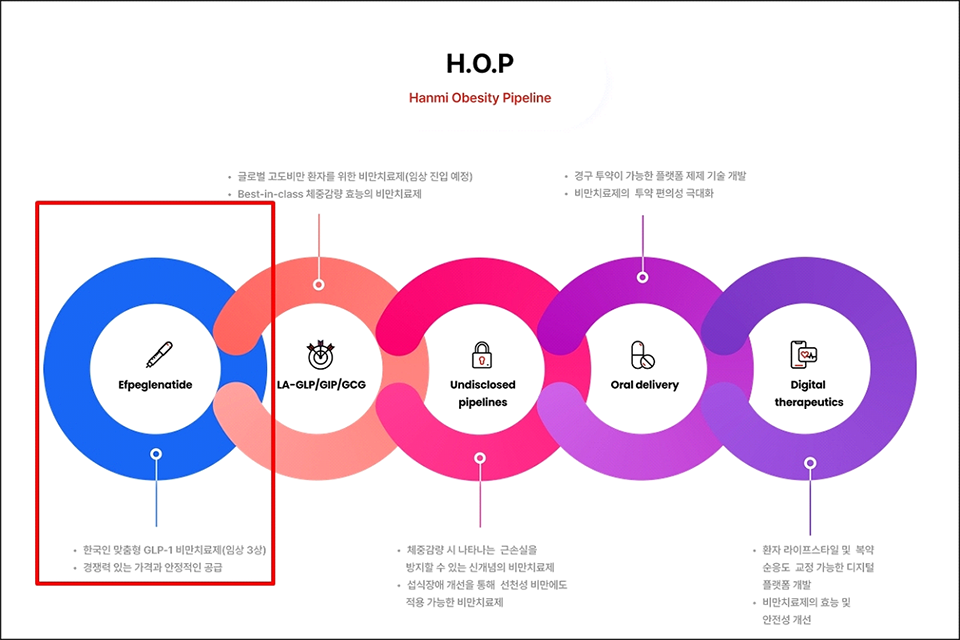
한편 한미약품은 임주현 사장(전략기획실장)의 리더십에 따라 비만 치료에서부터 관리, 예방에 이르는 전주기적 치료 방법을 모색하는 'H.O.P 프로젝트'를 적극적으로 추진하고 있다. H.O.P 프로젝트에는 에페글레나타이드 외에도 수술적 요법에 따른 체중 감량 효과(25% 내외)에 버금가는 강력한 효과를 확인한 'LA-GLP/GIP/GCG(코드명 HM15275)', GLP-1 제제 사용시 나타날 수 있는 근육량 손실을 방지해 체중 감량의 퀄리티를 개선하고 요요 현상 억제에 도움을 줄 수 있는 바이오신약을 비롯해 섭식장애 개선제, 경구용 비만 치료제, 비만 예방과 관리에 적용할 수 있는 디지털 치료제 등이 포함돼 있다.
관련기사
- 송영숙 한미그룹 회장 "새로운 50년, 새로운 한미 시작된다"
- 한미약품그룹, OCI그룹과 통합… 창업 2세 임주현 사장 승계 굳혔다
- 한미약품 "한국인 최적화 GLP-1 비만 치료제, 국내 임상 3상 승인"
- 한미사이언스, 비만 신약 5종 'H.O.P 프로젝트' 집중 육성
- 한미, 당뇨약 개발 '에페글레나타이드' 비만치료제로 변경
- 한미약품, 홈페이지 전면 개편… "제약사 정형화된 틀 벗어나"
- 3회 임성기연구자상 대상에 김빛내리 서울대 석좌교수
- 한미그룹 "OCI그룹과의 통합으로 절감되는 상속세 전혀 없다"
- 한미약품, 아이젠사이언스와 'AI 활용 항암신약 공동 연구개발' 나서
- 비만 진료는 급여를 해줘야 할까? "소아 비만 급여 시급"
- 한미약품, 차세대 비만 치료 삼중작용제, FDA에 임상 1상 승인 신청

