GC녹십자와 국립보건연 공동 국책사업으로 개발 추진
녹십자 "오랜 기간 인체에 사용돼 온 제제, 개발 간소화"
코로나19 환자를 대상으로 한 혈장치료제 임상시험이 식품의약품안전처의 승인 시 곧바로 진행될 전망이다.
중앙방역대책본부(이하 방대본)은 11일 코로나 대응 현황 정례브리핑을 통해 "지난 10일 임상시험용 혈장치료제 제조공정이 완료됐고 분병(만들어진 약물을 병에 담는 과정)을 진행, 임상시험 승인 시 환자 대상으로 곧바로 착수할 예정"이라고 밝혔다.
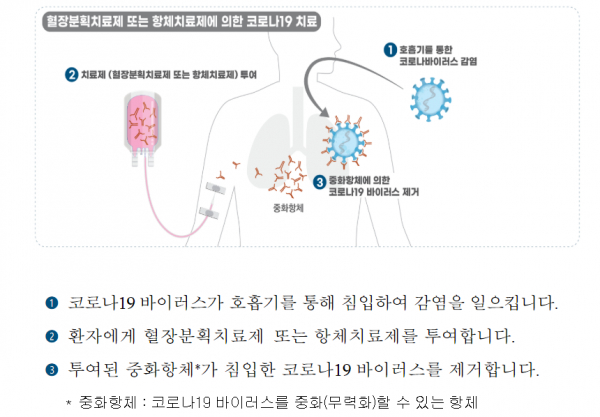
혈장치료제는 코로나19 완치자의 혈액 속 포함된 항체와 면역글로불린을 농축, 제제화한 의약품이다.
혈장치료제 개발은 국책사업으로 GC녹십자와 국립보건연구원이 연내 개발을 목표로 준비 중이다. 항체치료제나 약물 재창출, 신약 개발 대비 개발 목표 시기가 가장 빠르다.
혈장이 수집돼 지난달 18일 제제 생산이 시작된 바 있다. 임상시험계획(IND)은 지난달 29일 식품의약품안전처에 제출됐다.
GC녹십자에 따르면 국내 5개 병원에서 시험 대상자 60명을 대상으로 혈장치료제 'GC5131A'를 투여, 약물의 적정 용량을 설정하고 안전성과 유효성을 탐색할 계획이다.
이와 함께 방대본은 임상 근거에 기반을 둔 방역대책을 마련하기 위해 코로나19 확진자 5500여명의 임상역학정보를 공유하고 있다. 17개 기관에 대한 공개 후 3차 심의를 거쳐 9개 기관에 대해 추가 공개한다.
추가 승인된 9개 기관에서는 ▲중증 코로나19의 호흡기 위험인자와 예후 규명 ▲임상 양상 결정 요인분석 ▲기저질환에 따른 예후 차이 분석 등(붙임 3 참고)에 임상역학 정보를 활용할 예정이다.
이밖에도 코로나19 치료제로 특례 수입된 '렘데시비르'를 35개 병원에서 116명의 환자에 대해 신청해 현재 116명 모두에게 공급을 완료했다.

