식약처, 2022년도 신약 지정목록 의견 조회, 25일까지
혈액 및 체액용약 5품목, 화학요법제 4품목 등 뒤이어
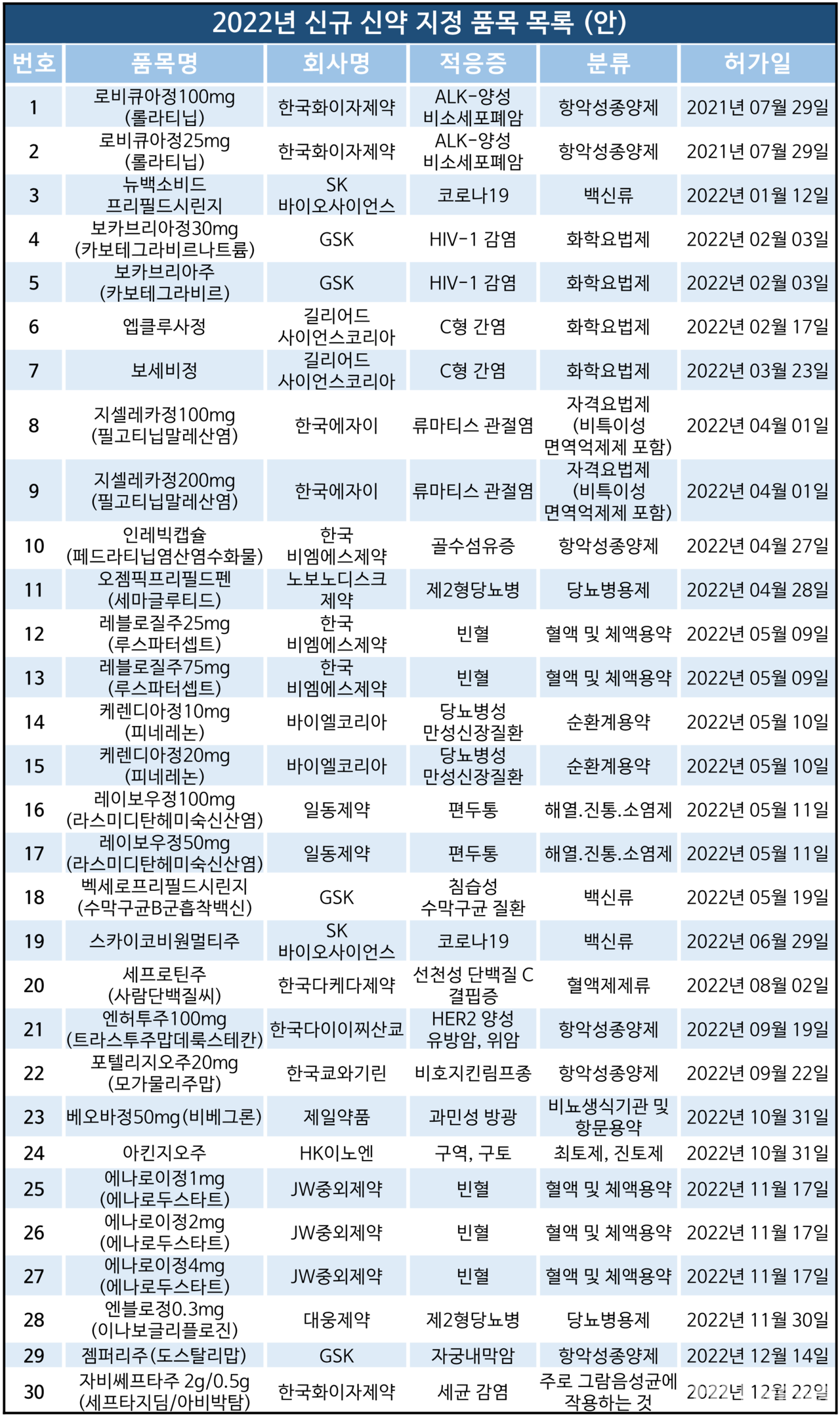
작년 식품의약품안전처가 신약으로 지정한 의약품 30품목 가운데 항암제가 6품목(20%)으로 가장 많았다.
식약처는 매년 '의약품의 품목 허가·신고·심사규정' 제52조, '생물학적제제 등의 품목허가·심사 규정' 제36조, '한약(생약)제제 등의 품목허가·심사규정' 제36조 등 규정에 의거 신약으로 지정된 의약품을 공고한다.
식약처는 6일 제약산업 협회들과 함께 '2022년도 신약 지정 목록 공고(안)'에 대한 업계 의견을 묻는 의견조회를 실시했다. 제출기한은 오는 25일까지다.
이견이 없는 경우 총 30품목의 신규 신약은 지정되고 전체 신약은 720개 품목으로 확대된다.
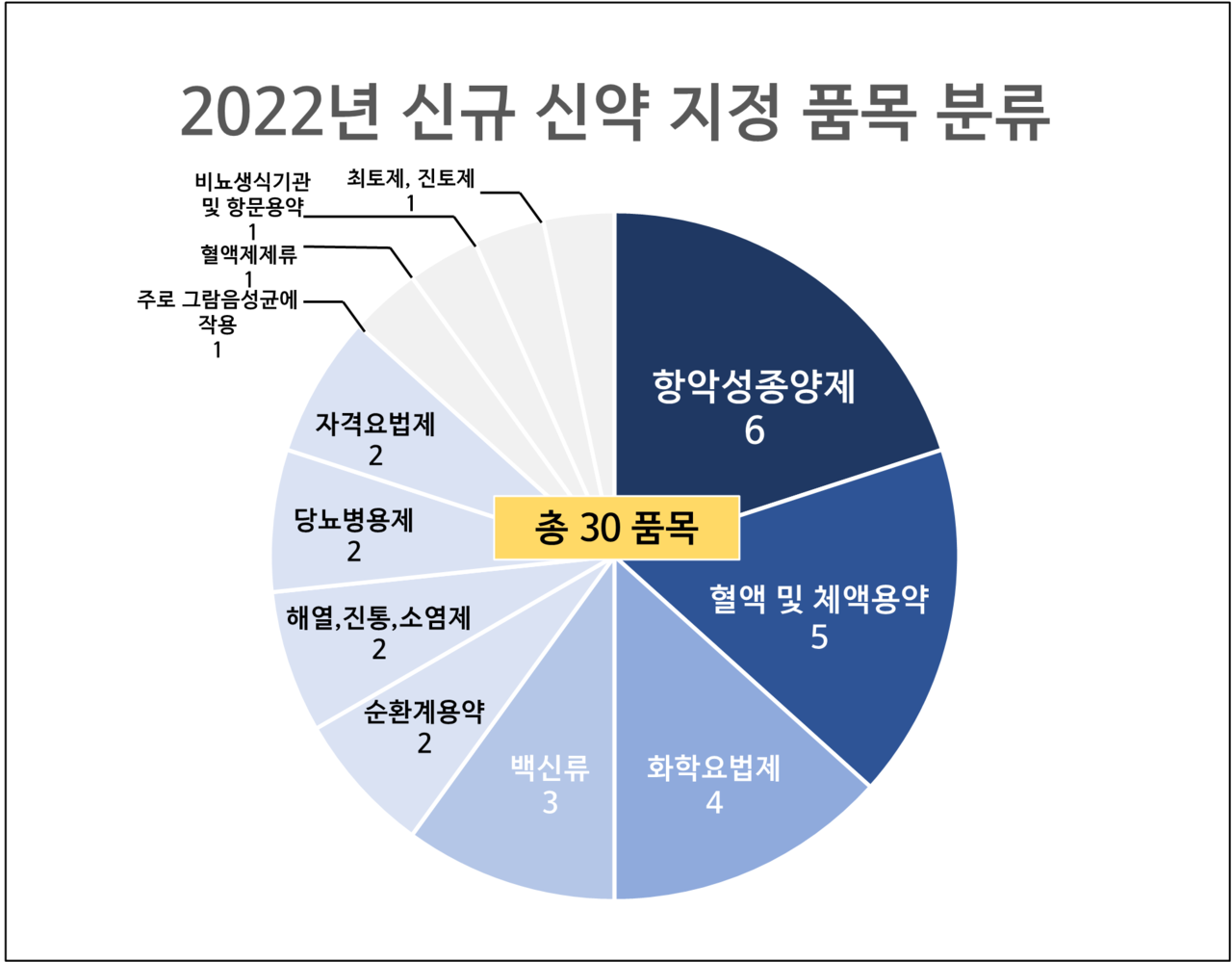
식약처 의약품 분류 체계에 따르면, 신규 신약 지정 30품목은 △항악성종양제(6품목) △혈액 및 체액용약(5품목) △화학요법제(4품목) △백신류(3품목) △순환계용약(2품목) △해열, 진통, 소염제(2품목) △당뇨병용제(2품목) △자격요법제(2품목) △주로 그람음성균에 사용(1품목) △혈액제제류(1품목) △비뇨생식기관 및 항문용약(1품목) △최토제, 진토제(1품목) 등으로 분류된다.
가장 많은 분류를 차지한 항목은 항악성종양제로 전체 품목의 20%를 차지했다. 세부 제품명은 △한국화이자제약 '로비큐아(성분명 : 롤라티닙)' △한국비엠에스제약 '인레빅캡슐(성분명 : 페드라티닙)' △한국다이이찌산쿄 '엔허투(성분명 : 트라스트주맙데룩스데칸)' △한국쿄와기린 '포텔리지오(성분명 : 모가물리주맙)' 등이다.
이 중 로비큐아는 2021년 7월 29일 조건부 허가됐지만, 올해 3상 임상 결과를 추가로 제출하면서 신약으로 지정됐다.
혈액 및 체액용약으로 분류된 품목도 항암제의 뒤를 이었다. 모든 제품은 '빈혈'을 적응증으로 가졌으며, 2개 제품이 총 5개 용량 품목으로 허가됐다. 대상 제품은 한국비엠에스제약의 '레블로질(성분명 : 루스파터셉트)'과 JW중외제약 '에나로이(성분명 : 성분명 : 에나로두스타트)'다.
이 외에도 국산 개발 신약으로 이름을 올린 SK바이오사이언스의 코로나19 변이 백신 '스카이코비원멀티주'와 대웅제약 제2형당뇨병 치료제 '엔블로(성분명 : 이나보글글리플로진)'가 이름을 올렸다.
제35호 국산 신약으로 작년 6월 29일 허가된 스카이코비원은 코로나19 예방을 목적으로 국내·외 정부 및 기관이 협업한 대표적 오픈이노베이션 사례다.
화이자 등 글로벌 빅파마에 비해 늦은 '웨이브2 백신'으로 개발된 이 백신은 작년 9월, 61만 도즈가 정부에 우선 공급된 바 있지만, 지난 11월 잠정 국내 생산을 중지했다.
제36호 국산 신약으로 작년 11월 30일 허가된 엔블로는 SGLT-2 억제제 성분 이나보글리플로진 제제다. 정제형 제2형당뇨병 치료제는 작용 기전에 따라 크게 DPP-4 억제제와 SGLT-2 억제제로 나뉘는 데, 국내에서 SGLT-2 억제제로 개발된 것은 엔블로가 최초다.
현재 대웅제약은 허가-평가 연계제도를 통해 엔블로의 급여결정을 신청한 상황이다.

