레이저티닙·아미반타맙… 1차치료 '타그리소'와 비교 임상
바이오벤처 잇따라 보툴리눔 톡신 수출용 허가…개발 포석
한 눈에 보는 임상 승인·품목 허가 - 9월 4주차 (09.21~25.)

유한양행이 얀센에 기술수출한 폐암 신약 후보물질 '레이저티닙'과 항암항체 '아미반타맙'을 더한 병용요법 임상 3상이 국내에서도 진행된다. 유럽에서는 해당 연구의 참여환자 전원이 치료효과를 보였다는 중간 결과가 나오기도 해, 치료제로 개발될 지 기대를 모으고 있다. 국내 바이오벤처들은 보툴리눔 톡신 개발에 박차를 가한다.
25건 중 신약 허가용 9건… 레이저티닙, 유의미한 결과 계속 입증할까

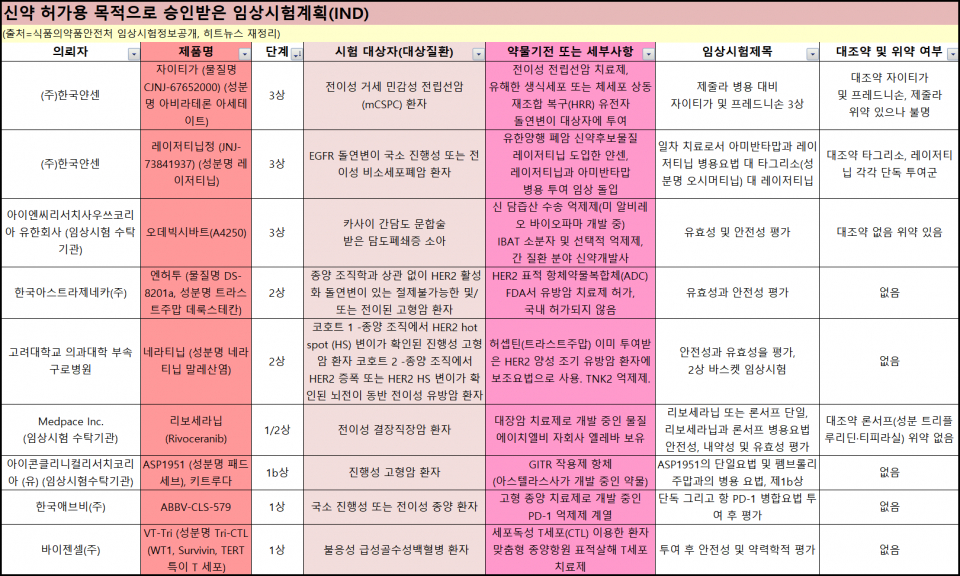
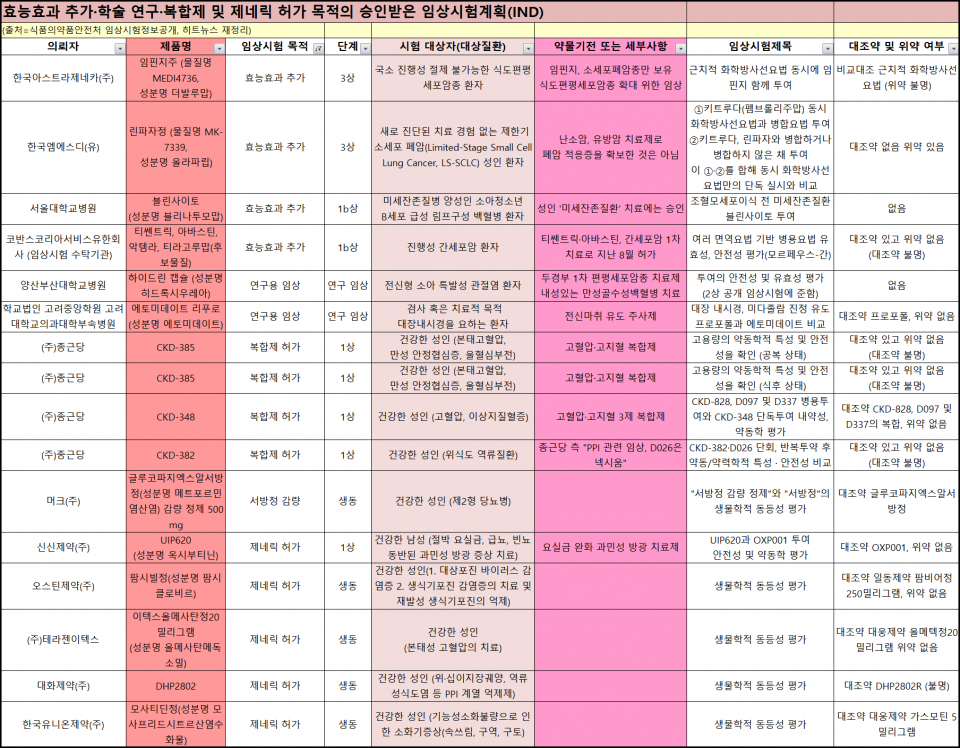
식품의약품안전처로부터 승인받은 임상시험은 총 25건이다. 용도에 따라 ▲신약 허가용 9건 ▲효능·효과 추가 4건 ▲연구용 임상 2건 ▲복합제 허가 4건 ▲서방정 감량 1건 ▲제네릭 허가 5건이다.
한국얀센은 지난 21일 레이저티닙·아미반타맙 병용요법의 유효성과 안전성을 확인할 임상 3상을 승인받았다. 전체 피험자 중 국내 환자는 8명으로 분당서울대학교병원 등 3개 의료기관에서 진행한다.
암세포 성장 수용체인 EGFR 돌연변이가 있는 비소세포폐암 환자에 1차치료제로 병용 투여를 하고, 이를 타그리소(오시머티닙)과 레이저티닙을 각 단독 투여한 환자군과 비교한다.
앞서 얀센은 지난 20일(현지시각) 유럽종양학회(ESMO)에서 '레이저티닙+아미반타맙' 병용 1b상 임상연구 중간결과를 공개했다.
EGFR 결손 또는 변이를 동반한 비소세포폐암 환자 중 선행 치료 경험없는 20명의 환자와 1차 치료제인 타그리소(성분명 오시머티닙) 복용 후 재발한 45명 중 16명의 환자에서 높은 반응률을 보였다.
EGFR 표적항암제 치료를 안 해본 20명의 환자는 약물치료 후 7개월(중앙값) 시점에 평가하니 전원이 종양 축소, 객관적 반응률(ORR) 100%를 보였다. 타그리소 투여 후 재발 환자 16명의 종양 크기도 줄었다.
추후 결과들은 레이저티닙·오시머티닙이 폐암 치료제로서의 가능성 있는지, 타그리소 내성 환자의 2차 치료제가 될지를 가늠케 할 전망이다.
식품의약품안전처 임상시험정보공개 현황 및 히트뉴스 재정리
식품의약품안전처 임상시험정보공개 현황 및 히트뉴스 재정리
국내 바이오벤처 바이젠셀은 급성골수성백혈병 면역세포 치료 후보물질(개발명) 'VT-Tri(1)-A'의 임상 1상을 승인받았다. 환자 9명을 대상으로 안전성과 내약성, 약물이 체내에 작용하는 특성 등을 평가한다.
'VT-TrI(1)-A'는 세포독성 T세포(CTL)를 이용한 환자 맞춤형 종양항원 표적 살해 T세포 치료 후보물질로 바이젠셀의 플랫폼 기술 바이티어(ViTier)에 기반했다. 2022년까지 1상 결과를 확보할 계획이다.
올해 신규 수출용 보툴리눔 톡신 5품목… 허가 줄잇는 이유
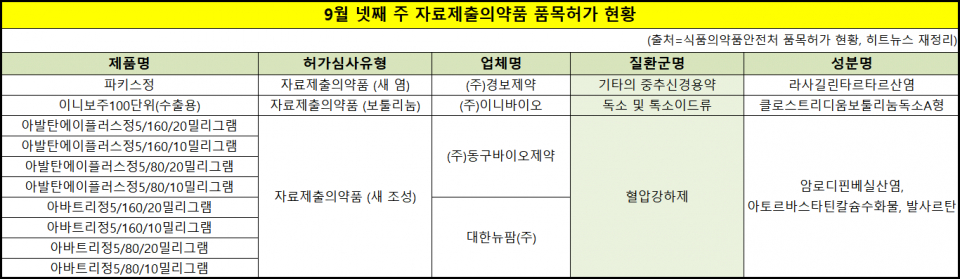
신규 허가 받은 품목은 총 53품목인데 자료제출의약품이 10품목, 제네릭이 43품목이다. 자료제출의약품 10품목은 염을 새롭게 한 1품목, 보툴리눔 톡신 1품목, 새로운 조합의 복합제 6품목으로 나뉜다.
식품의약품안전처 품목허가 현황, 히트뉴스 재정리

이니바이오는 지난 21일 이니보주100단위(클로스트리디움보툴리눔독소A형)(수출용) 품목 허가를 획득했다. 올 들어 수출용 허가는 ▲한국비엠아이 ▲한국비엔씨 ▲제테마 ▲프로톡스 ▲이니바이오까지 5곳이 받았다.
A형은 한국엘러간 '보톡스주'와 휴젤 '보툴렉스주'와 같은 유형이다. 참여 업체가 늘면서 보툴리눔 톡신 시장 경쟁이 치열할 전망이다. 수출용 허가는 국내 허가에 비해 간소해 연구개발의 포석으로 활용, 후발주자의 허가가 이어지고 있다.
경보제약은 파킨슨병 치료 보조요법으로 쓰이는 '아질렉트'의 첫 염변경 후발약을 내놓는다. 라사길린메실산염 성분인 아질렉트를 '라사길린타르타르산염' 성분의 '파키스정'으로 22일 허가받았다.
100억원 가량의 처방실적을 기록하는 아질렉트의 뒤를 이어 30여개 제약사가 제네릭을 출시, 각축을 벌이고 있다. 제네릭 시장 경쟁도 주목된다.

