오리지널 '가스터'와 생동 착수… 차등 약가제도 따른 조치
코19 혈장치료제 2상 진행할 녹십자 "가장 빠른 개발" 약속
키트루다·임핀지·티쎈트릭 등 면역항암제 임상 연구 줄이어
[HIT-DATA #3] [지난 주의 신규 임상승인 · 허가]
히트뉴스가 격주로 소개하던 '임상승인 현황'과 '품목허가 현황'을 통폐합, 각각 현황을 매주 통계로 제시합니다. 유의미한 경향성, 주요 사례의 목적을 짚습니다. 코로나19 치료제 · 백신 개발에 대한 국민적 관심이 큰 만큼 관련 현황에 대해서도 정보를 전하겠습니다.
이번 주 'HIT-DATA [지난 주의 신규 임상승인 · 허가]' 시작합니다.
임상시험 신규 승인=라니티딘의 공백을 파모티딘이 대체하자 위탁 제네릭을 급히 내놓던 제약사들과 달리 대웅제약과 한국콜마는 늦었지만 자체 생동에 나섰다.
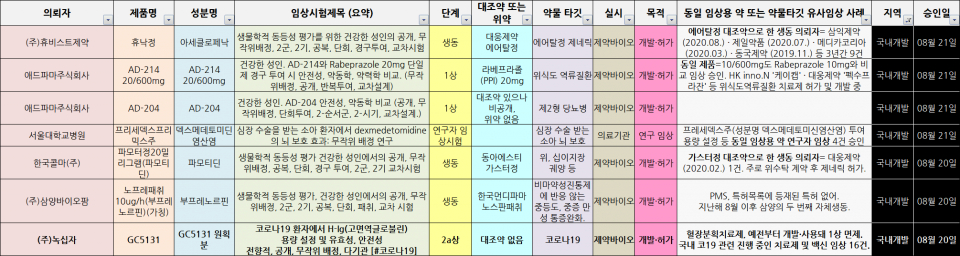
(사진출처=식품의약품안전처 임상시험 승인 현황, 히트뉴스 재정리)
지난 20일 한국콜마는 파모터정20밀리그램, 2월 대웅제약도 오리지널 '동아에스티의 동아가스터정20밀리그램'과 생물학적 동등성 평가 시험을 승인받았다. 이는 파모티딘 제네릭을 자체 생산하겠다는 회사들 의지다.
라니티딘 사태 후 파모티딘 제네릭은 38품목 늘어, 국내 파모티딘 제제는 81품목으로 집계됐다. 대부분 콜마파마와 삼익제약에 생산을 맡긴데 비해 대웅제약과 한국콜마는 자체 생산 전환해 약가인하를 피하고 수익 구조를 개선할 전망이다.
GC녹십자의 코로나19 혈장분획 치료제 'GC5131A'가 임상시험 2상에 돌입한다. 지난 20일 승인받아 가까운 시일 내 6개의 병원에서 코로나19 환자 60명에 투여가 개시될 예정이다.
'GC5131A'는 코로나19 완치자 혈장에서 항체가 들어있는 면역 단백질을 분획해 만든 고면역글로불린이다. 오랜 기간 인체에 사용 돼 온 제제라 임상 1상을 면제했고, 개발 과정도 간소화된다는 게 식품의약품안전처와 GC녹십자의 설명이다.
이로써 현재 국내에서 코로나19 관련, 진행 중인 치료제 및 백신의 임상시험은 총 16건(치료제 14건, 백신 2건)이다.
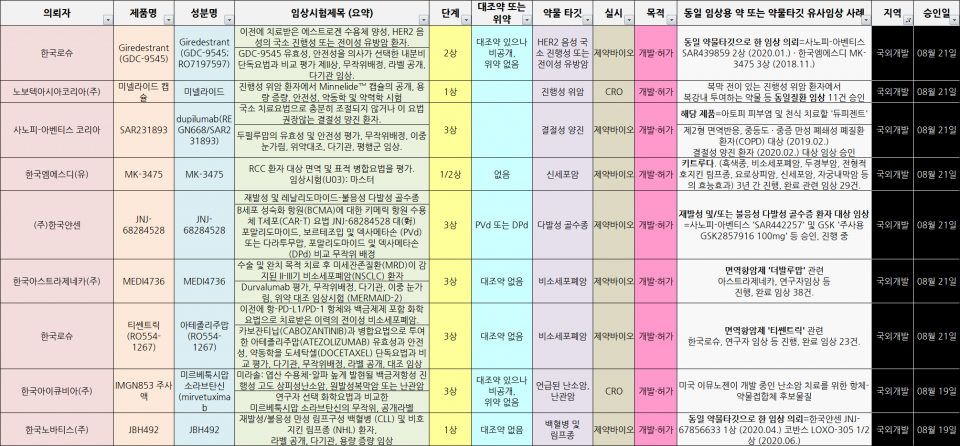
(사진출처=식품의약품안전처 임상시험 승인 현황, 히트뉴스 재정리)
이밖에 국외에서 개발, 국내 허가를 받은 면역항암제 ▲키트루다 ▲임핀지 ▲티쎈트릭에 대한 임상시험들은 ▲국내 품목허가 ▲효능효과(적응증) 추가 ▲임상 데이터 확보를 목적으로 승인됐다.
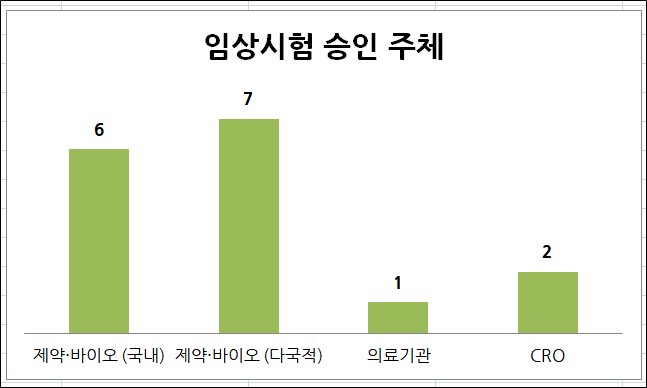
지난 한 주간 신규 승인받은 임상시험은 16건이다. 신청인(중복 포함)별로 ▲다국적 제약·바이오 7건 ▲국내 제약·바이오 6건 ▲CRO(임상시험수탁기관) 2건 ▲의료기관 1건이다.
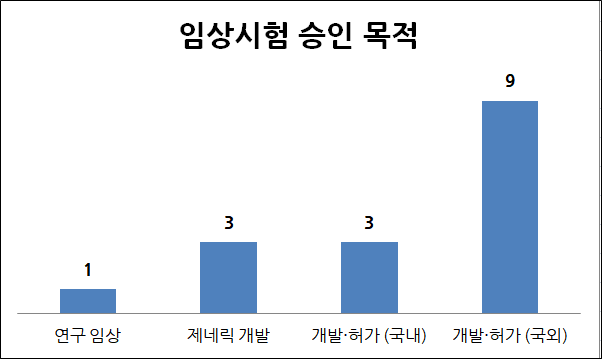
시험단계 상 ▲3상 5건 ▲1상 4건 ▲생동성(생물학적 동등성) 3건 ▲1/2상, 2상, 2a상 각 1건 순이다. 승인 목적에 따르면 ▲국외 약물 개발·허가 9건 ▲국내 약물 개발·허가, 제네릭 개발(생물학적동등성) 각 3건 ▲연구목적 임상 1건 순이다.
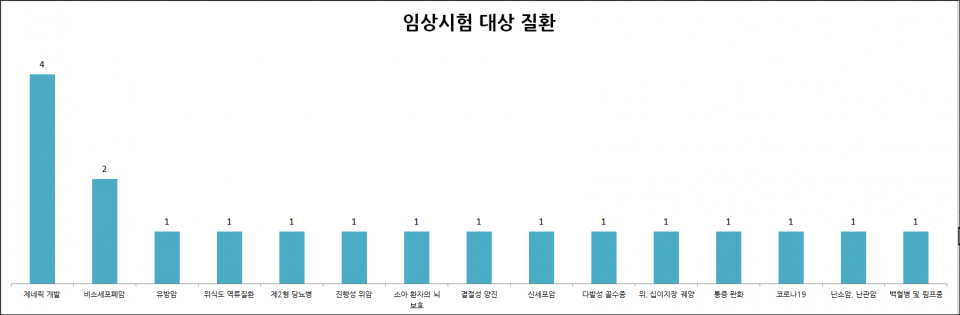
해당 임상시험이 대상으로 한 개발 및 질환은 ▲제네릭 개발 4건 ▲비소세포폐암 2건 ▲유방암 · 위식도역류질환 · 제 2형 당뇨병 · 진행성 위암 · 소아 환자의 뇌 보호 · 결절성 양진 · 신세포암 · 다발성 골수종 · 위, 십이지장 궤양 · 통증 완화 · 코로나19 · 난소암, 난관암 · 백혈병 및 림프종 각 1건이었다.
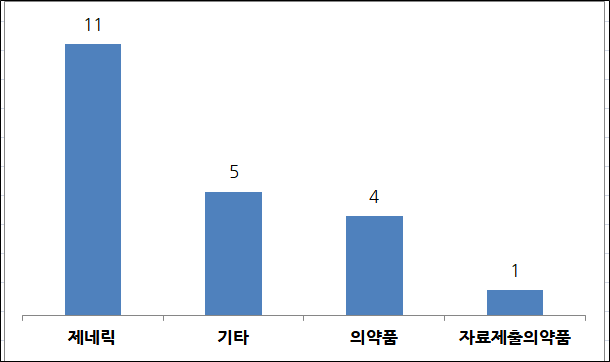
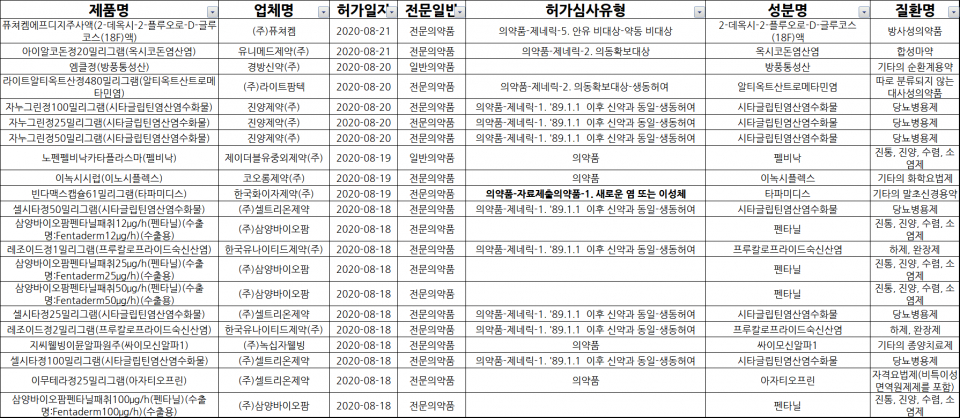
품목 신규 허가= 같은 기간 총 21품목이 허가받았다. 분류별로 ▲전문의약품 19품목 ▲일반의약품 2품목이다. 허가심사 유형에 따르면 ▲제네릭 11품목 ▲기타 5품목 ▲의약품 4품목 ▲자료제출의약품 1품목이다.
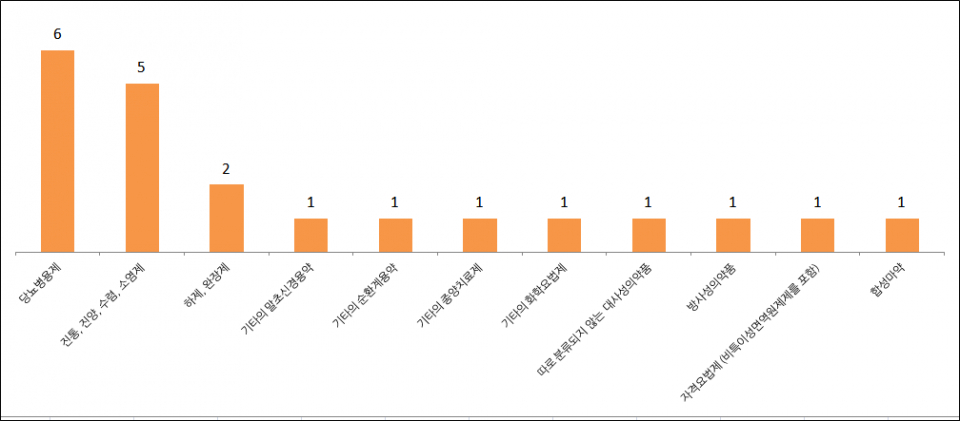
질환군에 따라 ▲당뇨병용제 6품목 ▲진통, 진양, 수렴, 소염제 5품목 ▲하제, 완장제 2품목 ▲기타의 말초신경용약 · 기타의 순환계용약 · 기타의 종양치료제 · 기타의 화학요법제 · 따로 분류되지 않는 대사성의약품 · 방사성의약품 · 자격요법제(비특이성면역원제제를 포함) · 합성마약 등 각 1품목 순이었다.