젤잔즈 굳건한 선두 유지…린버크 글로벌 시장에서 올루미언트 제쳐
린버크, 국내에서 약평위 넘으면서 국내 처방 확대 기대
스마이랍, 주용량인 150mg에선 허가 받지 못해 한계 지적
젤잔즈가 주도하던 JAK 억제제 시장에 린버크와 스마이랍이 가세하면서 시장 경쟁이 한층 치열해 질 전망이다.
히트뉴스(www.hitnews.co.kr)가 시장조사데이터 유비스트를 분석한 결과, JAK 억제제 시장에서 화이자의 젤잔즈(토파시티닙)의 올해 상반기 원외처방액은 64억원으로 전년도 같은기간 56억원보다 14% 성장했다.
일라이 릴리의 올루미언트(바리시티닙닙)는 올해 상반기 23억원을 기록하며, 전년도 같은기간 약 9000만원을 기록한 것 대비 큰 폭으로 성장했다.
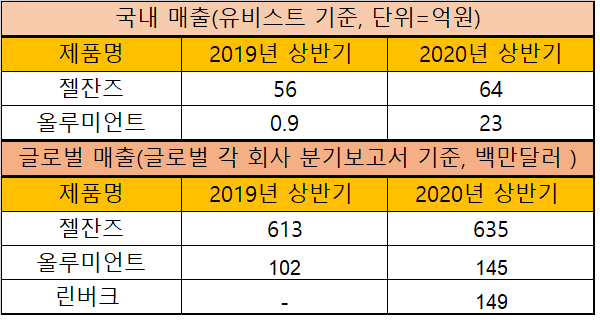
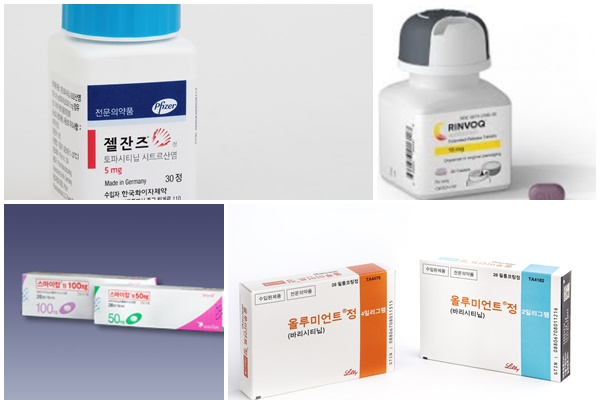
이처럼 젤잔즈와 올루미언트가 큰 폭으로 매출 성장을 하고 있는 가운데, 국내에는 이들과 같은 계열 약물인 애브비의 린버크(유파다시티닙), 아스텔라스제약의 스마이랍(페피시티닙)이 속속 허가를 받아 급여를 앞두고 있어 향후 JAK 억제제 시장은 한층 치열해 질 것으로 보인다.
특히 한국애브비의 경구용 JAK 억제제 '린버크(유파다시티닙)'는 급여등재에 성큼 다가서면서, 빠른 시장 확대를 꾀할 수 있을 것으로 보인다.
건강보험심사평가원은 지난 6일 진행된 제8차 약평위에서 심의한 결정신청 약제의 요양급여 적정성 심의결과를 공개했다. 심의결과, 중등증에서 중증의 활동성 류마티스관절염 치료제 린버크는 급여 적정성이 있는 것으로 나타나 공단과 약가 협상을 앞두고 있다.
린버크보다 앞서 지난 1월 식품의약품안전처로부터 허가를 받은 스마이랍은 가중평균가를 수용하는 협상면제 트랙을 밟아 올해 10월 중으로 급여 등재가 예상됐지만 아직까지 린버크보다 급여 속도는 더딘 편이다.
또 스마이랍의 메인 용량인 150mg은 임상시험에서 효능 차이에 대한 의문으로 식약처로부터 승인을 받지 못 해 임상 현장에서 한계로 지적될 것으로 보인다. 현재 국내 식약처로부터 승인 받은 용량은 50mg, 100mg이다.
글로벌 시장 역시 젤잔즈가 굳건한 선두를 지키고 있지만, 린버크가 올루미언트의 매출을 따라잡으며 치열한 2위 경쟁이 일어날 것으로 보인다.
각 회사가 발표한 올해 2분기 보고서에서 매출을 살펴보면, 젤잔즈 6억3500만달러 (약 7523억원), 린버크 1억4900만달러(약 1765억원), 올루미언트 1억4500만달(약 1718억원)으로 집계됐다. 올루미언트보다 늦게 출시된 린버크가 올해 2분기 매출에서는 앞서는 양상을 보였다.
JAK억제제 중 가장 먼저 허가를 받은 '젤잔즈'는 류마티스관절염뿐만 아니라 궤양성대장염과 건선성 관절염 치료에도 적응증을 받으면서 폭넓게 처방되고 있다.
젤잔즈의 아성에 도전하기 위해 후속 치료제들 역시 다양한 적응증 확대를 위한 임상을 진행하고 있다.
린버크는 건선관절염, 크론병, 아토피피부염, 궤양성대장염, 거대세포동맥염에 대한 3상 임상연구가 진행되고 있으며, 강직척추염에 대한 연구도 진행 중이다. 올루미언트는 성인 아토피피부염 환자를 대상으로 지난해 3상을 완료했다.
한편, 길리어드의 필고티닙은 JAK 억제제 공동 경쟁품목인 휴미라와 비교 임상을 진행했으며, 메토트렉세이트(MTX) 치료 경험이 없는 류마티스 관절염 환자에서 단일 처방, 병용 처방의 효과를 확인했다. 동시에 궤양성 대장염에서 유의미한 임상 3상 결과를 발표했다. 이를 바탕으로 미국, 일본, 유럽에서 품목 허가를 위한 심사 중이다.

