췌장암 동물모델에서 100% 완전관해 확인
임상중개이행연구로 전임상부터 임상 조건 수립
GC녹십자셀은 지난달 15일 기업설명회(IR)를 통해 췌장암 동물모델에서 100% 완전관해를 보인 메소텔린(Mesothelin) 표적 CAR-T 세포치료제(MSLN-CAR-T) 연구결과를 공개했다. 전임상 단계지만, 아직 어떤 글로벌 제약사도 고형암 대상 CAR-T 치료제 개발을 못 한 상황이라 혁신신약(first in class)개발의 작은 불씨를 지폈다는 점에서 이 연구는 의미가 깊다.
GC녹십자셀 CAR-T 치료제는 메소텔린을 표적으로 삼는다. 메소텔린은 인체의 강(cavity)과 내부 기관을 둘러싸는 중피(mesothelium)에 매우 적은 양이 분포돼 있다. 그러나 암 세포에는 많이 분포돼 있는데, 특히 췌장암(80~85%), 중피종(85~90%), 난소암(60~65%)과 비소세포폐암(60~65%)에서 발견돼 CAR-T 치료제의 새로운 표적으로 주목받는다.
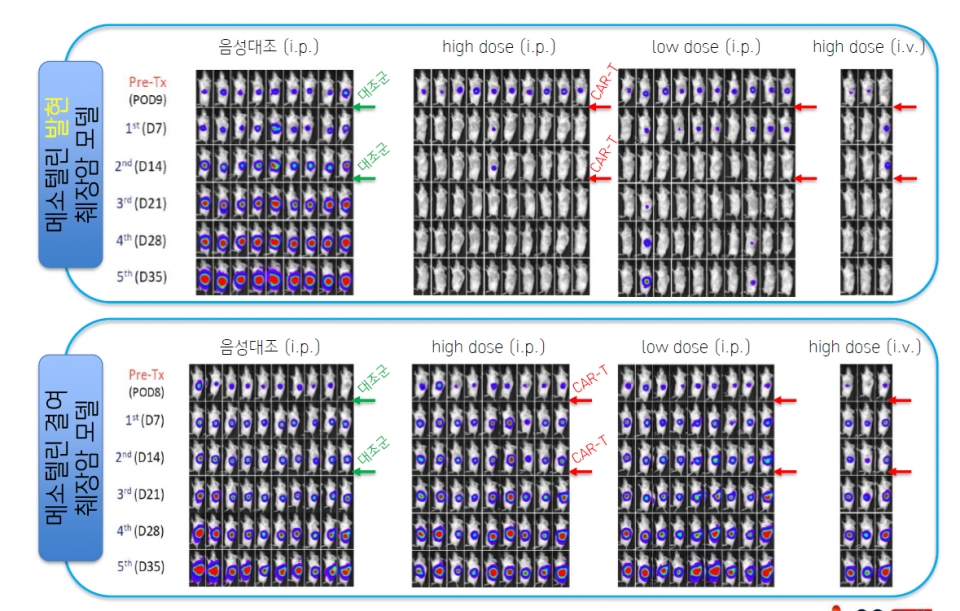
GC녹십자셀은 동소이식 췌장암 마우스모델(Orthotopic Pancreatic Cancer Model)에서 복강주사(IP)와 정맥주사(IV)로 MSLN-CAR-T를 투여했다. 그 결과 메소텔린을 과발현하는 동소이식 췌장암 마우스모델에서 MSLN-CAR-T세포 1차 투여 후 80~90%의 항암효과를 보였고, 2주 후 2차 투여 시 100%의 완전관해(CR)를 나타냈다.
반면 음성대조군에는 MSLN에 대한 ScFv(항체)를 포함하지 않는 CAR-T세포를 동일한 일정으로 2회차 투여했으며, 암세포는 계속 성장했다. 또한 메소텔린을 발현하지 않는 동소이식 췌장암 마우스모델에도 MSLN-CAR-T세포를 투여했으며, 음성대조군과 마찬가지로 췌장암이 지속 성장하는 모습을 보였다.
특히 GC녹십자셀의 이번 연구가 이처럼 유의미한 동물실험 데이터를 얻을 수 있었던 데는 플랫바이오의 동소이식모델 덕이 컸다. 동소이식 동물 모델은 임상 상황과 가장 유사한 조건을 갖춘 동물 모델을 이용해 전임상 시험을 진행하는 것이다. 이를 통해 암세포에 대한 약제의 반응이 사람을 대상으로 하는 임상시험에서 재현되는 확률을 높일 수 있어, 임상 성공 확률도 개선할 수 있다.
히트뉴스는 김선진 플랫바이오 회장의 자문을 바탕으로 ▲메소텔린(Mesothelin) 표적 CAR-T세포치료제(MSLN-CAR-T) 연구결과의 의미 ▲신약개발 전임상 연구에서 임상중개이행 연구의 중요성을 일문일답 형식으로 정리했다. 이어 김 회장의 기고문을 통해 신약개발에 있어 임상이행중개연구가 얼마나 중요한지도 다루게 된다.
MSLN-CAR-T 현재 연구 결과를 어떻게 바라봐야 하나.
전임상 데이터에서 어떤 의미를 얻을 수 있는지 궁금하다.
"7부 능선을 넘었다고 본다. 물론 사람을 대상으로 하는 임상시험에서 어떤 용법과 용량에서 최적의 약물 효과를 나타낼지 알아보는 어려운 단계가 남아 있긴 하다.
하지만 MSLN-CAR-T 세포가 우리가 원하는 종양 부위로 이동(trafficking)해, 표적 장기에서 임상적 효능(clinical efficacy)을 이미 동소이식모델을 통해 확인했기 때문에 다른 경쟁 물질 대비 확실한 우위를 점했다고 본다.
뿐만 아니라 이번 전임상 실험(1차 실험)을 통해 독성(toxicity), 표적 환자 그룹(target patients group), 환자 선택 바이오마커(patients selection biomarker (target expression threshold)) 등과 관련된 데이터도 확보했다. 이러한 데이터를 토대로 개발 속도를 현저히 높일 수 있으며, 2021년 임상에 진입하기 위해 임상프로토콜 최적화 과정을 거칠 수 있을 것으로 보인다."
기존 CAR-T 치료제는 혈액암에서만 유의미한 치료 효과를 내고 있다.
고형암에서 CAR-T 치료제가 유의미한 데이터를 내지 못 하는 이유는 뭔가.
"우선 전신으로 투여된 CAR-T 세포를 기반으로 하는 신약 후보물질이 종양부위까지 도달(trafficking)하지 못하는 것이 가장 큰 난관이다. 또 종양미세환경에서 여러가지 상호작용에 의해서 CAR-T 세포 신약 후보물질이 충분한 면역학적인 효능(efficacy) 을 나타내지 못하기 때문인 것으로 알려져 있다. 이번에 GC녹십자셀과 개발한 MSLN-CAR-T는 이러한 어려움을 극복한 것이다."
이번 전임상에서 임상중개이행연구 개념을 도입해 임상 성공 확률을 높일 수 있다고 들었다. 어떻게 임상 성공 확률을 높인다는 말인가.
"전임상 연구는 단순히 물질의 독성과 효능 등을 테스트 하는 것이 아니다. 전임상 단계부터 임상중개연구의 개념을 도입해, 실제 임상 디자인, 임상시험 진입과 성공을 위해 필요한 모든 정보를 파악하는 과정이다.
다시 말해 임상 성공 확률을 높이기 위해 전임상 동물시험 단계부터 ▲적응증 ▲바이오마커의 확보 ▲환자군의 조건(병기 등) ▲다른 치료법에 대한 반응 및 치료시기 (1차, 2차) ▲용법(단독, 병용, 동시, 순차적 등) 가능한 한 모든 정보를 확보한다. 이러한 정보를 바탕으로 임상 프로토콜 강화(protocol enrichment)를 목표로 하는 게 임상중개이행연구의 진정한 의미다."
보통 동물을 대상으로 하는 전임상 데이터 결과가 사람을 대상으로 하는 임상에서 재현되지 못 하는 걸로 알고 있다. 어떻게 전임상 단계 연구를 토대로 임상 성공 확률을 높이는 건가.
"예를 들어 설명하면 이렇다. 현재 전임상 효능 실험에서 가장 많이 이용하는 피하종양모델은 실제 임상 실행가능성(clinical feasibility)이 결여돼 있다. 왜냐하면 실제 암 환자의 경우 수술, 방사선 요법 등의 국소치료로는 종양을 제거할 수 없는 상태가 대부분이다. 즉, 실제 환자는 전이병변을 갖고 있는 경우가 대부분 인데, 전임상 동물모델은 이러한 조건이 반영돼 있지 않다.
따라서 중개이행연구를 하지 않은 전임상 데이터 결과를 적용하면, 전신 적용(Systemic administration)을 통한 약제 분포와 장기에 도달한 약제가 암세포에 작용해 효능을 발휘하는 기전이 달라질 수 있다. 이러한 문제를 해결하기 위해 동소이식모델을 활용한다. 동물모델에 임상 환자 상황과 가장 유사하게 갖춰 전임상 단계의 암세포에 대한 약제 반응이 임상에서도 유사하게 나타낼 수 있도록 해준다."
이번에 GC녹십자셀과 함께한 실험을 예로 설명해 준다면.
"만약 동소이식모델을 활용하지 않으면, 어떤 결과가 나타나는지 설명하겠다. 우선 일반 피하종양모델을 활용해 동물실험을 진행하면, 췌장암 주 전이기관(췌장, 간, 복강 내)이 아닌 전혀 다른 미세 환경 조건에서 실험을 진행할 수 밖에 없다. 즉, 일반 피하 조직 환경에서 암 세포 미세환경 상호작용(cancer cell-host microenvironment interaction)만 보게 되는 것이다.
또, 피하종양모델에서 보기 때문에 전신 적용(systemic administration)된 약제가 종양에 도달하는 기전과 분포상태 또한 임상적 유의성이 없다. 만일 약제가 종양에 직접 주사 되었다면 임상 실행 가능성(clinical feasibility)은 더욱 떨어질 수 밖에 없다.
이번 녹십자셀의 동소이식 모델을 이용한 MSLN-CAR-T 면역치료제의 효능시험에서 보여준 완전관해의 의미는 지금까지 다른 약제들과 비교해볼 때 매우 놀라운 결과다."

