식약처, 21일까지 사전 GMP 평가 개선 방안 의견조회
특수제제는 적용 대상 제외

식품의약품안전처가 완제의약품에 대한 사전 GMP를 평가할 때 기존 '대단위제형별' 실시 기준을 '약전제형별'로 전환하는 것을 염두에 두고 절차를 밟고 있다.
제약사 불법 제조 행위가 지속 적발됨에 따라 식약처 의약품품질과는 지난 2월 △사전 GMP 평가 개선 △시판전 GMP 평가 △적합판정 취소 근거 마련 등을 골자로 하는 'GMP 안전관리 체계 개선 세부계획'을 공개했었다.
이같은 맥락에서 식약처는 최근 '사전 GMP 평가 개선 방안 의견조회'라는 제목의 공문을 국내 제약사를 대상으로 송부하며, 21일까지 의견을 받는다. 사전 GMP 평가 개선으로 기존 대단위제형별 평가를 약전제형별 평가로 전환하는 '의약품 제조 및 품질관리에 관한 규정'을 개정하려는 것이다.
현재 국내 의약품 대단위제형은 △내용고형제 △주사제 △점안제 △내용액제 △외용액제 △연고제 △그 밖의 제형 등으로 분류되고 있다.
다만, 이번 개정안이 통과된다면 앞으로 '의약품 GMP 적합판정 및 적합판정서 발급 관련 업무처리방안(공무원 지침서)'에 수록된 약전제형별로 사전 GMP평가가 시행된다.
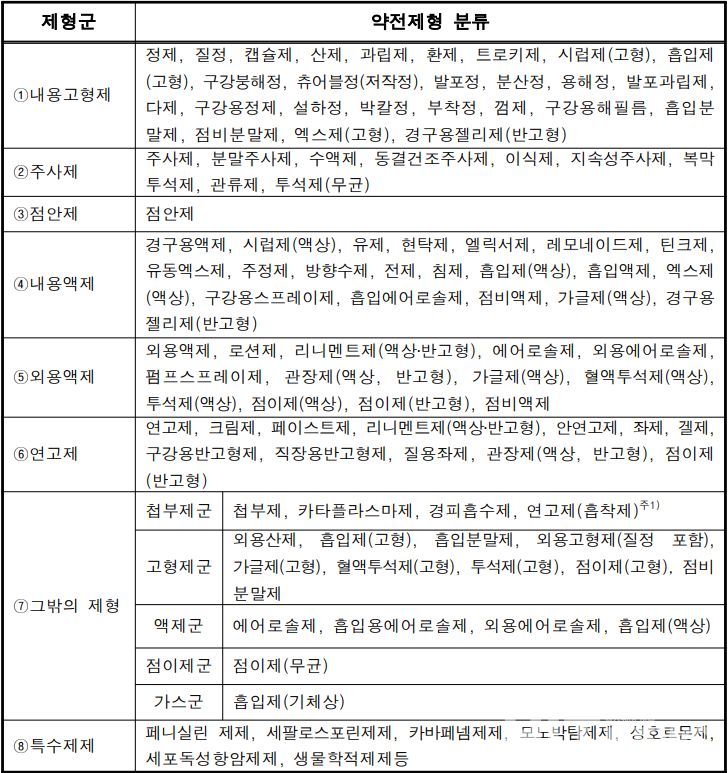
이 지침서는 약전제형분류를 내용고형제(정제 등 26개), 주사제(수액제 등 9개), 점안제, 내용액제(경구용액제 등 20개), 외용액제(로션제 등 13개), 연고제(크림제 등 12개), 그 밖의 제형(첩부제군 4개, 고형제군 9개, 액제군 4개, 점이제군 1개, 가스군 1개), 특수제제(페니실린 제제 등 7개) 등 106개 항목으로 제시하고 있다.
의약품품질과는 "기존 보유 제형이 내용고형제 중 정제인 경우, 캡슐제를 추가 제형으로 제조 판매허가 받기 위해선 적합판정이 필요 없었지만, 약전제형별로 분류하게 되면 적합판정을 받아야 한다"고 예시를 들었다. 이어 "의약품 제조업자가 이미 발급받은 GMP 적합판정서에 기재된 약전제형은 인정되고, 기재된 약전제형에 대해 추가적인 별도 사전 평가는 불필요하다"고 덧붙였다.
한편, 이번 개선안은 '특수제제'에 적용되지 않는다. 이 제제는 기존과 동일하게 제형군내 제제분류별 평가가 실시된다.

