Kim's Weekly 1월 4주차 의약품 품목허가·임상승인 현황
┖한 줄 요약 : 제2형 당뇨병

한국MSD의 제2형 당뇨병치료 복합제 자누메트정(시타글립틴, 메트포르민) 제네릭이 지난주에만 20개 쏟아졌다. 시타글립틴/메트포르민 복합제는 2022년에만 49개가 품목허가를 획득했다.
지난주 식품의약품안저처는 의약품 36품목(전문약: 34개, 일반약: 2개), 임상시험 30건(1상: 22개, 2상: 3개, 3상: 3개, 연구자: 2개)을 각각 승인했다.
품목허가 2/3은 제2형 당뇨병 치료제
지난주 식약처 품목허가를 획득한 36품목 중 제2형 당뇨병 치료제는 23개(63.8%)에 달했다.
광동제약, 메디카코리아, 보령바이오파마, 셀트리온제약, 일양약품, 위더스제약, 한림제약은 '광동메포시타정', '시글립틴엠정', '셀타메트정', '자누아린듀오정', '에스립틴엠정', '한림시타엠정' 품목허가를 각각 획득했다. 위더스 제약(시타글립틴/메트포르민, 50/850, 50/500mg)을 제외하면 6개 업체는 50/1000, 50/850, 50/500mg 세개 용량군 품목을 확보하게 됐다.
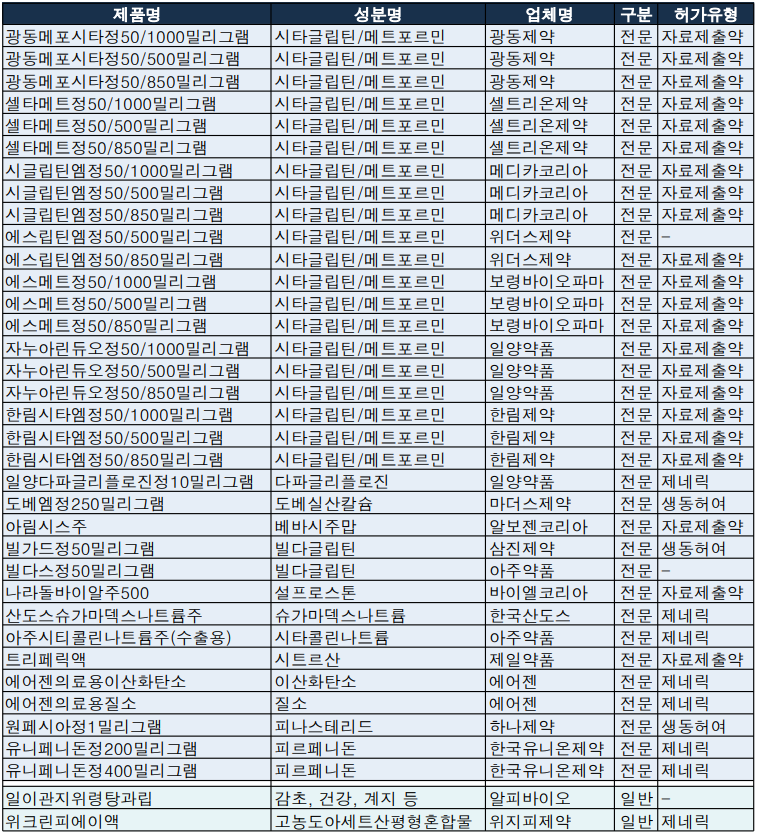
일양약품은 한국아스트라제네카 제2형 당뇨병치료제 '포시가정(다파글리플로진)' 단일제 품목허가를 획득했으며, 삼진제약, 아주약품은 한국노바티스 제2형 당뇨병치료제 '가브스(빌다글립틴)' 제네릭인 '빌가드정 50밀리그램'과 '빌다스정 50밀리그램' 허가를 각각 획득했다.
이밖에 알보젠코리아는 △전이성 직결장암 △전이성 유방암 △비소세포폐암 △진행성 또는 전이성 신세포암 치료제인 한국로슈의 '아바스틴(베바시주맙)' 바이오시밀러 품목허가를 획득하기도 했다. 베바시주맙의 바이오시밀러로는 세번째로 삼성바이오에피스(온베브지주), 한국화이자제약(자이라베브주)의 뒤를 이었다.
하나제약은 피나스테리드 성분 성인남성(만18~41세) 탈모 치료제 '원페시아정1밀리그램' 품목허가를 승인받았다.
새로운 당뇨병 3제 복합제 3상 진입
제일약품의 제2형 당뇨병 3제 복합제(피오글리타존염산염/메트포르민/다파글리플로진)가 임상시험 3상 승인을 획득했다. 서울대학교가 실시하는 이번 임상시험 3상은 국내 제2형 당뇨병 환자 256명을 대상으로 진행될 예정이다.
경동제약은 국내 본태성고혈압 환자 286명을 대상으로 'KDF1901' 물질 임상시허 3상을 승인받았다.
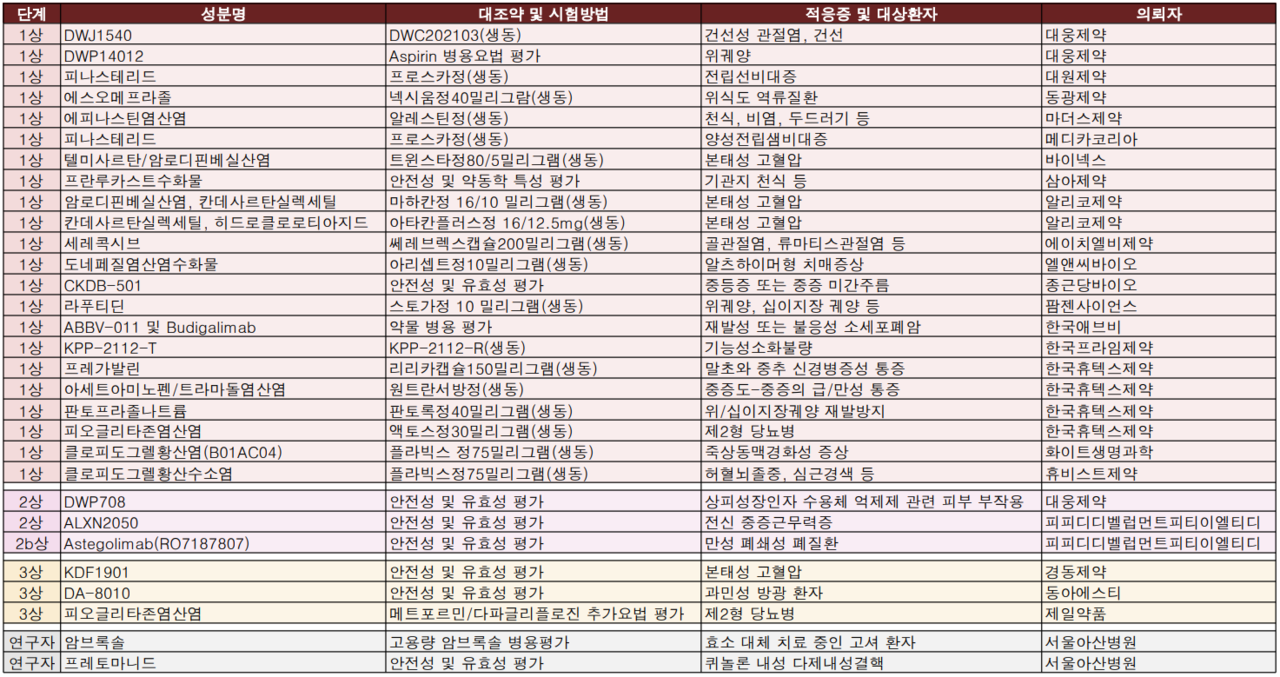
이밖에 화이트생명과학과 휴비스트제약은 한독의 허혈뇌졸중, 급성관상동맥증후군 치료제 '플라빅스정'의 생물학적동등성 시험을 승인받았다. 대상 적응증은 각각 죽상동맥경화성 증상과 허혈뇌졸중이다.

