Kim's Weekly 8월 1주차 의약품 품목허가 임상승인 현황

8월 1주차(8월 2일~6일) 식품의약품안전처는 26품목의 의약품(전문약 15품목, 일반약 11품목) 품목허가와 26건의 임상시험(1상 15건, 2상 4건, 3상 3건, 연구자 임상 3건)을 승인했다.
품목허가 및 임상시험에는 항응고제 '자렐토' 제2형당뇨병치료제 '자디앙' 제네릭과 위궤양·십이지장궤양 치료제 생동성 시험 등 제네릭 품목들이 다수 확인됐으며 3상에는 3건의 임상시험 승인이 이뤄졌다.
이어지는 자렐토 자디앙 제네릭
이번주 품목허가 동향을 살펴보면, 지난주에 이어 항응고제 자렐토(리바록사반)와 제2형 당뇨병치료제 자디앙(엠파글리플로진) 제네릭이 생동허여로 식품의약품안전처 품목허가에 이름을 올렸다.
제뉴원사이언스는 '제뉴원리바록사반정 20/15/10mg' 3개 제형을, 에이치케이이노엔은 '이노엔엠파글리플로진정25/10mg' 2개 제형에 대한 품목허가를 각각 획득했다.
미쓰비시다나베파마코리아가 시신경척수염범주질환 치료제 '업리즈나주(아네빌리주맙)'에 대한 품목허가를 획득했다. 업리즈나주는 희귀의약품으로 분류된 자료제출약으로 약 투입 전 코르티코스테로이드 정맥투여, 항히스타민제 경구투여 증 전처리가 요구된다.
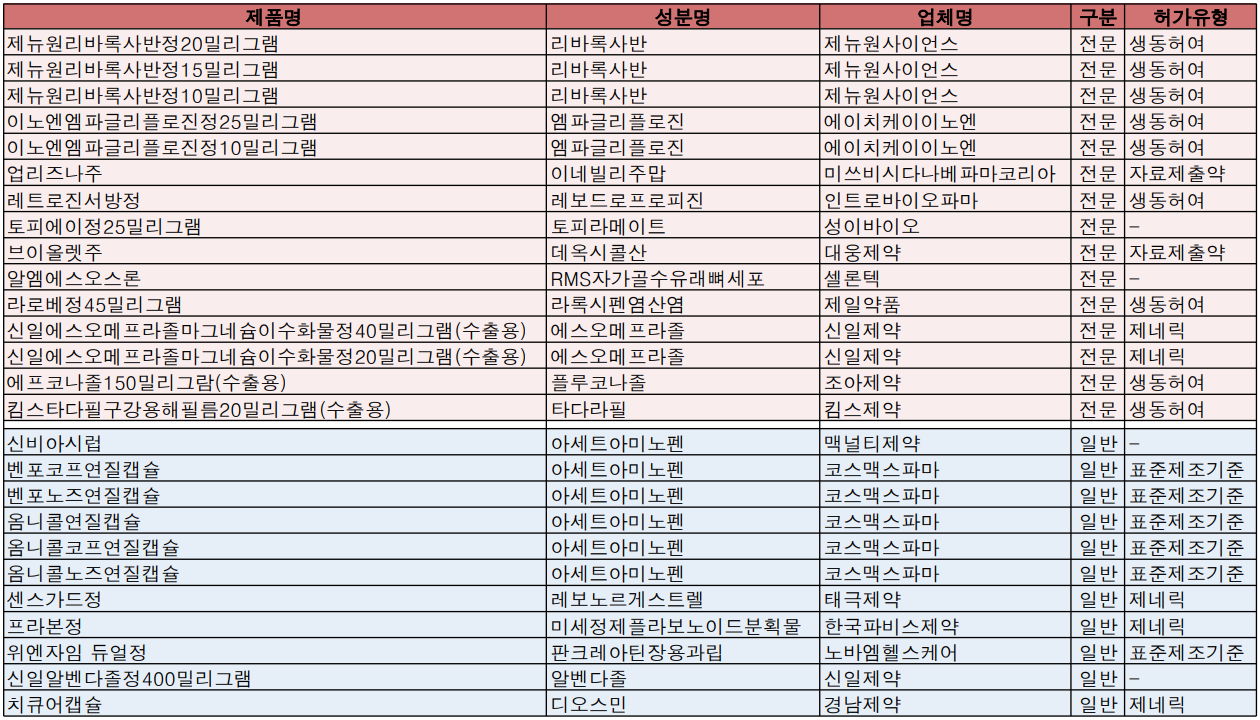
셀론텍은 RMS자가골수유래뼈세포를 제제로 국소 골형성을 촉진하는 자가세포치료제 '알엠에스오스론'을 허가받았다.
일반약에서는 아세트아미노펜 제제 일반약 6개 품목이 품목허가를 획득했다.
맥널티제약은 시럽제 '신비아시럽', 코스맥스파마는 △벤포코프연질캡슐 △벤포노즈연질캡슐 △옴니콜연질캡슐 △옴니콜코프연질캡슐 △옴니콜노즈연질캡슐 품목허가를 승인받았다.
노보노디스크 혈우병 치료제, 릴리 유방암 항암제 3상 진입
노보노디스크의 A형 혈우병치료제와, 릴리의 유방암 항암제, 한국아이큐비아가 대행하는 신생혈관성 황반변성체료제 3건이 임상시험 3상을 승인받았다.
노보노디스크는 성분명 'NNC0365-3769'에 대한 글로벌 임상시험 3상을 진행한다. 전체 대상환자 70명 중 우리나라 환자는 6명이며 임상시험 예정 기간은 2021년 10월부터 2023년 11월이다.
FVIII 억제인자가 있거나 없는 A형 혈우병이 있는 소아 환자에서 피하 투여된 NNC0365-3769 예방요법의 노출 및 안전성, 유효성을 평가한다.
한국릴리는 에스트로겐수용체 양성, HER2 음성 국소 진행성 또는 전이성 유방암 환자들을 대상으로 LYL3484356과 시험자가 선택한 내분비 요법을 비교하는 다기관 3상 시험에 돌입할 예정이다. 시험기관은 아산병원, 연대 세브란스병원, 서울대길병원 등이다.
한국아이큐비아는 'Opthea'의 신생혈관성 연령 관련 황반변성(nAMD) 환자를 대상으로 애플리버셉트 단독요법과 애플리버셉트-'OPT-302' 병용요법의 유효성 및 안전성을 평가하는 다기관 임상시험 3상을 승인받았다.
아주대병원, 강남세브란스병원, 경희대병원, 분당차병원 등이 임상시험기관으로 참여한다.
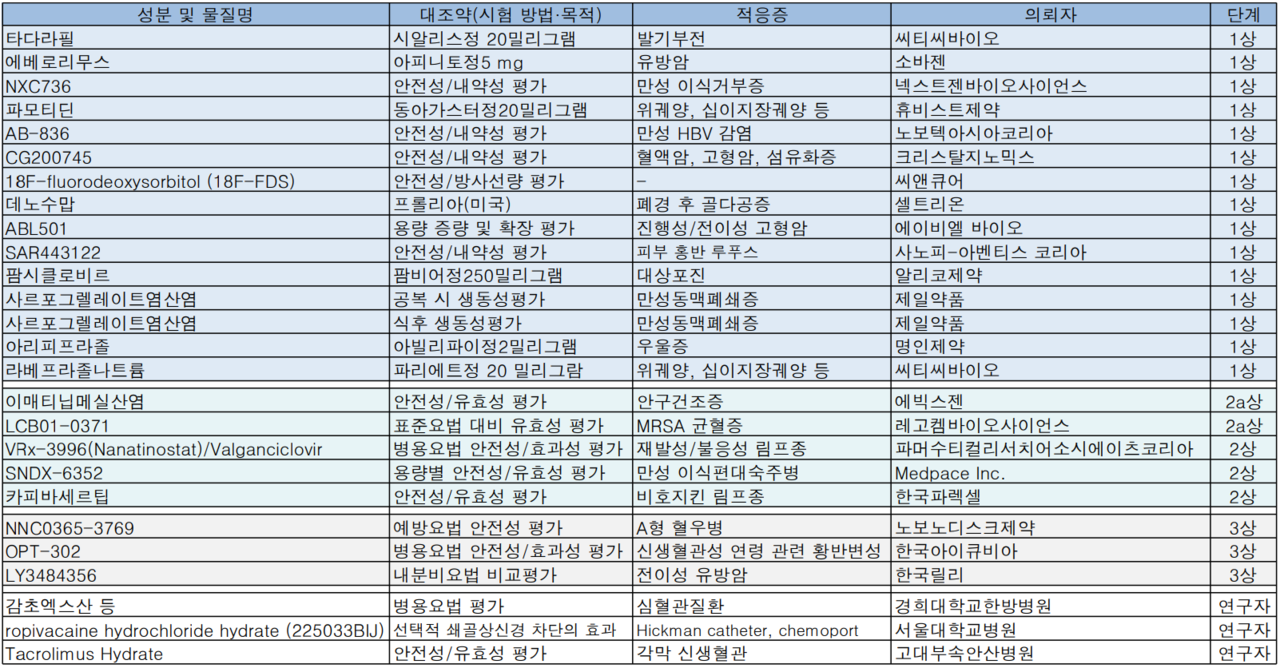
이밖에도 셀트리온은 폐경 후 여성 골다공증 치료제인 암젠의 '프롤리아(미국 허가품목)'와 'CT-P41'의 약동학, 약력학 및 안전성을 비교평가하는 임상시험 1상을, 휴비스트제약과 씨티씨바이오는 위궤양, 십이지장궤양 치료제 '동아가스터정 20밀리그램', '파리에트정 20밀리그람'과의 생물학적 동등성을 평가하는 임상시험 1상을 각각 승인받았다.

