항체치료제 'CT-P59' 2·3상 승인…환자 1000명 투여
신약 허가용 등 임상 28건 · 헌팅턴병 신약 등 21품목
한 눈에 보는 임상 승인·품목 허가 - 9월 3주차 (09.14~18.)
셀트리온이 코로나19 항체 치료제 개발에 속도를 내고 있다. 경증·중등증 환자 대상의 유효성과 안전성 평가를 위한 2·3상 임상시험을 승인받아 본격 돌입했다. 얀센은 항우울제 신약 후보물질 '셀토렉산트'의 임상 3상을 승인받아 상업화 계획을 구체화하고 있다.
28건 중 신약 허가 10건… 셀트리온 치료제 개발, 향방은 지켜봐야

항체치료제 'CT-P59'의 시제품
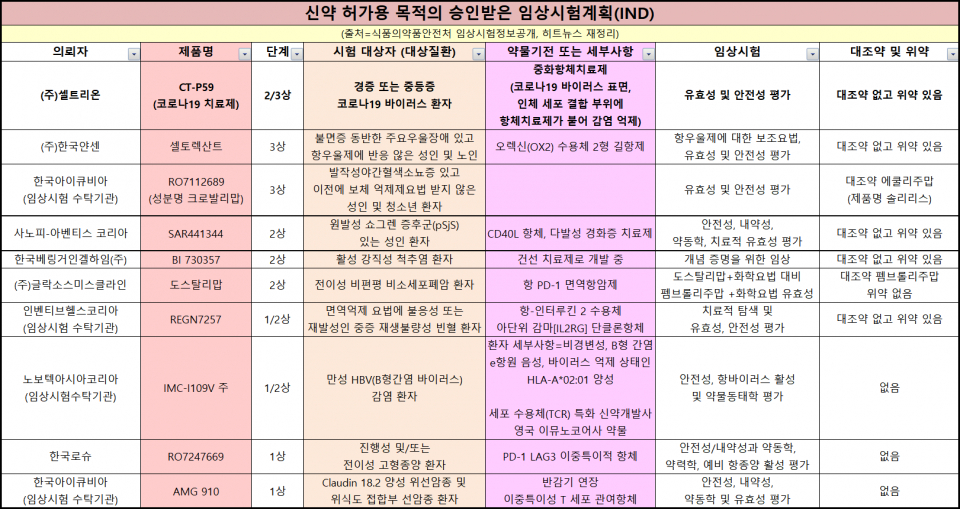
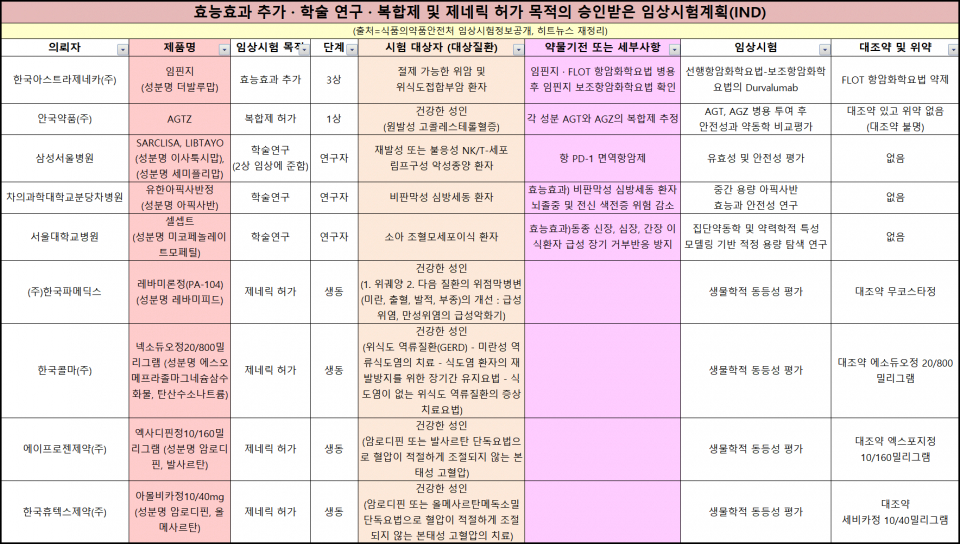
식품의약품안전처로부터 승인받은 임상시험은 총 18건이다. 임상시험 용도에 따라 ▲신약 허가용 (코로나19 신약 허가용 1건 포함) 10건 ▲효능·효과 추가 1건 ▲복합제 1건 ▲학술 연구용 3건 ▲제네릭 허가 4건이다.
셀트리온은 코로나19 항체 치료 후보물질 'CT-P59'의 2·3상을 승인받았다. 경등·중등증 환자에 2·3상을 동시에 진행하는데 2상에서 300명 대상, 3상 720명 대상이다.
10여개 의료기관과 협력해 유효성과 안전성을 평가하며 연말까지 국내 임상시험은 끝낼 계획이다. 건강한 사람 대상으로 한 국내 임상 1상 결과 안전성과 내약성을 입증해 다음 단계로 진행할 수 있게 됐다.
CT-P59는 코로나 바이러스 표면에 있는 인체 세포와 결합하는 부위에 항체치료제가 대신 붙어 감염을 막는다. 셀트리온이 신약으로 개발 중이며 미국, 루마니아 등 6개국에도 동시에 임상시험계획을 신청했다.
아울러 셀트리온은 향후 글로벌 임상 2상 결과와 코로나19 상황에 따라 식약처와의 사전 협의 하에 기준에 충족되면 조건부허가를 신청할 계획이다. 이에 대해 윤태호 중앙재난안전대책본부 방역총괄반장은 조건부허가 등 셀트리온의 치료제 개발에 대해 조심스러운 입장을 내놨다.
윤 반장은 "임상 2상 결과가 어떨지 가정하기 어렵다. 3상에서 안전성과 유효성에 대해 주된 점검을 해야하기 때문에 총괄적인 검토와 전문 위원회를 통해 조건부허가 여부는 논의되지 않을까 생각한다"고 했다.
식품의약품안전처 임상시험정보공개 현황 및 히트뉴스 재정리
식품의약품안전처 임상시험정보공개 현황 및 히트뉴스 재정리
한국얀센은 후보물질 '셀토렉산트'에 대해 임상 3상을 승인받았다. 구체적으로 불면증 동반한 주요 우울장애가 있고 항우울제에도 반응하지 않은 성인 및 노인 환자에 대해 항우울제의 보조요법으로 유효성과 안전성을 평가한다.
셀토렉산트는 오렉신(OX2) 수용체 2형 길항제의 약물이다. 오렉신2에 저해작용을 보여 과한 각성상태를 완화하는 기전이다. 국내 3상의 목적은 시판허가 획득을 위한 계획으로 풀이된다.
신약 3품목 · 자료제출 약 5품목 · 제네릭 1품목 · 일반약 13품목
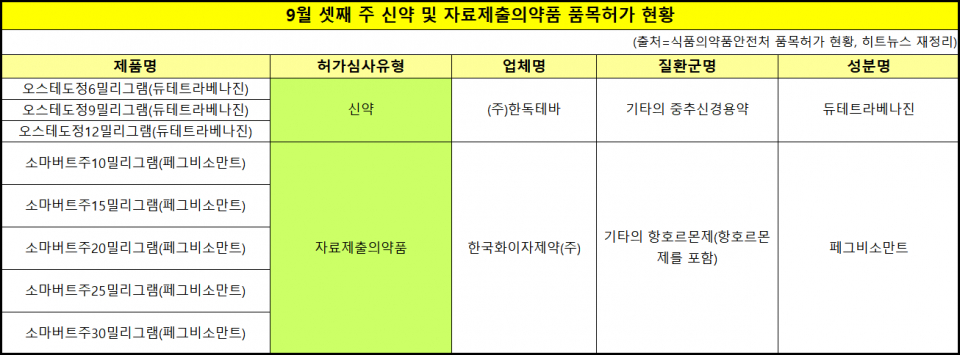
신규 허가 받은 품목은 총 22품목이다. 한독테바와 한국화이자는 국내 희귀질환 치료제를 각각 허가받았다. 환자 치료기회 확대를 기대할 수 있게 됐다.
한독테바가 신약으로 허가받은 듀테트라베나진 성분의 헌팅턴 무도병 치료제 '오스테도정'은 환각과 심한 정서 변화 증상을 개선해준다. 지난 2017년 미 식품의약국(FDA)에 시판 승인을 받았다. 투렛증후군 치료제로도 허가받기 위해 국내 임상 3상을 진행 중이다.
식품의약품안전처 품목허가 현황, 히트뉴스 재정리
한국화이자는 자료제출의약품으로 말단비대증 치료 목적의 '소마버트주'를 허가받았다. 유전자재조합 사람 성장호르몬 유사체로 성장호르몬 결합을 차단하고 시호전달을 방해하는 기전을 갖는다.

