생각을 HIT
공급이냐 안전이냐, 약업계 추는 어디로 기우나
수탁사(CMO)인 국내 모 제약사가 탐스로신 성분의 전립선비대증 치료제 출하 지연을 고객인 위탁사들에게 전한 것으로 나타났다. 갑작스럽게 나온 출하지연 알림에 대해 위탁사들은 (자신들도) 당황스럽다고 유통업체들에게 하소연 했다. 다음 내용은 한 위탁사가 거래처인 유통업체들에 보낸 제품 공급 지연 공문 내용이다.
'제조사로부터 납기 지연 일정을 통보받았다. 갑작스러운 제조사의 납기 지연 통보에 회사도 매우 당황스러운 상황이다. 최대한 제조 일정을 앞당길 수 있도록 노력하겠다.'
공문은 말그대로 '공'적인 '문'서로서 '감정'을 담지 않는다는 점을 생각해보면 감정적인 표현 한마디에 담당자 고충이 묻어난다.
탐스로신의 경우 올해 3월 N-니트로-탐스로신이라는 불순물이 검출되면서 보건당국이 완제의약품을 제조·수입하고 있는 업체를 대상으로 자료 제출 등 안전조치를 지시한 바 있다.
당시 식약처가 매년 사용기한 임박한 3개 단위 이상 제조번호를 기준으로 시험검사 결과를 제출하라고 했던 시점은 6월 12일이다.
업계가 이번 사태를 당황스럽게 보고 있는 것은 업계의 불순물을 바라보는 태도에 기인하는 듯 보인다. 바로 공급과 안전성이라는 가치에서 어느 부분에 초점을 두고 있느냐다.
모든 사람들이 기억하듯 2018년 고혈압치료제인 발사르탄에서 시작된 불순물 사태는 위장약 라니티딘을 거쳐 조사만 수십 품목에 다다를 만큼 흔한 사례가 됐다.
특히 이 과정에서 코로나19로 인해 의약품 수급이 더욱 어려워지면서 공급 불안은 더욱 심해졌다. 그리고 이 과정에서 업계는 의약품 불순물로 인한 불안감이 문제인지 혹은 의약품의 공급 문제로 인한 불안감이 문제인지를 고민하기 시작했다.
실제 업계 내에서도 단순히 기준치의 불안감보다 당장 환자가 약을 복용하지 못했을 때의 불편함이 더욱 클 것이라는 이야기가 나온 것은 이 즈음부터다.
이런 가운데 최근 등장한 아테놀롤 문제는 업계에는 일정 수준의 안도감을 불렀다. 식약처는 독성자료가 불충분해 허용기준을 설정하기 어려운 불순물의 경우 유럽 EMA 사례를 참고, 한시적 허용기준 적용 방안을 도입했고 그 기준을 적용해 불순물 178ng이 넘지 않는 아테놀롤은 향후 저감화 계획을 제출할 경우 제품 출하를 허용키로 한 상황이다.
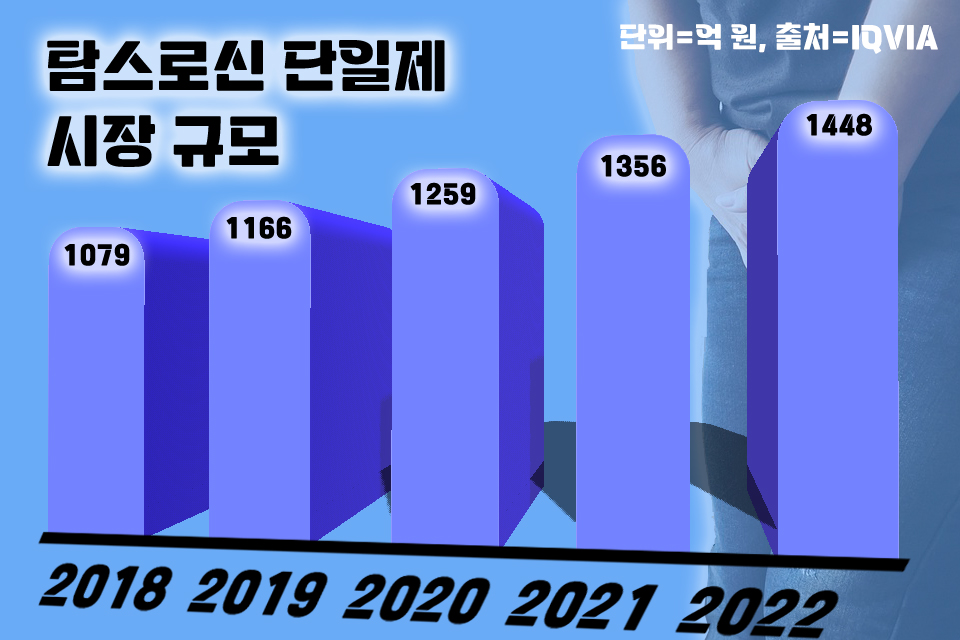
탐스로신 역시 국내 제약사가 무려 3분의 2의 점유율을 갖추고 있는 상황에서 큰 위탁사 중 하나인 다산제약이 제품을 생산할 수 없어 타사가 주력 제품인 0.4mg와 0.2mg 제품을 맡아 생산해왔다.
이런 상황에서 해당 제약사가 제품을 내놓지 못할 경우 수입에 의존하는 오리지널 제품만으로는 전체 수급을 맡기에는 어려운 상황이다.
즉 공문의 배경에는 제약사가 생각하는 '안전과 공급의 균형'에서 해당 회사가 공급을 생각하는 곳이었다는 이야기가 남겨 있는 셈이다. 세계적 분위기 속에서 국내 제약사 역시 일단은 '약을 내놓아야' 한다는 의식을 담고 있다는 뜻이기도 하다.
업계의 태도를 지적할 수 없다. 기준도 제대로 확립되지 않은 불순물의 위험도를 어떻게 알 것이며 그로 인한 공급 피해와 매출 더 나아가 환자의 복용 문제는 어떻게 해결할 것인지에 대한 답은 누구도 쉬이 전할 수 없는 이유에서다.
다만 최근 몇몇 회사들로부터 전해진 이 당황스러운 상황이 의약품을 만드는 이들의 도피처로 쓰일 우려가 있으며, 당국과 업계는 이를 진지하게 고민해야 할 것이다.

