대웅제약 "DWN12088, FDA 패스트 트랙 품목 지정"
브릿지바이오 "BBT-877, 독성 이슈 해결...3분기 글로벌 2상 진행"
한미약품 "LAPSTriple Agonist, FDA·EMA서 희귀의약품 지정"
특발성 폐섬유증(Idiopathic Pulmonary Fibrosis) 치료제의 글로벌 시장 규모가 커지고 있는 가운데 국내 제약바이오 기업들이 특발성 폐섬유증 치료제 개발에 나서고 있다.
글로벌 시장조사기관 리서치앤마켓(Research And Markets)에 따르면, 특발성 폐섬유증 치료제 시장은 매년 7%의 높은 성장률을 보여 2030년 61억 달러(약 8조원)에 달할 것으로 전망되고 있다.
폐가 딱딱하게 굳어지는 질환인 섬유화증은 명확한 발생 원인이 밝혀지지 않았고, 아직까지 근본적인 치료제가 없다. 그렇기 때문에 환자들의 미충족 의료 수요가 높은 대표적인 질환 중 하나다.
국내서 대웅제약, 브릿지바이오테라퓨틱스, 한미약품 등이 특발성 폐섬유증 치료제를 개발하고 있다.
대웅제약(대표 전승호·이창재)은 혁신신약(Fisrt-in-class)으로 자체 개발 중인 특발성 폐섬유증 신약 후보물질 'DWN12088'이 미국 식품의약국(FDA) 신속심사제도(FDA 패스트 트랙) 개발 품목으로 지정됐다고 지난 19일 밝혔다.
DWN12088은 세계 최초 PRS(Prolyl-tRNA Synthetase) 저해 항섬유화제 신약이다. 콜라겐 생성에 영향을 주는 PRS 단백질의 작용을 감소시켜 섬유증의 원인이 되는 콜라겐의 과도한 생성을 억제하는 기전을 가지고 있다. DWN12088은 지난 6월 FDA로부터 특발성 폐섬유증 2상 IND(임상시험계획) 승인을 받았다.

DWN12088의 경우 탁월한 항섬유화 및 폐 기능 개선 효과를 보인 비임상연구와 건강인 대상 임상 1상 결과를 통해 패스트 트랙으로 지정됐다. 대웅제약 관계자는 "FDA와 긴밀히 협의하고 개발 속도를 높여 하루 빨리 혁신신약을 상용화할 수 있도록 최선을 다하겠다"고 강조했다.
브릿지바이오테라퓨틱스(대표 이정규)는 FDA에 특발성 폐섬유증 치료제 후보물질 'BBT-877'의 임상 2상 진입 승인을 위해 제출한 자료와 관련해 잠재 독성 우려를 모두 해소하고, FDA서 임상 2상 개시를 최종 승인 받았다고 21일 공시했다.
브릿지바이오는 한국과 미국을 포함 8개 국가에서 BBT-877의 임상 2상을 개시할 계획이다. 이에 대해 회사 관계자는 "폐섬유화 질환 관련 경험이 풍부한 임상시험수탁기관(CRO)과 계약 절차를 모두 마쳤다"며 "이후 임상시험 개시에 필요한 몇 가지 구체적인 준비 과정들을 조속히 마무리해 이르면 8월 첫 임상시험 기관 활성화 및 환자 모집 단계에 곧바로 진입하게 된다"고 설명했다.
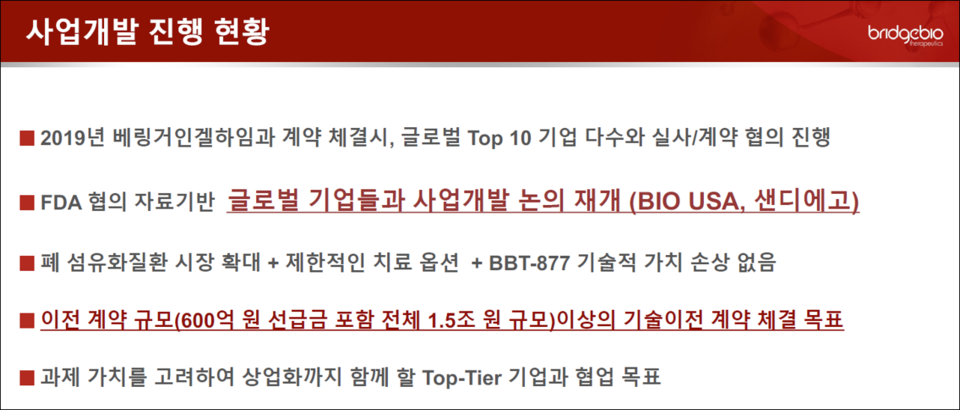
이정규 대표는 "BBT-877의 잠재 독성 이슈와 관련해 미국 FDA로부터 명쾌한 소명 결과와 더불어 당사에서 계획했던 개발 전략 상의 변경이나 지체를 야기하는 요소 없이 임상 2상 진입 개시 승인을 통지받게 돼 뜻깊게 생각한다"며 "폐섬유화 질환 영역에서 혁신신약 개발 성과를 선보일 수 있도록 노력할 것"이라고 전했다.
한미약품(대표이사 권세창·우종수)은 지난 6월 유럽의약품청(EMA)이 한미약품의 삼중작용 바이오 신약 'LAPSTriple Agonist(랩스트리플아고니스트, HM15211)'를 특발성 폐섬유증(IPF) 치료를 위한 희귀의약품으로 추가 지정했다고 밝혔다.
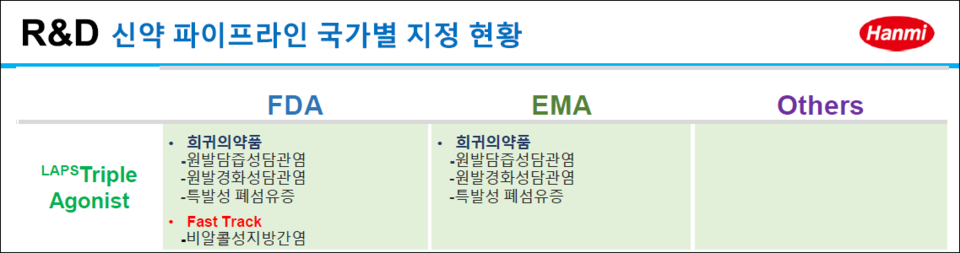
EMA가 지정한 적응증인 특발성 폐 섬유증은 원인을 알 수 없는 폐 염증 과정 및 섬유세포 과증식으로 나타난 조직 섬유화로 인해 폐기능이 급격히 떨어지면서 사망할 수 있는 희귀질환이다. 매년 10만명 당 100명 이하 꼴로 발생하지만 허가된 치료제들은 효능이 부족해 치료가 매우 어려운 상황이다.
LAPSTriple Agonist는 GLP-1 수용체, 글루카곤 수용체 및 GIP 수용체를 동시에 활성화하는 삼중작용제로 △섬유화를 억제하는 '글루카곤' △인슐린분비 및 식욕억제를 돕는 'GLP-1' △인슐린분비 및 항염증 작용의 'GIP'를 동시에 타깃한다.
한미약품 관계자는 "특발성 폐섬유증 동물모델에서 LAPSTriple Agonist의 항염증·항섬유화 효과를 확인한 바 있다"고 말했다.

