한국노바티스, 4세대 만성골수성백혈병 치료제 '셈블릭스' 허가
한국엠에스디, 신세포암종 새로운 치료옵션 될 벨주티판 3상 승인

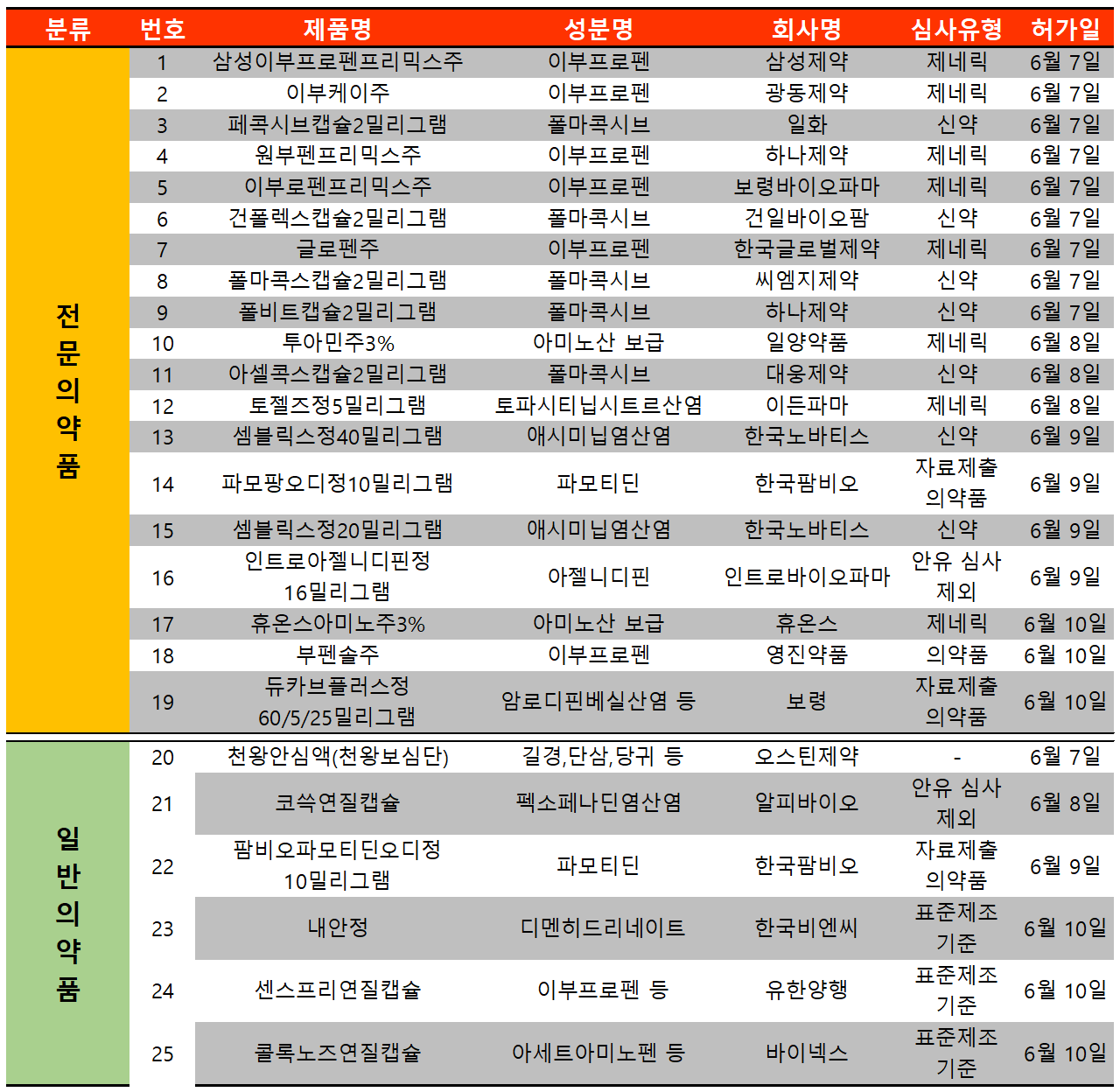
지난 주(6월 6일~6월 12일)에는 총 25개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 19건, 일반의약품은 6건이었다.
이부프로펜 성분 제네릭의약품이 6개 품목으로 가장 많이 허가받았으며 골관절염 치료제 성분인 폴마콕시브 제품 또한 5개 품목이 허가받았다.
폴마콕시브 성분 제품은 국내 22호 신약인 크리스탈지노믹스의 골관절염 치료제 '아셀렉스' 제네릭의약품으로 6월 첫 주에 이미 4품목이 신약으로 허가됐으며 △일화 페콕시브캡슐2밀리그램 △건일바이오팜 건폴렉스캡슐2밀리그램 △씨엠지제약 폴마콕스캡슐2밀리그램 △하나제약 폴비트캡슐2밀리그램 △대웅제약 아셀콜스캡슐2밀리그램 등이 추가로 허가됐다.
'아셀렉스'는 2015년에 허가받아 골관절염(퇴행관절염)의 증상이나 징후의 완화에 사용되고 있으며 염증과 통증을 유발하는 효소를 선택적으로 억제해 기존 품목과 비교해 위장 관계 부작용을 줄였다는 평가를 받았다.
아이큐비아 통계에 따르면 아셀렉스의 매출은 지난 2017년 기준 48억 원, 2018년 45억 원, 2019년 53억 원, 2020년 55억 원, 2021년 53억 원으로 꾸준한 매출을 보였기 때문에 향후 진입하는 제네릭의약품에 따라 매출 변화가 전망된다.
그외 신약 허가로 한국노바티스 '셈블릭스'가 있다. 만성골수성백혈병의 치료제 중 4세대 치료제로 국내에 진입한 셈블릭스는 2가지 이상의 티로신 키나아제 억제제(TKI)로 치료를 받은 만성기의 필라델피아 염색체 양성 만성골수성백혈병(Ph+ CML) 성인 환자의 치료제로 허가받았다.
만성골수성백혈병은 골수구계 세포가 백혈구를 만드는 과정에서 생긴 악성 혈액질환이다. 환자의 90% 이상에서 특징적인 유전자의 이상(필라델피아 염색체의 출현)으로 혈액세포가 과다하게 증식해 백혈구와 혈소판 등이 증가하며, 만성적인 경과를 보이는 혈액암이다.
만성골수성백혈병은 천천히 진행되지만 치료하지 않고 내버려 두면 점차 진행돼 급성백혈병으로 진행이 된다.
TKI 계열 4세대 표적항암제인 셈블릭스는 1~3차 치료제를 사용해도 불구하고 효과를 보지 못한 환자들의 미충족 수요를 해결하기 위해 개발됐으며 FDA로부터는 2021년 10월 승인받았다.
노바티스는 만성골수성백혈병 1세대 치료제인 '글리백'부터 2세대 '타시그나', 3세대 '이클루시그'까지 백혈병 치료제 옵션 확대에 앞장서고 있다.
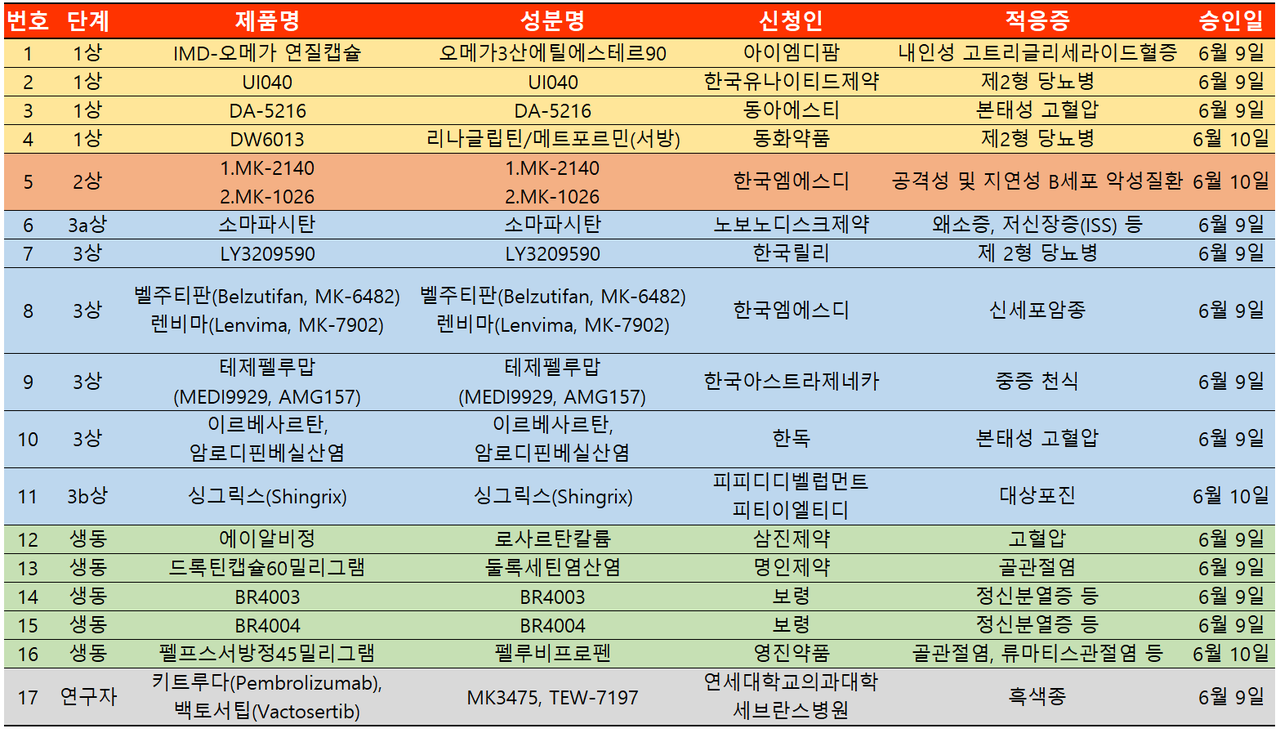
지난주 임상시험계획은 총 17건이 승인 완료됐다. 세부적으로 △임상1상 4건 △2상 1건 △3상 6건 △생물학적동등성 5건 △연구자임상 1건 등이다.
이번 임상시험은 제2형 당뇨병, 고혈압, 관절염 등 만성질환 치료제가 주로 승인받았으며 신세포암, 흑색종 등의 항암제 또한 승인받았다.
한국엠에스디가 신세포암종에 대해 식약처에 승인신청한 벨주티판, 렌비마의 경우 과거 항PD-1/L1 요법 이후 질병진행을 경험한 진행성 신세포암종 환자에서 치료를 위해 병합요법으로 카보잔티닙과 비교하는 라벨 공개, 무작위배정한 제3상 임상시험이다.
3상까지 진행해온 만큼 벨주티판은 이미 2021년 식약처로부터 벨주티판+키트루다 병용요법으로 신세포암종 보조요법제로 허가받은 바 있다.
벨주티판은 조직의 산소 수준을 조절하는 저산소증 유도인자-2α(HIF-2α)를 선택적으로 차단하는 기전을 가진 약물이다.
HIF-2α를 포함해 저산소증 유발인자로 알려진 단백질은 신체가 이를 올바르게 조절하지 못하는 환자에게 축적돼 적혈구 증식을 유발시키거나 암을 일으킨다.
한편 벨주티판은 올해 6월 3일부터 7일까지 열린 ASCO에서 임상데이터를 발표하며 향후 신세포암종의 새로운 치료 옵션으로 떠오르고 있다.

