성균관대 산학협 '2021년 의약품 허가특허연계제도 영향평가' 결과보고
작년 운영평가 결과, 기존 비슷한 제도 안정화 및 특허도전 활성화 시사

성균관대학교 산학협력단은 허가특허연계제도 도입의 긍정적 효과를 극대화할 수 있는 방안으로 적극적인 후발의약품 개발 지원과 정책 환경 조성의 필요성을 제언했다.
식품의약품안전처(처장 김강립)는 성균관대학교 산학협력단(주관연구책임자 손경복 교수)이 연구용역 과제로 실시한 '2021년 의약품 허가특허연계제도 영향평가' 연구결과보고서를 작년 29일 공개했다.
이 연구는 의약품허가특허연계제도 운영에 대해 2020년 발생한 운영실적을 평가하는 것을 목적으로 실시됐다.
우리나라는 '약사법' 제50조의11에 따라 허가특허연계제도가 국내 제약산업, 보건정책, 고용증감 등에 미치는 영향을 평가하고 국회에 보고토록 규정돼 있다.
허가특허연계제도 운영결과 평가 결과에 대해 연구진은 △등재 △판매금지 △우선판매품목허가는 기존과 비슷한 수준으로 제도의 안정화를, △통지는 증가하는 경향으로 특허도전의 활성화를 시사하고 있다고 평가했다.
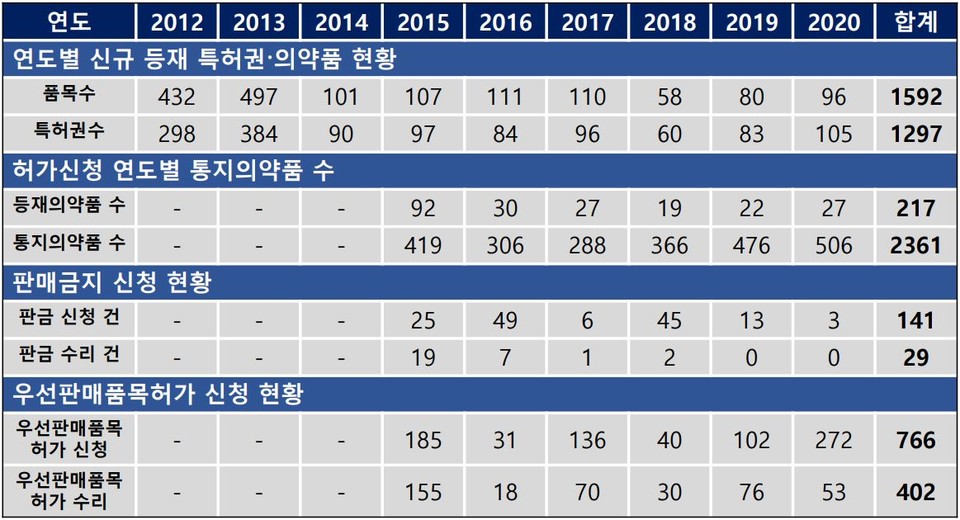
2020년 96개 품목에 대해 105개의 특허권이 등재됐다. 특허권자는 유럽(39.8%), 미국(25.4%), 한국, 일본이 전체 등재특허권의 약 97%를 차지했다.
또한, 2020년 27개 등재의약품에 대해 506개 후발의약품이 품목허가를 신청해 그 사실을 특허권자에게 통지했다. 후발의약품이 활발하게 특허에 도전하는 것을 반영해 2018년 이후 통지 의약품 수는 증가하고 있는 것으로 나타났다.
판매금지는 동기간 3개 후발의약품에 대해 특허권자가 신청했다. 다만, 후발제약사가 특허심판 등에서 승소해 판매금지가 되지 않았다. 판매금지가 되지 않은 주요 사유는 후발제약사가 승소했거나, 신청인이 자진취하했기 때문으로 확인됐다.
후발제약사는 동기간 우선판매품목허가를 272개 품목에 대해 신청했고, 53개 품목이 우선판매품목허가를 획득했다.
연구진은 이 수치들을 기반으로 판매금지 또는 우선판매품목허가가 발생했다가 2020년 만료된 경우를 대상으로 직·간접 영향을 평가했다.
직접 영향 평가 결과를 보면, 시장진입은 우선판매품목허가를 받은 후발의약품이 1.2~5.7개월 가량 시장에 조기 진입했다. 시장점유율로 봤을 때, 우선판매기간 종료 시점에 후발의약품의 시장점유율은 4.38~39.45% 더 높았다. 약품비 지출은 2.3~5.7억 원 절감됐다. 해당 제약사의 매출액은 8~15억 원 증가했다.
간접 영향 평가를 보면, 우선판매품목허가로 그렇지 않은 경우에 비해 연구개발비는 등재의약품 제약사의 연구개발비는 0.9~1.9억 원 감소하고, 후발의약품은 0.7~1.4억 원으로 증가했다.
제약사의 고용 변화도 나타났다. 등재의약품 제약사의 고용은 0.5명~1.1명이 감소하고, 후발의약품 제약사의 고용은 0.4~0.8명이 증가했다.
이 영향 평가를 기반으로, 연구진은 허가특허연계제도 도입의 긍정적 효과를 극대화할 수 있는 적극적인 후발의약품 개발 지원과 정책 환경 조성을 제안했다.
연구진은 "중장기 영향평가 결과 주사제와 경구제, 시장 규모가 작은 성분의 우선판매품목허가는 제한되었다"며 "제한된 후발의약품 개발 현황을 고려해 후발의약품 개발을 지원할 필요가 있다"고 해당 제약사에 대한 정보제공과 컨설팅을 대안으로 제시했다.
또한, "제네릭 사용량 증대는 제약사의 특허도전 및 우선판매품목허가 획득의 유인 구조를 바꿀 수 있는 중요한 내용"이라며 제네릭 사용량 증대를 위한 정책 환경 조성의 중요성을 시사했다.

