첫번째 환자군 코호트1 연구에서 ORR 14.8% 기록
"PR 14.8%, DOR 7.4개월, DCR 68.7% 확인"

항암 혁신신약 '포지오티닙'(Poziotinib)의 글로벌 임상2상(ZENITH20) 코호트1 연구 결과, 객관적 반응률(ORR)이 14.8%를 기록하며 1차 평가변수 목표 17%에 도달하지 못한 것으로 확인됐다.
27일 한미약품 파트너사인 미국 스펙트럼은 '과거 치료전력이 있는 EGFR 엑손20(Exon20) 삽입 변이 비소세포폐암 환자' 115명을 대상으로 진행한 포지오티닙의 첫번째 환자군 연구에서 이 같이 나타났다고 밝혔다.
스펙트럼에 따르면, 1차 평가변수 목표에는 도달하지 못한 반면 일부 긍정적인 결과도 있었다. 부분 반응(PR) 14.8%(17명), 반응 지속기간(DOR) 7.4개월, 질병조절율(DCR) 68.7%(79명) 등 유의미한 치료반응 데이터가 확인된 것이다.
스펙트럼은 이번 코호트1 임상의 세부 데이터를 면밀히 분석한 뒤 현재 진행 중인 나머지 6개 코호트 임상에 집중할 계획이다. 조 터전 스펙트럼 사장은 "2020년 공개될 코호트2·3 결과를 기대하고 있다. 2020년 1분기 내 전반적인 프로그램 전략 업데이트를 제공할 예정"이라고 했다.
프랑수아 레벨 CMO(최고의학책임자)는 "코호트1에서 다른 평가변수들을 통해 명백한 포지오티닙의 활성도를 확인했다"며 "현재 전반적인 분석 검토를 진행 중이며, 향후 학회를 통해 이 내용들을 발표할 계획"이라고 했다.
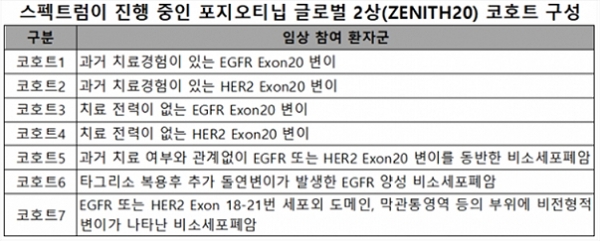
한편, 포지오티닙의 본임상 연구 'ZENITH20'(미국·캐나다·유럽 지역 등 글로벌 2상)은 총 7개의 코호트 연구로 구성돼 있다. 코호트1~4는 각각의 다른 통계학적 가설로 사전 명시된 객관적 반응율(ORR)을 1차 평가변수로 두고 있다. 코호트5~7은 연구 목적의 시험들로 구성됐으며 임상 프로토콜 계획대로 진행되고 있다. 이 중 코호트2~3은 임상 지속 진행을 위한 무용성평가(Futility Analysis)를 최근 통과해 2020년 내 임상결과가 발표될 예정이다.
포지오티닙은?
한미약품의 항암신약 포지오티닙은 2015년 3월 미국 제약기업 스펙트럼에 기술이전된 약물이다. 포지오티닙이 주목받는 이유는 엑손20(Exon20) 변이에 대한 높은 반응률 덕분이다. 지난해 9월 세계폐암학회(WCLC)에서 발표된 임상결과에 따르면, 포지오티닙을 투여한 비소세포폐암 환자 중 엑손20 변이가 나타나는 환자군에서 기존 EGFR 티로신키나아제억제(TKI) 치료제(8% 미만)보다 높은 43%의 객관적 반응률(ORR)이 나왔다.

