융복합지원단장과 전문가들로 혁신제품조정협의회 구성
허가심사 과정 중 이의제기 가능...민원인 소통창구 역할

의약품 등 허가심사 과정에서 보완 결정이 나올 경우 중도에 이의를 제기할 수 있는 ‘보완요구 조정신청제’가 오늘부터 본격 시행된다.
통상 행정행위에 대한 이의제기는 최종 행정결정이 나온 이후에야 소송 등을 통해 가능했는데, 식약처가 이번에 도입한 조정신청제는 허가심사 과정에서 민원인이 공식적으로 의견을 제기할 수 있는 소통의 통로를 연 것이어서 의미있다.
민원인이 조정신청을 할 수 있는 조정대상은 ▷보완사항이 관련 법령에 근거하고 있지 않다고 판단되는 경우 ▷융복합 혁신의료제품의 이중규제 해결을 요청하는 경우 ▷사전검토 통지서 또는 기술문서 적합통지서 수령 후 허가신청시 보완이 필요한 경우 등이다.
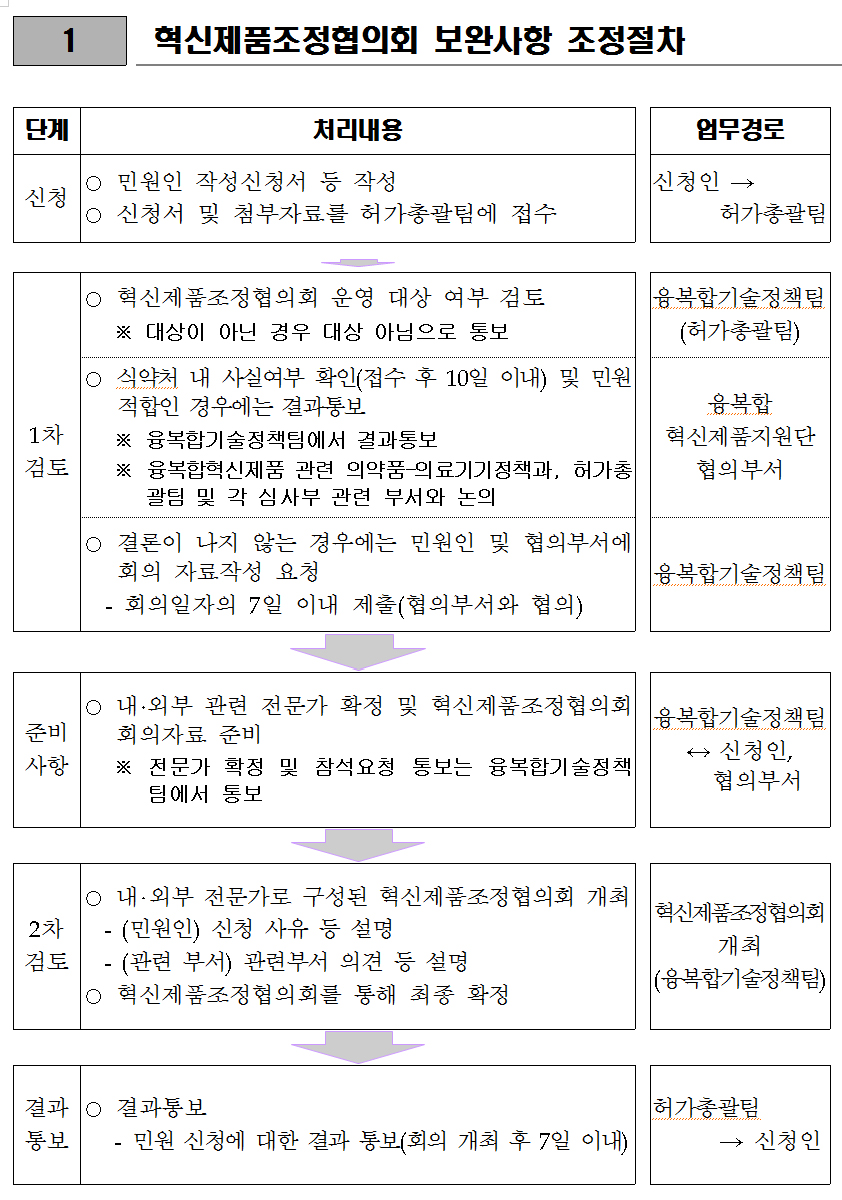
식약처는 융복합혁신제품지원단장과 산학연관 전문가로 혁신제품조정협의회를 구성하고 민원인들이 제기한 조정신청의 타당성 여부를 검토하여 회신한다.
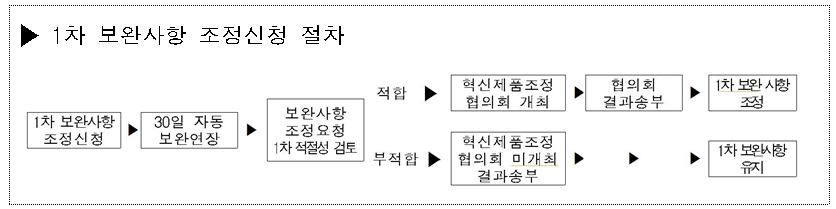
조정신청 절차는 1차 보완요구를 받은 후 10일 이내 조정을 신청하면 보완에 필요한 기간 30일은 자동 연장되고 혁신제품조정협의회 개최 후 조정신청 결과를 통보받게 된다.
조정신청제는 그 동안 담당 심사관에만 묶여 있던 민원업무 창구를 제3의 위원회로 확대시킨 것이어서 심사관의 심사업무 질 향상에도 기여할 것으로 보인다.
융복합혁신제품지원단 오정원 허가총괄팀장은 “조정신청제는 보완사항에 대한 민원 신뢰도를 높이고 행정절차의 투명성을 확보하기 위해 도입됐다”며 “민원인과 허가심사부처 간 소통을 확대할 것으로 기대한다”고 말했다.
관련기사
키워드
#융복합혁신제품지원단
박찬하
hahaha@hitnews.co.kr
헬스케어 생태계의 연결점은 사람! 사람에 대한 애정을 바탕으로 글쓰기를 즐기는 히트뉴스 기자입니다.

