국내 사용 가능한 코19 진단시약 16품목
정식허가 신청 18품목 · 임상적 성능시험계획 승인 14품목
코로나19와 독감(인플루엔자) 동시 진단시약은 1개 제품이 임상적 성능시험을 진행 중이며 다음 달에는 식품의약품안전처의 정식허가를 받을 전망이다.
식약처는 5일 이같이 밝혔다. 현재 코로나19 진단 등을 위해 국내 사용이 가능한 제품은 ▲확진 검사용 긴급사용승인 제품 7개 ▲응급 선별용 긴급사용승인 제품 9개 ▲정식허가 제품 1개로 총 16개 제품이다.
수출용으로 166개 제품이 허가됐다. 그 중 16개 제품이 미 식품의약국(FDA) EUA(긴급사용승인) 제품으로 등록돼 있다.
현재 유전자 진단시약(RT-PCR) 및 면역검사(항원검사, 항체검사) 등 총 18개의 코로나19 진단시약 제품이 임상적 성능시험을 거쳐 정식허가를 신청했다. 임상적 성능시험계획 승인을 받은 14개 제품이 성능시험 중에 있다.
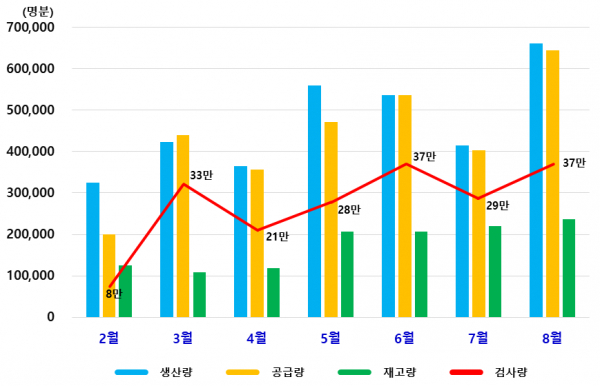
국내 방역에 사용 중인 코로나19 진단시약의 1일 최대 생산량은 약 16만명분이고, 현재까지 359만명분을 생산해 이중 329만명분이 공급됐다. 질병관리청 통계에 따르면, 지금까지 총 212만건의 검사를 진행했다.
확보된 재고 약 30만명분은 최근 일주일 동안 1일 평균 검사량 1.5만명분을 감안했을 때 약 20일 간 의료현장에 공급할 수 있는 물량이라 안정적인 수급을 이어가고 있다는 게 식약처의 설명.
한편, 수출용 코로나19 진단시약은 지난 달까지 150여개 국가에 총 1억9613만 명분을 수출했다. 지난 4월 3464만명분을 수출한 이후 8월까지 매월 3000만 명분 이상을 남아메리카, 미국 등 전세계로 수출하고 있다.
양진영 식품의약품안전처 차장은 15일 코로나19 진단시약 승인·허가 진행 상황 브리핑을 통해 "독감이 유행하는 계절이 다가옴에 따라 코로나19와 독감을 동시에 진단할 수 있는 진단시약이 신속하게 허가받을 수 있도록 노력하겠다"고 했다.
이어 "식약처는 앞으로도 코로나19 진단시약이 신속하게 허가를 받을 수 있게 적극 지원해 코로나19 극복에 도움이 될 수 있도록 최선을 다하겠다"고 했다.

