CT-P39 3상, CT-P43 1상 착수…CT-P17ㆍCT-P16와 차세대 성장동력 기대

셀트리온의 바이오시밀러가 글로벌 임상에 속속 진입한다.
셀트리온은 졸레어(알러지성 천식 및 만성 두드러기 치료제) 바이오시밀러 ‘CT-P39’이 글로벌 임상 3상에, 스텔라라(자가면역질환 치료제) 바이오시밀러 ‘CT-P43’는 글로벌 임상 1상에 착수했다고 12일 밝혔다.
졸레어는 제넨테크와 노바티스가 개발한 항체 바이오의약품으로 2019년 3조9000억원 매출(노바티스, 로슈 경영실적 자료 기준)을 기록한 블록버스터 제품으로, 셀트리온은 최근 글로벌 CRO(임상시험수탁기관) 회사와 계약을 체결하고 2022년까지 CT-P39 임상을 완료할 계획이다.
스텔라라는 얀센이 개발한 건선, 크론병, 궤양성 대장염 등 자가면역질환 치료제로, 2019년 존슨앤존슨 경영 실적 기준 매출 8조원을 기록했다.
셀트리온은 스텔라라 바이오시밀러 CT-P39에 대한 임상 역시 글로벌 CRO 계약 체결을 통해 진행하며 2021년 상반기까지 1상 임상 완료와 올해 하반기 글로벌 임상 3상 진입을 목표로 하고 있다.
두 개의 바이오시밀러는 지난 3월 유럽의약품청(EMA)에 승인을 신청한 CT-P17(휴미라 바이오 시밀러)과 현재 글로벌 임상 3상을 진행중인 CT-P16(아바스틴 바이오시밀러)와 함께 셀트리온의 차세대 성장동력의 한 축을 담당할 것으로 기대된다.
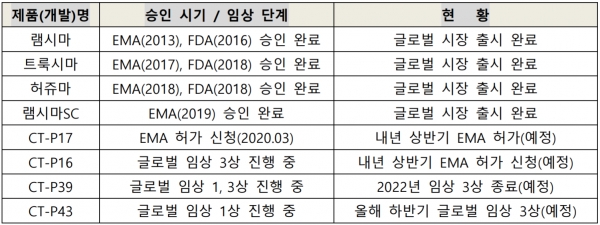
특히 인터루킨(IL)-12, 23 억제제 CT-P43이 상업화되면 셀트리온은 글로벌 TNF-α 억제제 강자인 램시마(IV, SC) 제품군 및 내년 상반기 EMA 허가가 예상되는 CT-P17을 포함해 자가면역질환 치료제 시장에서 강력하고 다양한 포트폴리오를 확보하게 된다.
셀트리온 관계자는 "셀트리온은 세계 최초의 항체 바이오시밀러 램시마를 필두로 글로벌 수준의 바이오의약품 개발 및 임상, 허가 역량을 갖추고 있다"며 "이번 CT-P39 및 CT-P43 임상을 성공적으로 진행해 미국, 유럽 등 글로벌 빅마켓에 제품을 조기에 선보일 수 있도록 노력하겠다"고 말했다.

