(2019.05.13~19) 97품목 시판 허가·11건 임상 승인
이미 포화상태인 디아세레인 성분의 골관절염치료제 제네릭이 지난주 5품목이 더 시판 허가됐다. 혈압강하제는 매주 10품목 이상씩 계속 허가가 이어지고 있다. 해외에서 시판된 지 10년이 넘은 만성 변비 치료제도 뒤늦게 신약으로 국내에 도입됐다.
▶ 품목 허가 현황 = 지난 한 주간(13~17일) 30개 질환군 97개 의약품이 새로 식약처로부터 시판허가받았다.
전주와 비교하면 질환군(전주 27개)은 3개가 늘었지만 품목수(전주 108개)는 오히려 11개 줄었다. 그만큼 다양한 제품이 새로 진입했다는 의미다. 제네릭의약품은 73품목으로 74.4%를 차지했다.
제제별로는 ▲ 혈압강하제 (14품목) ▲ 따로 분류되지 않는 대사성의약품 (8품목) ▲기타의 화학요법제·소화성궤양용제·진해거담제 (각 7품목) ▲ 기타의 중추신경용약·당뇨병용제 (각 6품목) ▲ 동맥경화용제·정신신경용제·주로 그람양성 음성균에 작용하는 것·하제,완장제 (각 4품목) ▲ 해열 진통 소염제·혈액응고저지제(항응고제) (각 3품목) ▲ 기타·기타의 알레르기용약·기타의 호흡기관용약·부신호르몬제·진통 진양 수렴 소염제·통풍치료제 (각 2품목) ▲ 간장질환용제·국소마취제·기생성피부질환용제·기타의 비뇨생식기관용약·기타의 순환계용약·안과용제·이비과용제·주로 그람양성균 리케치아 바루스에 작용하는 것·치과구강용약·항히스타민제·혈관확장제 (각 1품목) 순이었다.

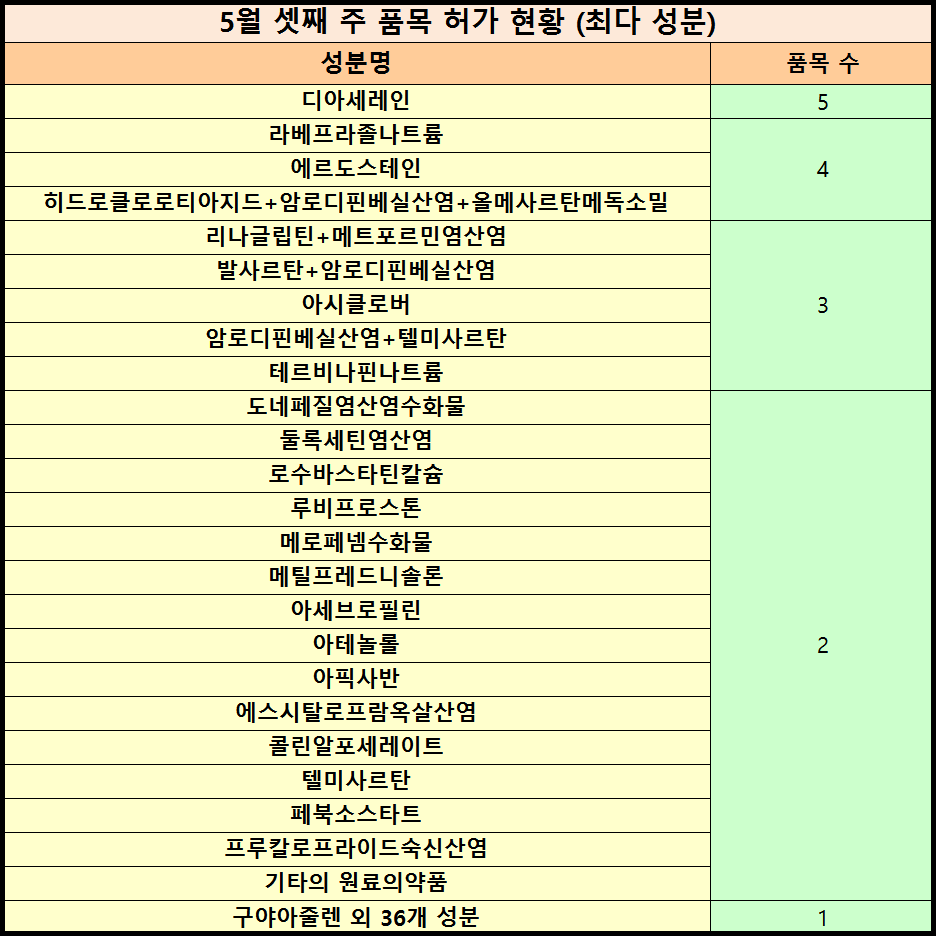
성분별로는 ▲ 디아세레인 (5품목) ▲ 라베프라졸나트륨·에르도스테인·히드로클로로티아지드+암로디핀베실산염+올메사르탄메독소밀 (각 4품목) ▲ 리나글립틴+메트포르민염산염·발사르탄+암로디핀베실산염·아시클로버·암로디핀베실산염+텔미사르탄·테르비나핀나트륨 (각 3품목) ▲ 도네페질염산염수화물·둘록세틴염산염·로수바스타틴칼슘·루비프로스톤·메로페넴수화물·메틸프레드니솔론·아세브로필린·아테놀롤·아픽사반·에스시탈로프람옥살산염·콜린알포세레이트·텔미사르탄·페북소스타트·프루칼로프라이드숙신산염·기타 원료의약품 (각 2품목) ▲ 구아야줄렌 외 총 36개 성분 (각 1품목) 등으로 분포했다.
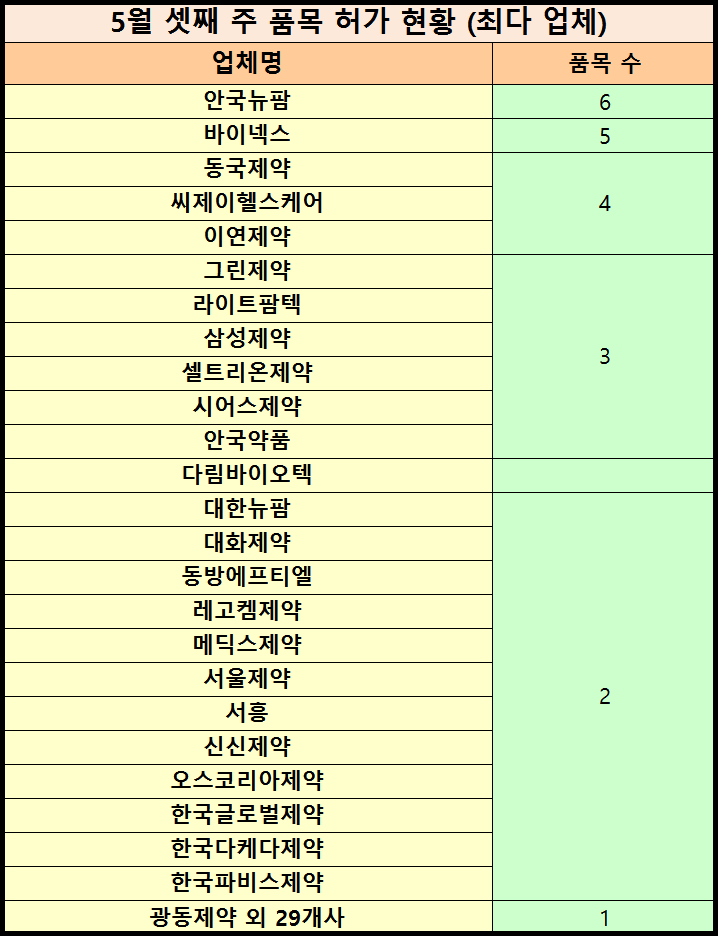
업체별로는 ▲ 안국뉴팜 (6품목) ▲ 바이넥스 (5품목) ▲ 동국제약·씨제이헬스케어·이연제약 (4품목) ▲ 그린제약·라이트팜텍·삼성제약·셀트리온제약·시어스제약·안국약품 (3품목) ▲ 다림바이오텍·대한뉴팜·대화제약·동방에프티엘·레고켐제약·메딕스제약·서울제약·서흥·신신제약·오스코리아제약·한국글로벌제약·한국다케다제약·한국파비스제약 (각 2품목) ▲ 광동제약·구주제약·뉴젠팜·대웅제약·대웅바이오·대원제약·동구바이오제약·씨티씨바이오·아리제약·아주약품·알피바이오·유니메드제약·유한양행·오스틴제약·이니스트바이오제약·일양약품·일화·제이에스제약·제일헬스사이언스·정우신약·주식회사다나젠·중헌제약·조아제약·코스맥스파마·콜마파마·태극제약·테라젠이텍스·한국신약·한국파마·현대약품 (각 1품목) 등의 순으로 많았다.
디아세레인 성분의 경우 골(고관절, 슬관절) 관절염(관절증, 퇴행성관절질환) 적응증을 갖고 있는데, 명문제약이 1988년 '아트로다캡슐'을 선보인 이후 50여개 제네릭이 현재 시판되고 있다. 이런 와중에 바이넥스, 한국파비스제약, 안국뉴팜, 안국약품, 대한뉴팜 등 5개사가 지난 주 제품을 더 추가했다.
한국다케다제약은 변비 치료신약 '아미티자연질캡슐(루비프로스톤)'을 새로 국내에 도입했다. 성인에서 만성 특발성 변비의 치료와 만성 비암성 통증 성인환자에서 마약성 진통제(opioid) 유발성 변비의 치료에 쓰인다.
▶ 임상 승인 현황 = 같은 기간 총 11건의 임상시험이 승인됐다. 시험단계별로 ▲ 생동 (2건) ▲ 1/2상 (1건) ▲ 1상 (2건) ▲ 1b상 (1건) ▲ 2상 (1건) ▲ 3상 (1건) ▲ 연구자임상시험 (3건) 등으로 나타났다.
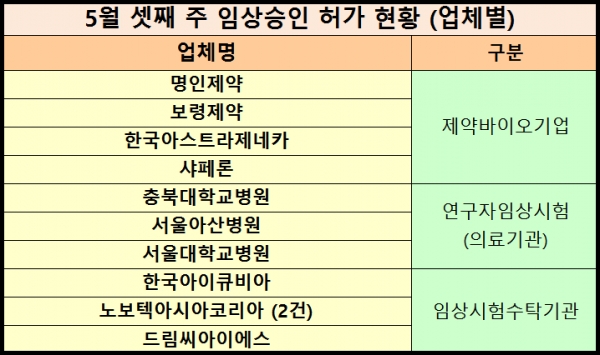
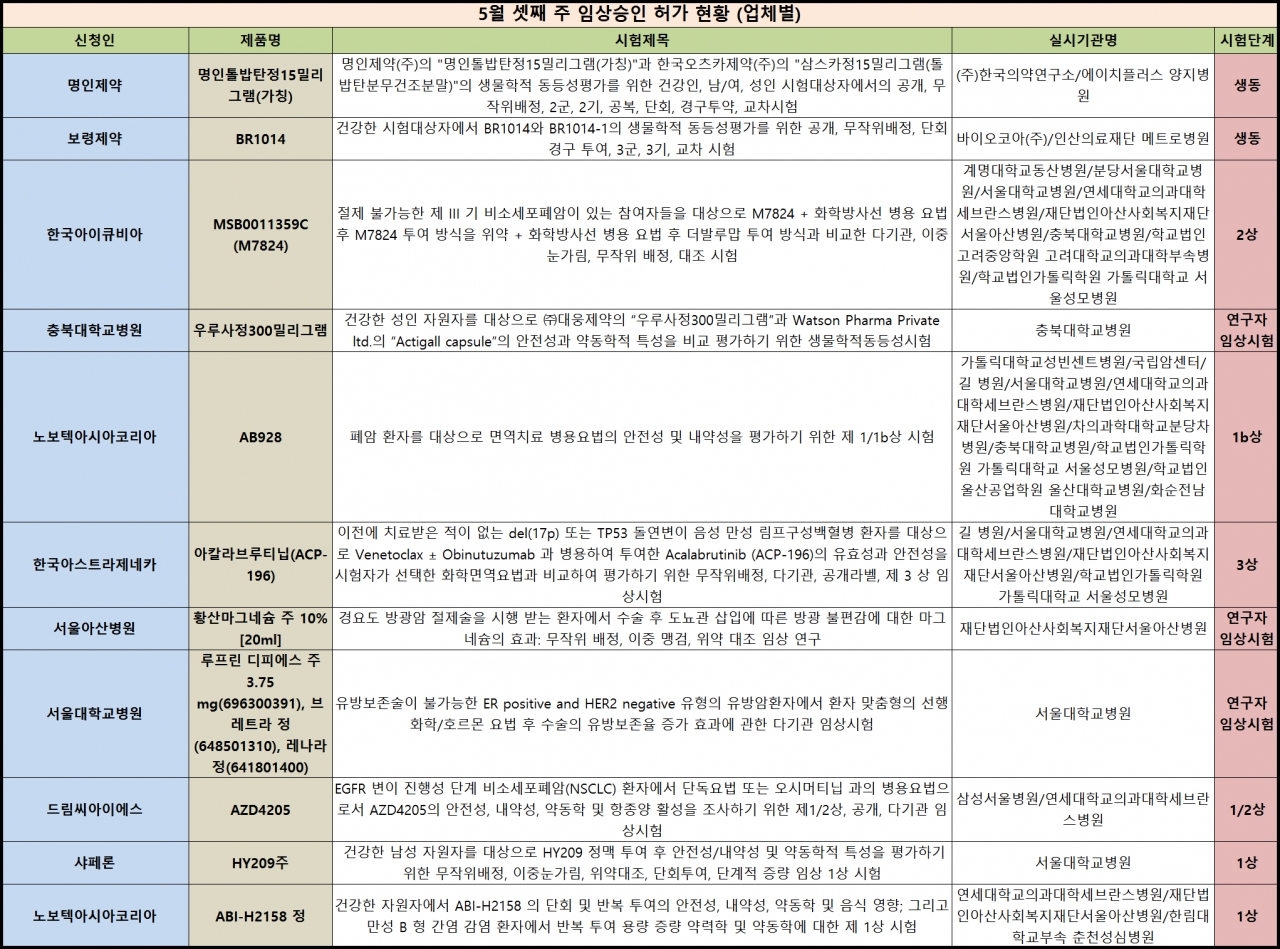
신청주체별로는 제약바이오기업 3건, 임상시험 수탁전문기업(CRO) 4건, 의료기관 3건 등으로 분포했다. 서울아산병원은 황산마그네슘 주 10% [20ml]를 투여해 경요도 방광암 절제술을 시행 받는 환자에게 수술 후 도뇨관 삽입에 따른 방광 불편감에 대한 마그네슘의 효과를 비교하기 위한 무작위 배정, 이중 맹검, 위약 대조 임상 연구를 승인받았다.
서울대학교병원은 다케다제약의 자궁근종 주사제 루프린 디피에스 주 3.75mg, 신풍제약의 유방암치료제 브레트라 정, 광동제약의 유방암치료제 레나라 정을 '유방보존술이 불가능한 ER positive and HER2 negative 유형'의 유방암환자에게 투여해 환자 맞춤형의 선행화학/호르몬 요법 후 수술의 유방보존율 증가 효과를 파악하기 위한 시험을 진행하기로 했다.
충북대학교병원은 '우루사정300밀리그램'과 Watson Pharma Private ltd.의 'Actigall capsule'의 안전성과 약동학적 특성을 비교 평가하기 위한 생동시험을 승인받았다.
아스트라제네카는 BTK억제제 아칼라브루티닙(ACP-196)을 이전에 치료받은 적이 없는 del(17p) 또는 TP53 돌연변이 음성 만성 림프구성백혈병 환자를 대상으로 Venetoclax ± Obinutuzumab과 병용하는 임상시험을 승인받았다.Acalabrutinib (ACP-196)의 유효성과 안전성을 시험자가 선택한 화학면역요법과 비교해 평가하기 위한 무작위배정, 다기관, 공개라벨 등으로 진행할 예정이다.
드림씨아이엔스는 EGFR 변이 진행성 단계 비소세포폐암(NSCLC) 환자에서 단독요법 또는 오시머티닙과 병용요법으로 'AZD4205'의 안전성, 내약성, 약동학 및 항종양 활성을 조사하기 위한 제1/2상, 공개, 다기관 임상시험을 승인 받았다.
노보텍아시아코리아는 ▶ 폐암 환자를 대상으로 면역치료 병용요법의 안전성 및 내약성을 평가하기 위한 제 1/1b상 시험 ▶ 건강한 자원자에서 ABI-H2158 의 단회 및 반복 투여의 안전성, 내약성, 약동학 및 음식 영향, 만성 B 형 간염 감염 환자에서 반복 투여 용량 증량 약력학 및 약동학에 대한 제 1상 시험을 진행한다.
각각 폐암 환자의 면역치료제와 만성 B형 간염치료제를 개발하려는 움직임으로 포착된다.
한국아이큐비아는 시험약 'MSB0011359C (M7824)'을 가지고 절제 불가능한 제 3기 비소세포폐암이 있는 참여자들을 대상으로 M7824 + 화학방사선 병용 요법 후 M7824 투여 방식을 위약 + 화학방사선 병용 요법 후 더발루맙 투여 방식과 비교한 다기관, 이중 눈가림, 무작위 배정, 대조 시험 등의 임상 2상을 승인 받았다.
2008년 설립된 벤처기업 샤페론은 개발 중인 염증완화치료제 'HY209주(성분명 타우로데옥시콜린산나트륨)'의 패혈증치료제 개발에 대한 1상 임상을 승인받았다. 건강한 남성 자원자를 대상으로 HY209 정맥 투여 후 안전성/내약성 및 약동학적 특성을 평가하기 위한 무작위배정, 이중눈가림, 위약대조, 단회투여, 단계적 증량 방식으로 시험을 진행할 예정이다. HY209주는 신체유래물질을 기반으로 한 약물로 알려져 있다.

