7번째 GMP 서면확인서 면제 국가로

식품의약품안전처(처장 이의경)는 14일(현지시각) 벨기에 브뤼셀에서 유럽연합(EU)이 이사회를 열고 우리나라를 7번째로 EU 화이트리스트(GMP 서면확인서 면제 국가)에 등재했다고 15일 밝혔다.
앞으로 국내 제약사는 EU에 수출하는 원료의약품에 대한 GMP 서면확인서 제출을 면제받는다. 수출을 위한 소요시간이 약 4개월 이상 단축된다.
EU 비회원국은 원료이약품을 EU로 수출할 때 반드시 GMP 서면확인서를 제출해야 한다.
그러나 EU 화이트리스트에 등재되면 이 확인서 제출을 면제받는 것이다.
EU 화이트리스트는 EU 집행위원회가 등재국의 GMP 기준 및 운영체계가 EU GMP 기준과 동등한지 직접 평가한 국가들로, EU가 GMP분야에서 인정하는 국가 목록이다.
식약처는 "우리나라가 이 리스트에 등재된 것은 국내 원료의약품 GMP 운영체계나 국내 제약사의 원료의약품 품질이 EU는 물론 미국, 일본 등 제약 선진국과도 동등한 수준임을 전 세계적으로 인정받은 것"이라고 평가했다.
지난달까지 EU 화이트리스트에 등재된 국가는 스위스, 호주, 일본, 미국, 이스라엘, 브라질 등 총 6개국이었다.
아울러 식약처는 "이번 화이트리스트 등재는 지난 2014년 가입한 의약품실사상호협력기구(PIC/S)에 이어 다시 한 번 우리나라 제약 산업의 글로벌 시장 진출의 기폭제가 될 것"이라며 기대감을 드러냈다.
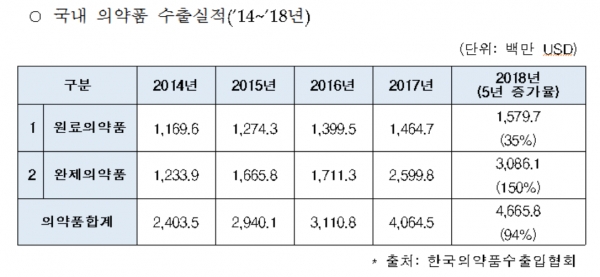
실제 국내 의약품 수출액은 2014년 24억400만달러에서 2018년 46억6600만달러로 PIC/S 가입 후 94% 상승했다.
한국의약품수출입협회에 따르면 2014년 12억339만달러였던 완제의약품 수출실적은 2015년 16억658만달러, 2016년 17억113만달러, 2017년 25억998만달러, 2018년 30억861만달러로 무려 150% 가량 증가했다.
원료의약품 수출실적은 2014년 11억696만달러, 2015년 12억743만달러, 2016년 13억995만달러, 2017년 14억647만달러, 2018년 15억797만달러로 5년전에 비해 35% 증가했다.
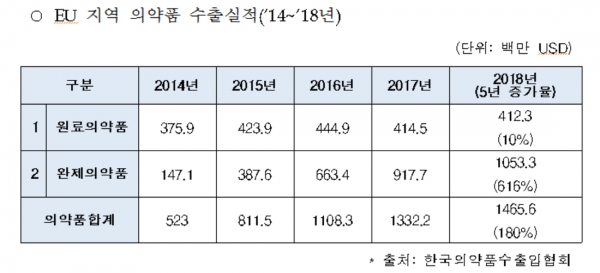
EU 지역에 한정하면 2014년 5억230만달러, 2015년 8억115만달러, 2016년 11억83만달러, 2017년 13억322만달러, 2018년 14억656만달러로 180% 성장했다.
원료의약품은 2014년 3억759만달러에서 2015년 4억239만달러, 2016년 4억449만달러, 2017년 4억145만달러, 2018년 4억123만달러로 10% 가량 증가했지만 완제의약품은 2014년 1억471만달러, 2015년 3억876만달러, 2016년 6억634만달러, 2017년 9억177만달러, 2018년 10억533만달러로 616%나 증가했다.
식약처는 "직접적으로 미국 다음으로 의약품 시장규모가 크고 국내 의약품 수출액의 31%를 차지하고 있는 EU를 중심으로 수출이 확대되고 관련 산업이 성장할 것"으로 예상했다.
이어 "EU의 경우 의료보장비용 절감 등을 이유로 제네릭 의약품을 확대하는 상황에서, 국내 제약산업에서 높은 비중을 차지하는 제네릭 의약품의 원료의약품 생산 업체에 수출 확대의 호재가 될 것"이라고 강조했다.
아울러 장기적으로 제네릭 의약품을 중심으로 시장이 형성돼 있는 러시아 등 독립국가연합(CIS)이나 최근 의약품 분야 국가 간 협력이 강화되고 있는 베트남 등 아세안 시장으로의 진출도 기대할 수 있게 됐다.
식약처는 "이번 EU 화이트리스트 등재가 2015년 1월 신청서를 제출한 이후 전담 대응팀을 중심으로 4년여 간 치밀하게 현장평가와 평가단 면담 등 심사절차에 대응한 결실"이라며 "앞으로도 우리 의약품의 품질경쟁력에 기반한 글로벌 시장 진출 확대를 위해 국가 간 협력을 강화하고 각종 국제 협의체 활동에 적극적으로 참여하겠다"고 했다.

