유한, 선도물질-탐색 단계 2건 계약...JW중외, 에이비엘바이오 등도
물질탐색을 포함한 전임상 단계서 조기 기술수출에 성공하는 사례가 늘어 주목된다.
유한양행이 7일 길리어드사에 기술수출한 비알콜성지방간염치료제(NASH) 신약후보물질 2건은 모두 전임상 단계서 계약이 체결됐다.
관련 업계와 유한양행 관계자의 말을 종합하면, NASH 파이프라인 2건은 선도물질 단계인 YHC1102와 탐색단계인 YHC1117, YHC1108 중 하나로 예상되는데 GLP 독성연구 수준까지만 진행됐다.
이처럼 전임상 단계서 조기 기술 수출된 파이프라인은 ▲JW중외제약의 JW1601(전임상 단계 신약후보물질로 전임상 독성시험 진행) ▲에이비엘바이오(전임상 단계 후보물질 5개, 독성시험 시행 전 단계) 등으로 작년 하반기부터 속속 나타났다.
신약개발 관계자는 "유한 사례처럼 개발후보물질이 정해지고 IND 전 라이선스아웃(license-out)되는 사례는 해외서도 많이 있다"며 "전임상 약효 시험에서 효력이 좋고, GLP 독성시험에서 안전성이 상당 수준 입증이 된다면 충분히 가능한 사례"라고 했다.

지난해 ▲동아에스티가 누로보파마슈티컬즈에 기술수출한 당뇨병성신경병증치료제 'DA-9801'은 임상 2상을 미국에서 완료된 뒤 ▲유한양행 퇴행성디스크 치료제 YH14618과 레이저티닙은 각각 임상 2상과 임상1/2상에서 ▲크리스탈지노믹스의 CG400549는 임상 2a상 ▲인트론바이오의 슈퍼박테리아항생제는 임상 1상 단계에서 기술수출 됐다.
실제 사람 대상 임상을 진행하기 전 단계인 전임상(pre-clinical)은 새로 개발한 신약후보물질을 실험 동물에게 사용해 부작용이나 독성, 효과 등을 알아보는 과정이다. 약물이 체내에 어떻게 흡수, 분포, 배설되는지 알아보는 체내동태연구와 약효약리연구가 이뤄진다. 이후 부작용 및 독성을 검색하는 안전성 평가가 실시된다.
업계 관계자들에 따르면, 유한양행이 이번에 기술수출한 파이프라인은 전임상 단계서 독성시험까지 일정 부분 진행됐다.
현재 JP모건 컨퍼런스에 참석 중인 최순규 유한양행 연구소장은 기술수출 의미와 후보물질에 대한 기대와 관련 "유한양행 자체 R&D 기술력의 성과가 인정받은 것"이라며 "후보물질 도출 전의 기술수출로써, 향후 길리어드와 공동연구를 통해 유한의 신약개발 역량도 크게 발전할 것으로 기대한다"고 했다.
길리아드사 기출수출로 유한은 퇴행성 디스크 치료제 YH14618, 11월 비소세포폐암 신약후보물질 레이저티닙 등 3연타석 홈런을 쳤다. 이로써 유한은 계약금만 총 6565만달러(약 730억원)를 벌었다.
유한은 YH14618을 미국 스파인바이오파마(Spine Biopharma)에 기술수출해 국내를 제외한 전세계 독점실시권을 허여하는 계약을 맺었다. 이 계약으로 총 기술수출 금액은 2억1815만달러(약 2441억원)로 계약금 규모는 65만달러(약 7억원)다. 또 얀센에 레이저티닙을 수출해 계약금 5000만달러(약 550억원)를 포함해 총 12억500만달러(약 1조3255억원) 규모 계약을 성사시켰다.
유한은 종양 파이프라인을 중심으로 비알코올성지방간염, 비만, 퇴행성디스크, 변비 등으로 다양한 신약개발 파이프라인을 구축했다.
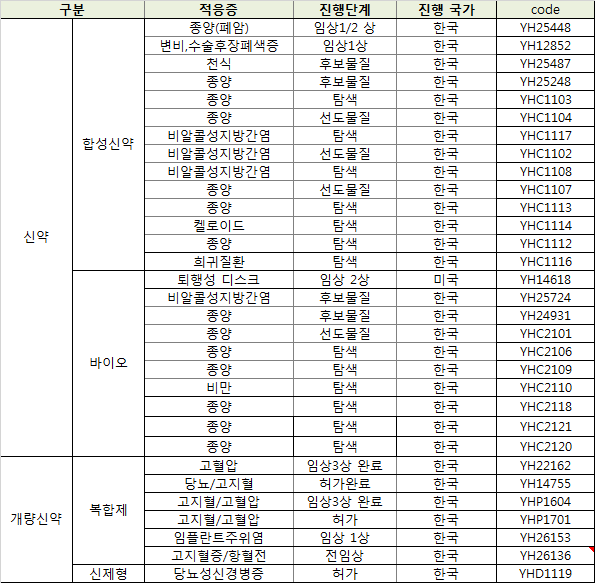
현재까지 공개된 유한의 파이프라인은 종양관련 파이프라인이 14개로 가장 많고, 비알코올성지방간염 파이프라인도 4개로 그 뒤를 이었다.
한편 술을 먹지 않아도 간염에 걸릴 수 있는 비알코올성 지방간염(NASH)는 평균 발병률은 10-24%이며, 비만한 사람은 약 58-74%까지 걸릴 수 있지만 아직까지 특별한 치료제가 없다. 지난해 글로벌 투자은행 골드만삭사는 올해를 ‘NASH의 해’로 선포하고 ‘블로버스터 신약’이 등장할 것으로 전망했을 정도로 NASH 신약 개발에 대한 관심은 전 세계적으로도 뜨겁다. 미국 시장 조사 결과에 따르면, 2009년 NASH 시장 규모는 약 5억 달러였고, 향후 10년간 연평균 45%씩 증가해 2026년에는 약 253억달러(약 28조원)에 이를 것으로 예측된다.
현재 제품화에 가장 근접한 임상 3상 단계에 진입한 NASH 치료제 파이프라인을 가진 회사로는 ▲엘러간 세니크리비록 ▲길리어드 셀론설팁 ▲인터셉트파마슈티컬 오칼리바 ▲장피트 ▲젠핏 엘라피브라노 5개사가 있다.
국내 제약사 역시 NASH 치료제 개발에 적극적이다. 지난해 NASH 치료제 개발을 위해 임상 1상 허가를 받은 국내 제약사는 CJ헬스케어를 포함해 한미약품, 동아에스티, 휴온스, 삼일제약 등이 있다. NASH 치료제 개발에 가장 앞선 곳은 휴온스의 HL정과 삼일제약의 아람콜로 이미 임상 2상과 임상 2b상을 마쳤다. 또 동아에스티의 에보글립틴과 한미약품의 HM152111, CJ헬스케어는 임상1상을 진행 중이다.
김원 서울대학교 의과대학 보라매병원 내과 교수는 대한간학회 기고문을 통해 “현재 NASH 치료제로 승인된 약제가 전혀 없고, NASH 확진에 간생검이 반드시 필요하여 진단율이 낮다는 점, 드문 약물 처방 빈도, 적극적으로 치료를 희망하는 환자들이 많지 않다”며 “국내에서도 항산화제, 항당뇨병약 및 항고지혈증약 등이 현재 NASH 환자에서 가장 널리 사용되는 오프라벨(off-label) 약물”이라고 언급했다.

