Trop-2 타겟 ADC '트로델비', 삼중음성유방암 3차 치료제로 허가
LG화학, 2019년 미국 빌게이츠 재단 지원 이후 6가 백신 개발 지속
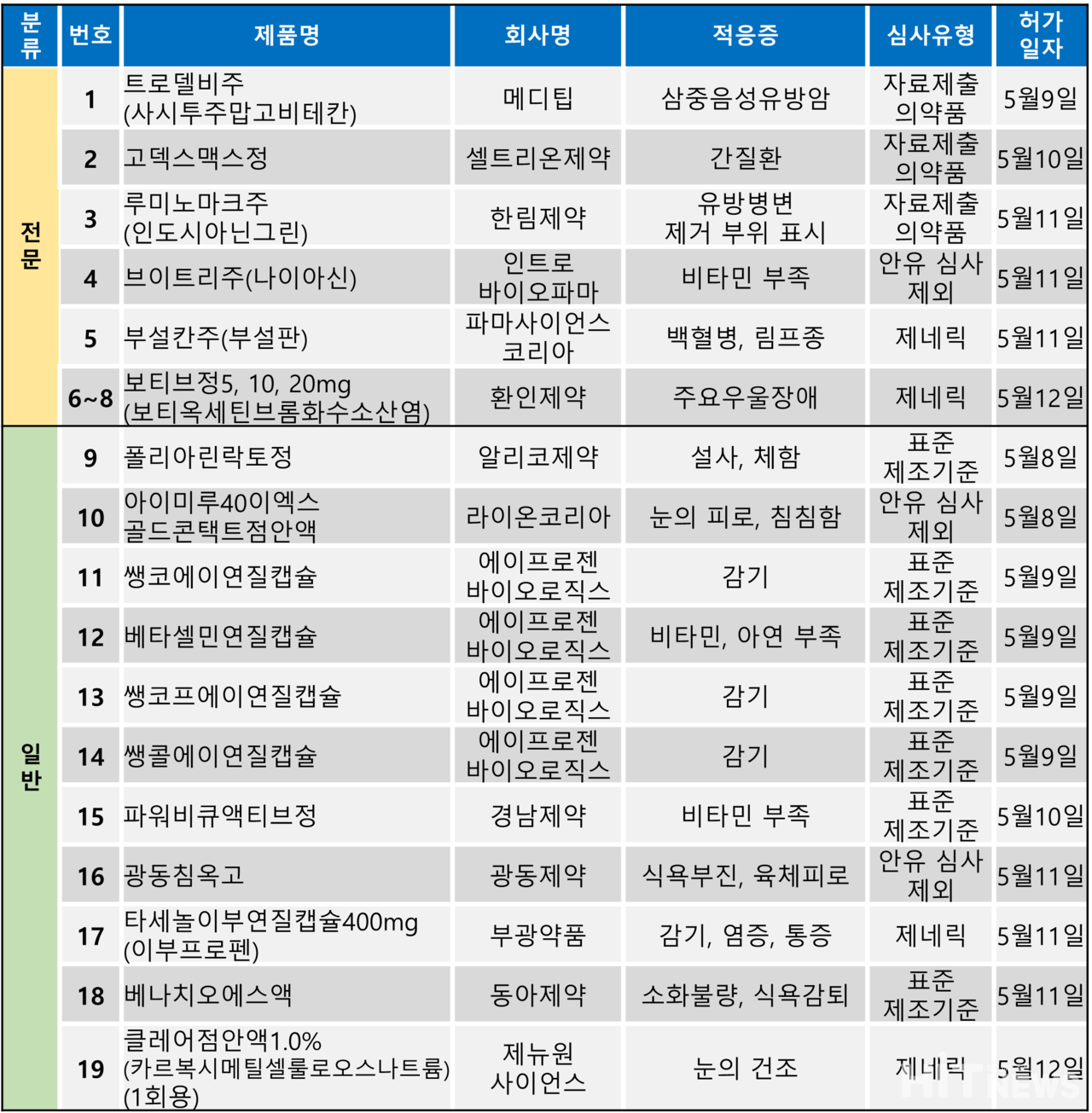
지난주(5월 8~12일) 총 19개 품목이 식품의약품안전처로부터 품목허가를 받았다. 전문의약품은 8개 품목, 일반의약품은 11개 품목이었다. 허가 품목들은 삼중음성유방암, 간질환, 백혈병, 주요우울장애 등 다양한 적응증으로 허가됐다.
미국 제약사 길리어드가 개발한 삼중음성유방암 항체약물접합체(ADCㆍAntibody-Drug Conjugate) 치료제 '트로델비주(성분 사시투주맙고비테만)'가 지난 9일 허가됐다. 국내 허가는 의약품 허가 컨설팅업체인 '메디팁'이 진행했다. 트로델비주는 '이전에 두 번 이상의 전신 치료를 받은 적이 있고, 그 중 적어도 한번은 전이성 질환에서 치료받은, 절제 불가능한 국소 진행성 또는 전이성 삼중음성유방암'을 적응증으로 허가됐다. 삼중음성유방암은 에스트로겐 수용체(ER), 프로게스테론 수용체(PR) 및 사람상피세포성장인자수용체2형(HER2) 등 3가지 수용체의 발현이 모두 음성인 유방암으로, 전체 유방암 환자 중 약 15~20%를 차지할 것으로 추정되고 있다.
식약처에 따르면, 트로델비주는 유방암 세포의 표면에서 많이 관찰되는 Trop-2(영양막 세포 표면 항원-2) 단백질을 표적으로 하는 ADC 치료제다. 이 약물의 항체(사시투주맙) 부분이 세포 표면에 발현된 Trop-2에 결합하면서 세포 내로 이동하며, 세포 내에서 세포 분열을 억제하는 약물(SN-38, SN-38 glucuronide)을 방출해 암세포의 사멸을 유도한다.
한편 길리어드는 기존 미국 식품의약국(FDA)으로부터 허가받은 트로델비주의 적응증인 전이성 삼중음성유방암, 전이성 요로상피세포암 적응증 외에 지난 2월 3일 HR(호르몬수용체)+/HER2- 전이성 유방암 환자를 대상으로 적응증을 확장한 바 있다. 회사는 이 적응증으로 허가받기 위해 '절제가 불가능한 국소 진행성 또는 전이성 HR+/HER2- 유방암 환자'를 대상으로 임상 3상(TROPiCS-02)을 진행했다. 임상 결과에 따르면, 트로델비주는 화학항암제 단독투여 대비 mOS(전체 생존율 중간값)와 mPFS(무진행 생존기간 중간값) 모두에서 유의미한 개선을 보인 것으로 나타났다.
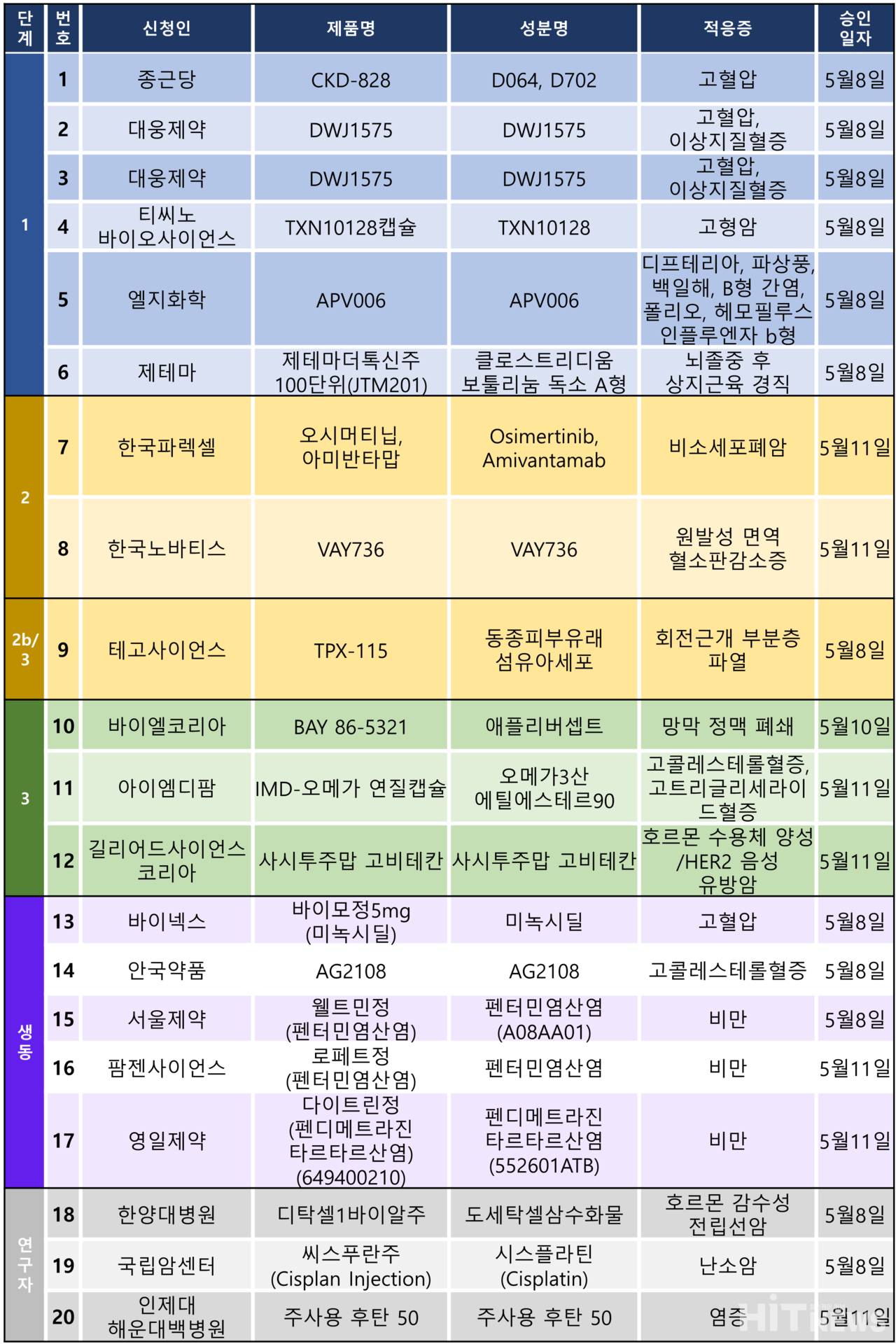
임상시험계획은 총 20건이 승인됐다. 세부적으로 △임상 1상 6건 △임상 2상 2건 △임상 2b/3상 1건 △임상 3상 3건 △생물학적동등성 5건 △연구자임상 3건 등이다. 이 임상시험들은 고혈압, 이상지질혈증, 원발성 면역 혈소판 감소증, 망막 정맥 폐쇄 등 다양한 질환과 고형암, 비소세포폐암, 유방암, 난소암 등 암종을 대상으로 승인됐다.
LG화학이 개발 중인 6가 혼합백신인 'APV006'의 1상 임상시험계획이 지난 8일 식약처로부터 승인됐다. APV006은 △디프테리아(Diphtheria) △파상풍(Tetanus) △백일해(Pertussis) △B형 간염(Hepatitis B) △폴리오(Poliovirus) △헤모필루스 인플루엔자 b형 (Haemophilus influenzae type b)에 의한 침습성 질환 등의 예방을 위한 6가 혼합백신이다. 이번 임상은 국내 환자를 대상으로만 진행되며, 목표 대상자 수는 42명이다. 연구 책임자는 김남중 서울대 교수가 맡았으며, 예상 임상 종료일은 내년 2월이다.
해당 임상의 1차 유효성 평가변수로는 △이상반응(AE)(①Immediate reactions(임상시험용 백신 접종 후 30분 이내에 발생한 모든 이상반응), ②Solicited AE(임상시험용 백신 접종 후 7일간 발현된 예측된 이상반응), ③Unsolicited AE(동의서 취득 이후 임상시험 기간 동안 발현된 Solicited AE를 제외한 모든 이상반응) △실험실 검사 △활력징후 △신체검진 △심전도 등이 설정됐다.
한편 LG화학은 지난 2019년 미국 빌앤드멀린다게이츠재단(Bill & Melinda Gates Foundation)으로부터 약 3340만달러(450억원) 규모의 개발비를 지원받아 개발도상국 영유아를 위한 6가 혼합백신(디프테리아ㆍ파상풍ㆍ백일해ㆍB형 간염ㆍ뇌수막염ㆍ소아마비) 개발을 지속해 왔다. 당시 회사는 2023년부터 유니세프(UNICEF) 등 국제 기구를 통해 세계에 6가 백신을 공급할 것이라고 발표한 바 있다. 이를 위해 현재 동남아시아에서 임상 2/3상을 진행 중이다.
이 외에도 지난 3월 유니세프와 소아마비 백신 '유폴리오'와 5가 혼합백신 '유펜타'의 수주 계약을 체결하는 등 영유아를 대상으로 한 글로벌 백신 공급에 박차를 가하고 있다. 공급 규모는 각 1억달러(약 1300억원)로, 회사는 유폴리오를 2024년부터 2년간, 유펜타의 경우 5년간 공급하게 된다.
관련기사
- 길리어드, 삼중음성유방암 ADC 치료제 '트로델비' 국내 허가
- "트로델비, 첫 HR+/HER2- 유방암 타깃 ADC"
- [허가/임상] TZD·DPP-4i·메트 3제 복합 당뇨약 '듀비메트에스' 허가
- [허가/임상] 암젠 ASCVD RNAi 치료제 '올파시란' 3상 승인
- [허가/임상] 장 정결제 오라팡 상대로 수푸렙미니정 등장
- [허가/임상] 릭시아나 후발약 허가, BsAb 항암제 탈라타맙 3상 승인
- [허가/임상] 한 주간 임상시험계획 31건 승인
- [허가/임상] 뇌전증치료제 세노바메이트 청소년 임상3상 승인
- [허가/임상] 소아 관절염 젤잔즈시럽, 혈우병A 오비주르 허가
- [허가/임상] 다발골수종 CAR-T 카빅티, 빈혈 바다넴 허가

