에페리손과 아세클로페낙 성분 첫 복합제... 1500억 시장
아두카누맙, 3b상으로 국내 승인... 국내 11명 참가 예정

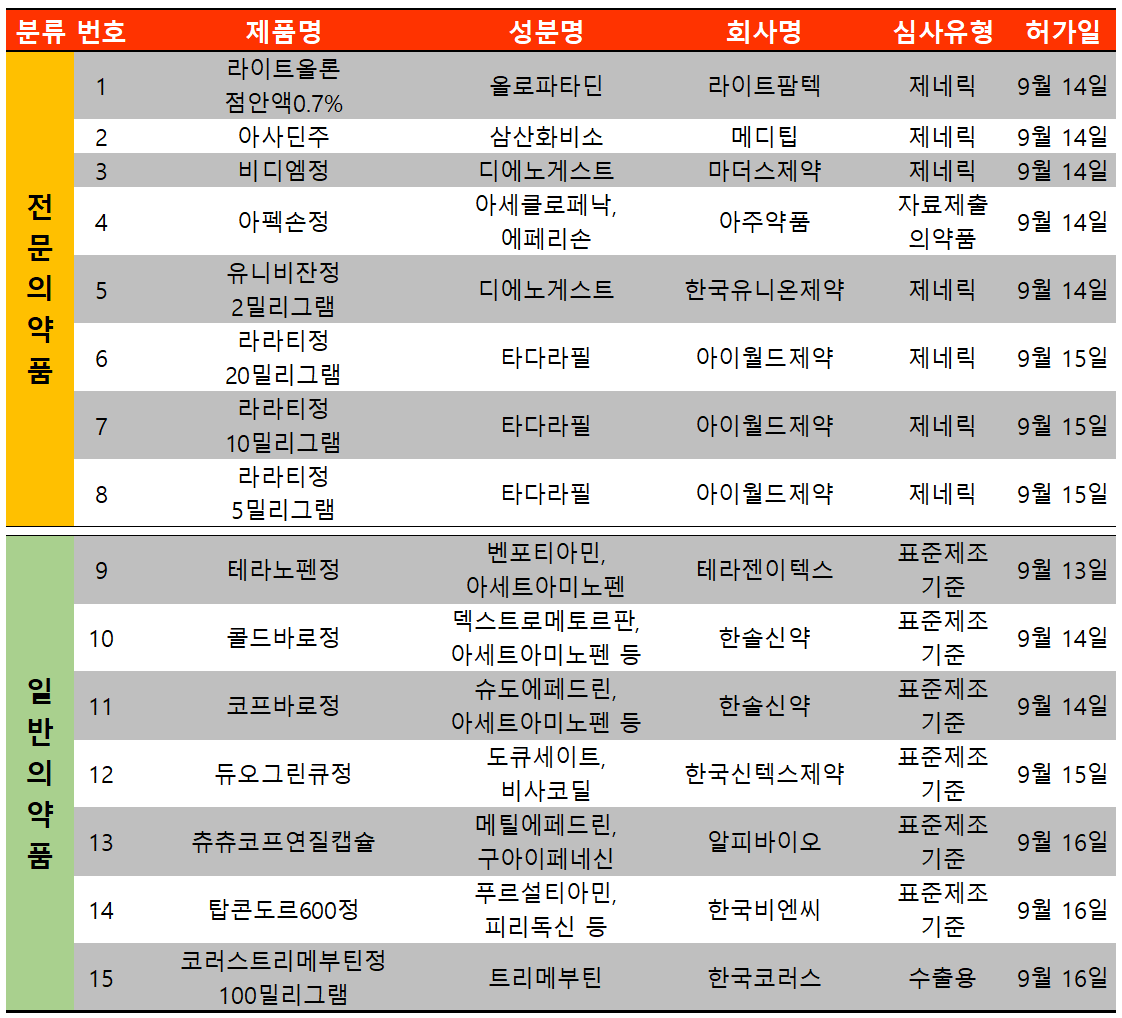
지난주(9월 12일~9월 18일) 15개 품목이 식품의약품안전처에서 허가받았다. 전문의약품은 8건, 일반의약품은 7건이었다.
지난 8월 급여적정성 재평가에 대한 평가 결과가 제약사에게 통보된 가운데 주요 처방 적응증에서 급여적정성이 있는 것으로 결정된 에페리손의 복합제가 허가받았다.
아주약품 아펙손정(성분 아세클로페낙, 에페리손)이 주인공으로 통증치료제로 쓰이던 두 성분을 합친 복합제다.
아펙손은 급여는 축소됐지만 적정성을 인정받은 에페리손의 첫 복합제일 뿐만 아니라 아세클로페낙 성분에서도 등장한 첫 복합제다.
유비스트 통계에 따르면 에페리손 성분 제제의 2021년 원외처방액은 630억원이었으며 2018년 497억원과 비교해 꾸준히 증가하고 있다.
명문제약 '에페신 SR정'이 2021년 기준 연매출 37억원을 기록해 가장 많이 팔리고 있으며 대원제약 '네렉손 서방정' 33억원, 제일약품 '에페리날 서방정' 29억원으로 뒤를 이었다.
아세클로페낙 성분 제제의 경우 2021년 원외처방액 860억원으로 집계됐다. 대웅제약 '에어탈 정 100mg'이 연매출 83억원으로 다음제품인 '아클펜 정 100mg'과 두 배 이상 차이를 내고 있다.
에페리손과 아세클로페낙 시장을 더하면 약 1500억원 대의 규모다. 이같은 시장에서 두 성분의 복합제가 얼마나 선방할지 주목된다.
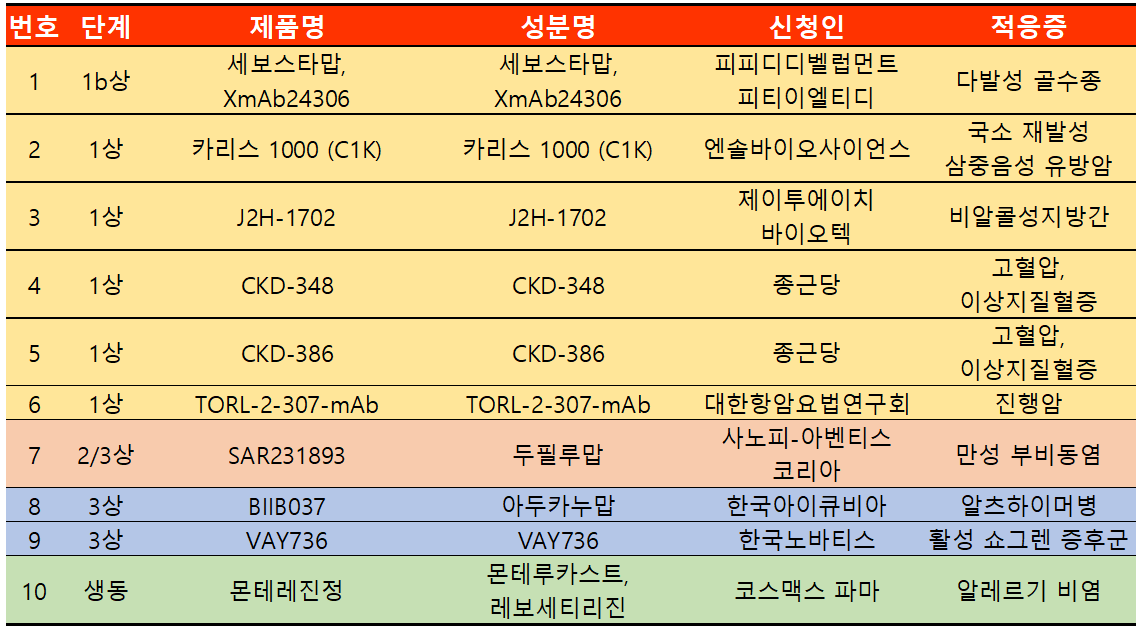
지난주 임상시험계획은 총 10건이 승인됐다. 임상1상 6건, 2상 1건, 3상 2건, 생동 1건 등이다.
알츠하이머병 치료제로 전 세계를 기대하게 했던 바이오젠의 아듀헬름(성분 아두카누맙)이 여러 악제로 국내 출시를 포기했지만 이와 별개로 임상 3b상을 국내 승인받았다.
이번 승인은 알츠하이머병이 있는 참여자에서 아두카누맙(BIIB037)의 임상적 이익을 확인하기 위한 제3b/4상 무작위배정, 이중 눈가림, 위약대조, 평행군 시험으로 다국가로 진행되며 전체 시험대상자 수는 1512명, 국내환자는 11명이 참여할 예정이다.
아두카누맙은 중앙약사심의위원회를 통해서도 부정적인 평가를 받은 바 있다. A 위원은 "1차 평가 변수를 성공하지 못했는데 허가를 논의하는 것 자체가 타당하지 않다"며 강력히 발언했다.
전반적인 의견으로 현재 공개된 임상시험으로는 확증적 임상결과로 동의할 수 없다는 것과 임상은 실패했지만 바이오마커에 대한 의의는 있다는 것으로 뭉쳤다.
한편, 아두카누맙과 경쟁하는 성분으로는 릴리의 '도나네맙', 바이오젠·에자이의 '레카네맙', 로슈의 '간테네루맙' 등이 있다.

