식약처, 실태조사 투명성·신뢰성 확보 목적
내년 1월 1일 이후 수행된 실태조사 결과부터 공개 계획

의약품 제조품질관리(GMP) 실태조사 결과가 대중에 공개된데 이어 '의약품 임상시험 실태조사' 결과 공개도 추진된다.
내년 1월 1일 이후 수행된 실태조사 결과부터 공개한다는 계획이다.
5일 관련업계에 따르면 식품의약품안전처는 투명성과 신뢰성을 확보하고, 국민 알권리를 보장하기 위해 임상시험 실태조사 결과 대국민 공개를 추진하고 있다.
식약처는 2020년 국내외 제약사, 시험책임자 등과 임상시험 관련 협의체를 구성해 실태조사 결과 공개관련 회의를 했었다.
이번에 마련된 추진안을 살펴보면, 공개 대상은 품목허가 단계에서 수행되는 임상시험 실태조사 결과를 우선 공개하고, 그외 실태조사 결과는 단계적으로 확대할 방침이다.
조사대상기관(시험책임자 포함), 임상시험 제목, 조사기간 및 조사관, 조사결과와 지적사항 요약 등이 공개내용이다.
조사대상자에게 통지한 날로부터 180일 이내 공개한다.
임상시험 실태조사 결과 공개(안) 작성하면 조사대상기관에게 의견조회(조회기간 30일)를 진행하고, 의견조회 결과 검토 및 공개안을 확정해 의약품안전나라에 공개하는 방식이다.
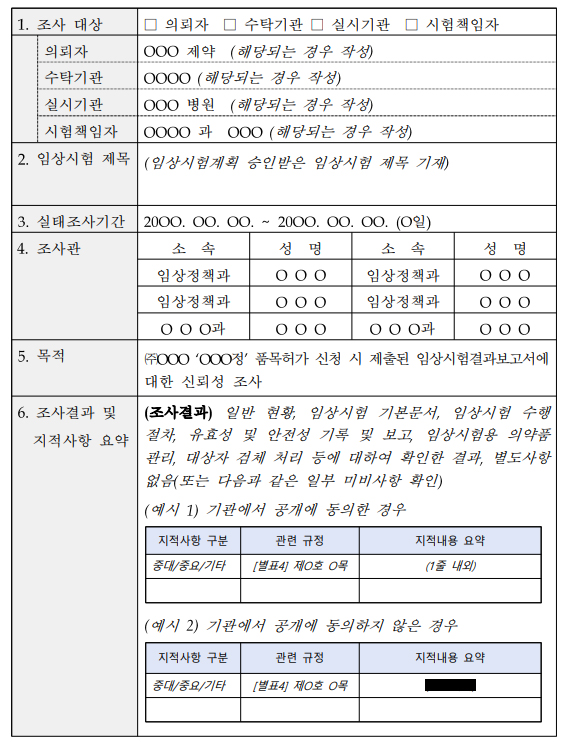
실태조사대상 기관이 경영 또는 영업비밀에 해당하는 부분에 대해 비공개 요청하면, 이를 제외하고 공개한다는 방침이다.
한편 식약처는 GMP 실태조사 투명성을 제고하고, 제약업체들의 GMP 수준 향상을 위해 지난 5월부터 GMP 실태조사 결과 정보를 공개하고 있다.
관련기사
이현주 기자
hjlee@hitnews.co.kr
폭 넓은 취재력을 바탕으로 제약산업과 건강보험정책 사이 퍼즐찾기에 주력하고 있습니다.

