시중 유통가능한 아시클로버 성분 완제약 시험결과 9월 22일까지 제출
품목취하 경우 등도 해당없음으로 보고해야

대상포진 치료에 사용되는 항바이러스제 '아시클로버' 성분 완제약에서 니트로사민류 불순물(NDMA)이 검출됐다는 해외 정보에, 식약당국이 안전조치에 나섰다.
관련업계에 따르면 식품의약품안전처는 제약사들에 아시클로버 성분 함유 완제약에 대한 자료제출을 오는 9월까지 제출하라고 지시했다.
식약처는 "최근 해외에서 아시클로버 성분 정제 완제약에서 NDMA가 초과 검출됐다는 안정성 정보에 따라 사전 예방조치를 취하는 것"이라며 "제조(수입)하는 아시클로버 성분 완제약에 대한 자료를 요청한다"고 설명했다.
이에 제약사들은 시중 유통 가능한 아시클로버 성분 완제약 중 대표성 있는 제조번호(매년 사용기한 임박한 3개 제조단위 이상, 매년 3개 이하로 생산한 경우 전 제조번호 등)에 대한 시험결과를 9월 22일까지 제출해야 한다.
또한 제출기한 전이라도 시험검사 완료 시 그 결과를 즉시 제출해야 하고, NDMA 불순물이 검출되는 경우 식약처에 보고해야 한다.
품목 취하 또는 시중유통가능한 제품이 없어서 제출할 자료가 없는 경우 사유서와 증빙자료를 함께 '해당없음'으로 제출하면 된다.
시험검사는 국내 의약품(GMP) 제조업자, 수입자의 실험실, 식약처 지정 품질검사기관, 한국의약품수출입협회 등에서 가능하고, 해외제조원의 시험결과(시험성적서) 인정된다.
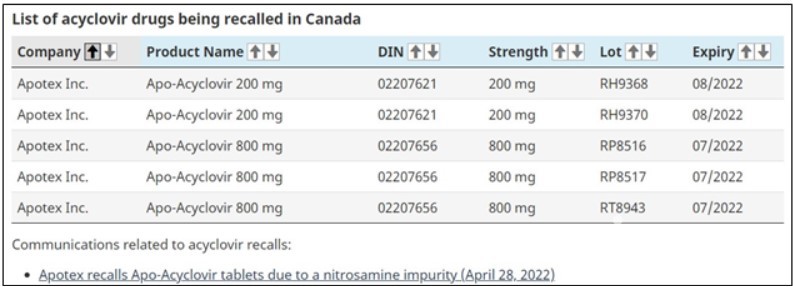
한편, 지난 4월 28일 캐나다보건부(Health Canada)는 'Apotex' 사의 아시클로버 성분 정제(제품명 Apo-Acyclovir)에서 허용 수준을 초과하는 NDMA가 검출됨에 따라 회사에 해당 로트 회수를 명령한 바 있다.
문제가 된 정제는 200mg(유효기간 2022년 8월, 2개 로트), 800mg(유효기간 2022년 7월, 3개 로트) 용량 제제로, 총 5개 로트가 회수됐다.

