전문의약품 152개 허가 품목 중 94%가 제2형당뇨 치료제
녹십자, 중증형 헌터증후군 치료제 '헌터라제ICV 국내 임상 개시

품목허가
전문의약품 152개 허가 품목 중 94%가 제2형당뇨 치료제?


지난 주(4월 4일~4월 8일)에는 DPP-4 억제제와 SGLT-2 억제제 등과 메트포르민 복합체가 무더기로 식품의약품안전처(처장 김강립)로부터 품목허가를 받았다.
전체 품목허가 수는 총 158건이며, 이 중 전문의약품은 152건, 일반의약품은 6건이었다. 이번 허가 전문의약품들은 143건에 달하는 94%가 제2형당뇨병을 적응증으로 하는 치료제로 확인됐다.
세부적으로 살펴보면, 디에이치피코리아의 DPP-4 억제제 다파플로글로진 단일제 '다파플로정'을 제외하고는, 메트포르민과 DPP-4 억제제 또는 SGLT-2 억제제간 복합제였다.
메트포르민과 DPP-4 억제제 복합제로는, 테네리글립틴 또는 시타글립틴이 포함된 2가지 경우로 나뉘었다.
메트포르민과 테네리글립틴 복합제는 △한국휴텍스제약 '다낼리아엠서방정' △이연제약 '디포테리엠서방정' △유영제약 '유테네엠서방정' △한림제약 '제넬리아엠서방정' △영일제약 '테글리엠서방정' △진양제약 '테네그린듀오서방정' △한국파비스제약 '테네글리틴엠서방정' △에이치엘비제약 '테네립틴엠서방정' △아주약품 '테네스엠서방정' △대원제약 '테네틴엠서방정' △국제약품 '테넬디엠서방정' △다림바이오텍 '테넬라엠서방정' △메디카코리아 '테넬엠서방정' △대한뉴팜 '테넬포민서방정' △동화약품 '테디엠메트서방정' △팜젠사이언스 '테라립틴듀오서방정' △삼천당제약 '텔리아엠서방정' △바이넥스 '티네글립엠서방정' △한국프라임제약 '테네론엠서방정' △넥스팜코리아 '테네린엠서방정' △동광제약 '테디포엠서방정' 등 21개 제품, 63개 품목(용량별)이다.
메트포르민과 시타글립틴 복합제는 서흥의 '자누렌듀오정' 뿐이었다.
메트포르민과 SGLT-2 억제제 복합제는 엠파글리플로진이 주성분인 경우만 존재했다. 허가품목은 △국제약품 '글리앙듀오정' △한국휴텍스제약 '다이디앙듀오정' △신풍제약 '신풍엠파글리플로진플러스정' △대한뉴팜 '엔피앙듀오정' △메디카코리아 '엠파글엠정' △구주제약 '엠파디듀오정' △테라젠이텍스 '엠파디앙듀오정' △아주약품 '엠파릴듀오정' △삼성제약 '엠파메타정' △대원제약 '엠파메트정' △동구바이오제약 '엠파앙듀오정' △진양제약 '엠파진듀오정' △삼천당제약 '엠포가듀오정' △삼익제약 '엠포리듀오정' △동광제약 '엠플로엠정' △팜젠사이언스 '엠플로진듀오정' △명문제약 '엠피앙듀오정' △위더스제약 '위디앙듀오정' △일양약품 '이디앙듀오정' △영풍제약 '자디메트정' △하나제약 '자디스듀오정' △제이더블유신약 '자디엠듀오정' △대웅바이오 '자디엠파듀오정' △대화제약 '자디엠프듀오정' △안국약품 '파리엠듀오정' △대우제약 '자디플로엠정' 등 25개 제품, 75개 품목(용량별)이다.
'DPP-4 억제제'는 혈당 강하 호르몬 인슐린 분비를 촉진하는 'GLP-1'을 분해시키는 'DPP-4'의 작용을 억제해, 제2당뇨병 환자의 혈당을 감소킨다. 'SGLT-2 억제제'는 DPP-4 억제제와 다르게 비인슐린의존성 당뇨병 치료제다. 따라서, 인슐린 저항성에 영향을 받지 않으며, 신장의 포도당 재흡수를 저해해 포도당 배출을 촉진시켜 혈당을 강하시킨다.
테네글립틴 성분은 한독이 DPP-4 억제제 계열 당뇨병 치료제 ‘테넬리아’를 오리지날 품목을 보유하고 있다. 테네글립틴 성분이 올해 10월 25일 물질 특허 종료를 앞두고 있어, 후발 의약품들이 대거 허가 절차를 발은 것으로 파악된다.
엠파글리플로진 성분은 한국베링거인겔하임과 한국릴리가 공동판매하고 있는 '자디앙'이 오리지널 품목이다. 지난해만 엠파글리플로진 단일제 자디앙의 제네릭이 100개 이상의 품목이 허가를 받았을 정도로 업계의 관심이 집중됐었다.
다만, 이번 한주간 엠파글리플로진과 메트포르민 복합제가 75개 품목이 허가되면서, 양사의 '자디앙 듀오'까지 시장을 위협받게 됐다.
유비스트에 따르면, 한독 '테넬리아 엠'과 '테넬리아'는 지난해 국내 DPP-4억제제 시장 상위 8, 9위를 차지했으며, 한국베링거인겔하임과 한국릴리의 '자디앙', '자디앙 듀오'는 SGLT-2 억제제 시장 2위, 4위를 차지한 바 있다.
임상승인
녹십자, 중증형 헌터증후군 치료제 '헌터라제ICV 국내 임상 개시
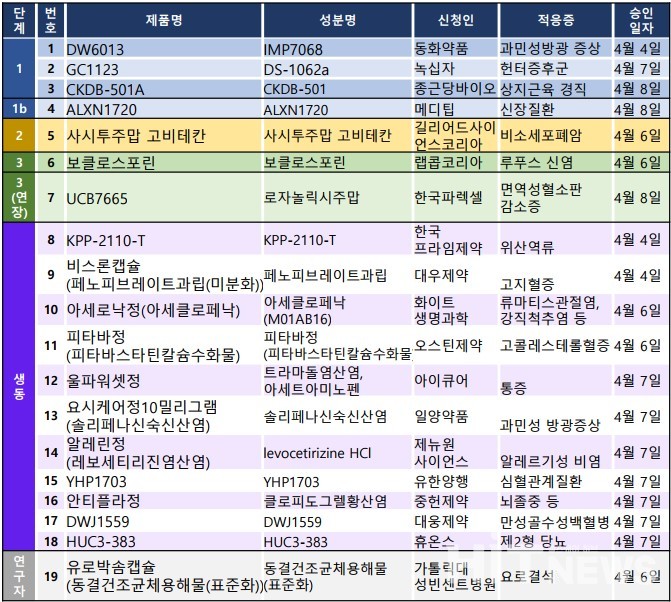
지난주 임상시험계획은 총 19건이 승인완료됐다. 세부적으로 임상 1상 3건, 1b상 1건, 2상 1건, 3상 2건(연장 1건 포함), 생물학적동등성 11건, 연구자임상 1건 등으로 확인됐다.
해당 임상시험은 과민성방광 증상, 헌터증후군, 비소세포폐암 등 다양한 적응증에 대해 승인됐다.
GC녹십자는 지난 7일, 지난해 1월 일본에서 세계 처음으로 품목허가를 획득한 바 있는 중증형 헌터증후군 치료제 '헌터라제ICV'의 임상1상계획을 식약처로부터 승인받았다.
회사 측이 제공한 의약품 설명에 따르면 '헌터라제ICV'는 머리에 디바이스를 삽입해 약물을 뇌실에 직접 투여하는 치료법으로, 기존 정맥주사 제형의 약품이 뇌혈관장벽(BBB, Blood Brain Barrier)을 통과하지 못해 '뇌실질 조직(cerebral parenchyma)'에 도달하지 못하는 점을 개선한 것이다.
회사는 일본에서 진행한 임상시험에서 "'헌터라제ICV'는 중추신경손상을 일으키는 핵심 물질인 '헤파란황산(HS, heparan sulfate)'을 크게 감소시키고, 발달 연령 유지 혹은 개선 효과를 확인했다"고 발표한 바 있다.
임상시험은 삼성서울병원, 서울대학교병원, 양산부산대학교병원 등 3개 의료기관으로 중증형 헌터증후군 환자 12명을 대상으로 진행될 예정이다.

