지현배 박사의 샌디에이고 통신 [7]
중국 바이오제약은 빠르게 진화하는 규제 환경과 성숙하는 혁신 생태계를 통해 상당한 가치 창출에 박차를 가함에 따라 세계 무대에서 두각을 나타내고 있다. 중국의 바이오제약 생태계는 이전의 제네릭 중심에서 혁신을 육성하는 방향으로 중대한 전환을 경험하고 있으며, 의료와 산업계에 상당한 영향을 미치고 있다. 이번 기사에서는 중국의 활기찬 혁신 생태계의 흐름과 바이오제약 산업을 이끄는 주요 트렌드를 살펴보고, 다국적 제약 회사가 세계에서 두 번째로 큰 의료 시장에서 혁신 기회를 활용하는 전략들을 기술하고자 한다.
물이 깊으면 고기가 모여들고 숲이 깊으면 새가 모여든다
(有闺女不愁没有婆家)
중국 바이오제약의 혁신은 글로벌 자본 시장에서 상당한 가치를 창출함으로 빠르게 주목을 받고 있다. Nasdaq, 홍콩 증권 거래소(HKEX), 상하이 증권 거래소 STAR(Scientific and Technology Innovation Board)에 걸쳐 상장된 중국 바이오 제약 혁신 기업의 시장 가치는 2016년 30억 달러에서 2021년 7월 3,800억 달러 이상으로 급증했다. 중국에서 시작된 바이오텍 회사는 그 총계에서 1,800억 달러에 이르고 있다 (그림 1).
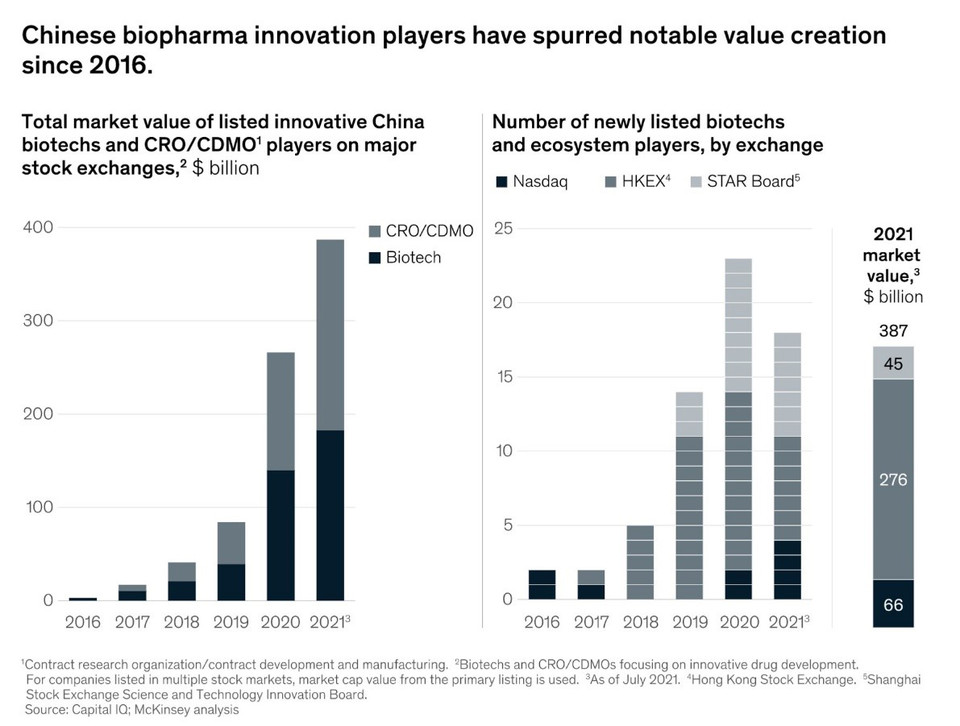
2020년 한해만 23개의 IPO 를 통해 볼 수 있듯이 중국 기업 공개는 가속화되고 있다. 실제로 중국 바이오텍 회사들은 2018년부터 2020년까지 세계 10대 바이오 기업들의 IPO 중 7개를 중국에서 시작된 IPO 기금 마련을 통해 주도했다. 국내 시장과 그 외의 시장에서 미충족 요구 사항 (unmet needs)을 해결할 수 있는 잠재력을 지닌 신약 개발의 급속한 확산을 통해 중국은 2015년 4.1%에서 2020년 13.9% 로 글로벌 혁신 파이프라인의 점유율을 높일 수 있었다.
중국의 혁신 생태계: 빠르고 느린 진화
규제 개혁, 쑤저우 시와 같은 지역에서 바이오클러스터의 출현, 해외에서 돌아온 인재, 중국 자본 시장의 개방은 모두 글로벌 혁신 단계에서 중국 바이오제약이 부상할 수 있는 생태계를 형성하는데 중요한 요소로 평가된다. McKinsey 는 China Drug Innovation Index (CDII) 에서 업계 전문가들에게 정책 환경(규제 개혁과 시장 접근 정책 간 분할), 자금 지원, 연구 개발(R&D) 역량, 지역 혁신 성과, 글로벌 시장과의 통합 등 건강한 바이오제약 혁신을 유도하는 5가지 요소들을 측정했다. 참가자들은 0에서 10까지의 척도로 중국을 평가했고 10이 가장 높은 점수이며 미국은 8점으로 벤치마크 역할을 한다 (그림 2).
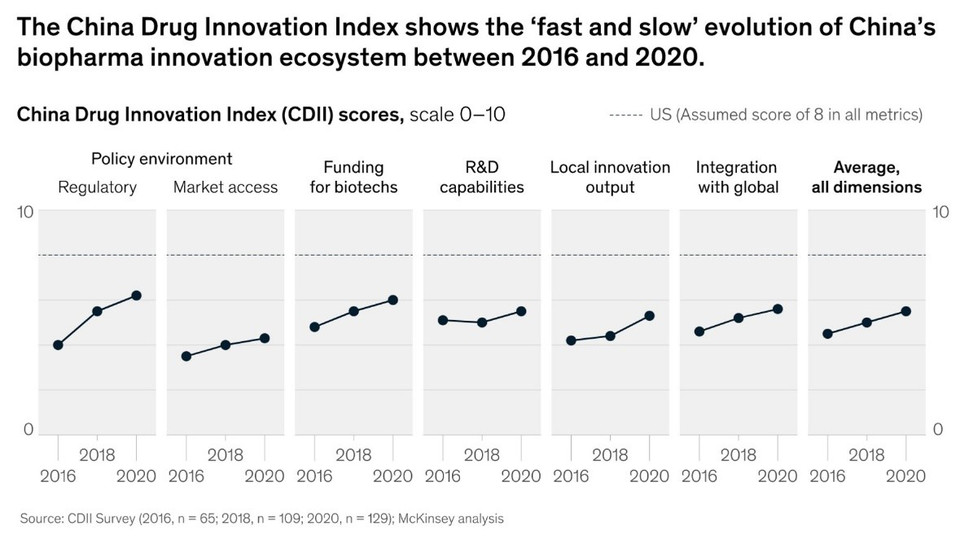
이러한 점수를 바탕으로 중국 바이오 산업의 발전을 다음과 같은 6 가지의 주요한 요소들로 정리했다.
신속한 규제 개혁으로 더 빠른 개발 및 승인 지원
규제 환경은 2016년 4.0점에서 2020년 6.2점으로 상승하면서 가장 큰 개선을 보였다. 개혁의 속도와 규모는 중국 역사상 유례가 없는 것으로 평가된다. 중국의 제약 규정을 국제 표준에 맞추는 것을 목표로 2015년 개편을 통해 2017년까지 인체용 제약에 대한 기술 요구 사항 조화를 위한 국제 위원회 (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use)에 쉽게 가입할 수 있었다. 이러한 단계를 통해 중국의 신약 개발 및 개발 생태계가 전 세계적인 수준으로 통합될 수 있었다.
한편, 약품평가센터(Center for Drug Evaluation, CDE)의 직원 수를 2015년 150명에서 2018년 700명 이상(600명 이상의 외부 위원회 위원으로 보충)으로 늘리는 등 신약 심사를 가속화하기 위한 조치는 2년 동안 20,000건의 신청이 가능한 것으로 알려져 있다. 또한 중국 제약 시장에 대한 인텔리전스 및 분석 제공업체인 GBI의 데이터에 따르면 CDE는 2016년부터 2020년까지 200개 이상의 New Drug Applications (NDA, 신약 신청)을 승인했다. 이와 동시에 중국의 NMPA(National Medical Products Administration)는 2016년 우선 심사 도입을 시작으로 신약 승인 절차를 간소화했다.
NMPA 데이터에 따르면 우선심사 대상 의약품의 비율은 2016년 14%에서 2019년 77%로 증가했다. 2018년 NMPA는 임상 시험 데이터를 기반으로 한 조건부 승인 (conditional approvals)을 추가했으며 2021년 중국 임상 종양 학회(Chinese Society of Clinical Oncology) 회의에서 발표된 CDE 데이터에 따르면 34건의 조건부 약물들을 승인했다. 2020년 7월, 의약품 등록 규정(Drug Registration Regulations)은 2021년 8월 현재 70개 이상의 의약품이 획기적인 치료법 (breakthrough therapies)의 새로운 방식으로 지정을 받았다. 이러한 개혁은 강력한 혁신 파이프라인을 활성화하는 데 도움이 되었다.
시장 접근은 여전히 느리다
설문 조사에서 시장 접근은 가장 낮은 4.3점을 받았으며 2016년에 비해 약간 개선된 것이다. 2017년 이후 매년 업데이트되는 NRDL(National Reimbursement Drug List)은 혁신적인 의약품에 대한 접근성을 확대하는 데 도움이 되었다. 그러나 설문 조사 참가자의 81%(129명 중 105명)에 따르면 NRDL 가격 책정 압력이 이런 등급에 영향을 미쳤다고 평가되었다.
혁신을 위한 자본에 대한 충분한 접근성
주요 지수에서 두 번째로 높은 것으로 2020년 6.0점은 중국 바이오제약의 자금 조달 환경에 대한 상당한 신뢰를 반영한다. 벤처 캐피탈과 사모 펀드를 통한 자금 조달 및 투자는 가장 접근 가능한 자금 출처로 남을 것으로 예상된다. 한편, 주식 시장, 특히 HKEX(Everest Medicine의 5억 2천만 달러 자금으로 시작) 와 상하이의 기술 중심 STAR 이사회는 2020 년23개의 중국 생명공학 IPO 중 21개 (나스닥 2개, HKEX 12개, STAR 9개)를 차지하는 매우 활발한 금융 채널로 부상했다.
혁신 가치의 역량을 향상시킨 생태계
수십 년에 걸친 약물 개발 전문 지식과 계약 연구 기관(contract research organizations, CRO) 및 계약 개발 및 제조 조직(contract development and manufacturing organizations, CDMO)의 급성장에 기여한 해외 귀국자들이 2020년 R&D 점수를 5.5로 높이는 데 도움이 되었다. CRO 및 CDMO 기반 시설의 확산은 생명 공학 혁신을 촉진하는 데 도움이 되었으며 중국은 일정 부문에서 선도적인 서비스 제공 업체 중 하나로 부상할 수 있었다. 예를 들어, WuXi AppTec과 Pharmaron은 현재 세계 최대의 전임상 화학 서비스 제공업체이다. 또한 생태계 성장을 지원하는 데 필요한 임상 개발 및 화학, 제조 및 제어(chemistry, manufacturing, and control, CMC) 기능의 개선도 이 분야에서 중요한 역할을 하고 있다. 그러나 CDII에 따르면 학계에서 산업으로의 기술 이전을 위한 학술 연구, 약물 발견 및 인프라는 여전히 격차가 있는 것으로 평가되었다.
지역 혁신이 중심
CDII는 지역 혁신 기업의 결과물이 중국 바이오제약의 가장 개선된 분야로 2016년 4.2에서 2020년 5.3점으로 상승했다고 보고 했다. 이는 2016년부터 매년 평균 32%씩 증가한 임상 시험 지원을 근거로 할 때 강력한 성장을 반영하고 있다. 한편, 현지 바이오텍 기업들은 중국에서 개발 중인 혁신 약물들의 점유율을 점진적으로 높여 2020년 전체의 50% 이상을 차지하게 되었다 (그림 3).
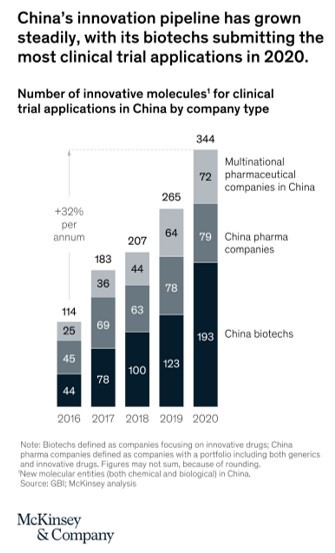
현지 혁신 기업의 NDA도 2017년 중국 전체 2%에서 2021년에는 53% 로 증가했다(7월 말 기준 43개의 NDA 중 23개). 이러한 새로운 자산들은 시간이 지남에 따라 향상되어 방향성 없이 빠르게 쫓아가는 방식과는 다른 차별화된 접근 방식으로 발전되고 있다.
국제 시장 통합을 뒷받침하는 국경 간 거래
중국의 혁신은 2016년에 비해 확고하게 개선된 5.5의 글로벌 통합 등급으로 상승하여 세계 시장에 깊은 인상을 남기고 있다. 지난 12개월 동안 중국 바이오텍은 다국적 제약 회사(multinational pharmaceutical companies, MNC)와 혁신 의약품에 대한 12건의 주요 라이선스 아웃 계약을 체결했으며, 거래 가치의 중앙값은 9억 달러 이상을 기록하고 있다 (그림 4).
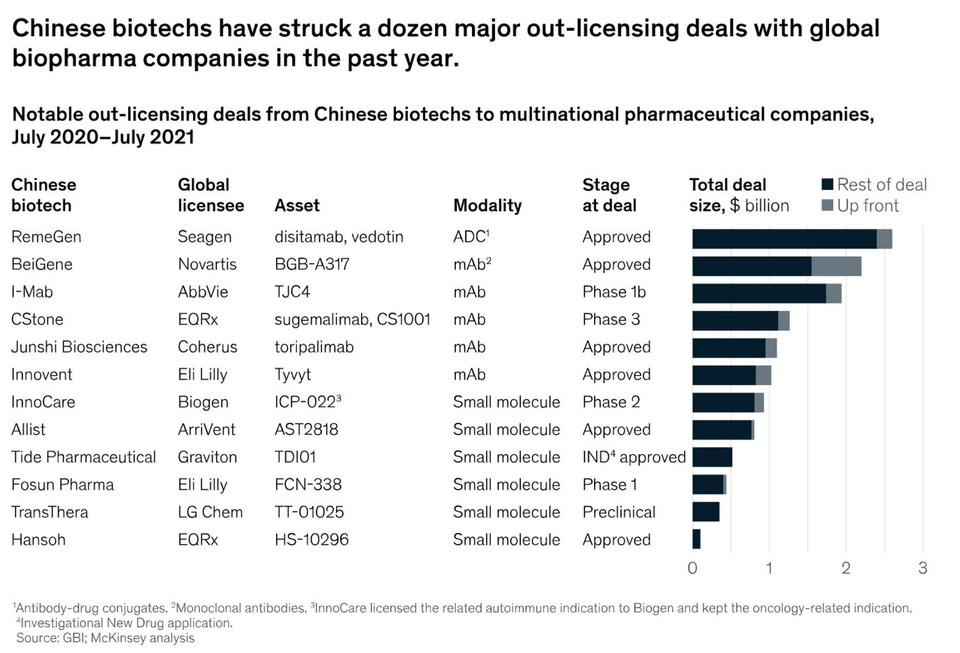
거래는 특히 잘 정립된 PD-1 자산을 중심으로 암 면역 치료에서 강점을 보여주고 있다. 또한 지역 생명 공학이 얼마나 발전하고 있는 지를 주목할 필요성이 있다. 즉, I-Mab Biopharma의 백혈병과 같은 혈액암에 대한 항-CD47 단일클론항체(mAb)는 현재 임상 3 상 진행중인 길리어드 사이언스의 선두주자에 이어 임상 2상이 진행 중이다. 이와 동시에 GBI 데이터를 기반으로 볼 때 중국 바이오제약은 2020년에 60개 이상의 in-licensing partnerships을 체결하면서 세계 시장에서 혁신을 계속해서 주도하고 있다. 또한 주식 투자를 포함한 전략적 파트너십, 혁신을 촉진하기 위한 다국적 기업과 중국 기반 벤처 캐피털 펀드 간의 제휴를 포함한 보다 창의적인 거래 구조가 형성되고 있다.
주목해야 할 중국 혁신의 세 가지 트렌드
중국의 바이오제약 생태계는 전반에 걸쳐 올바른 방향으로 발전하고 있으며 혁신을 촉진하는 데 필요한 대부분의 영역에서 점진적인 개선을 보여주고 있다. 이러한 개선은 중국의 바이오 제약 산업을 3가지 주요 트렌드로 특징지을 수 있는 새로운 단계로 나아가고 있다. 그 특징들은 더 빠른 약물 개발, 더 깊은 차별화, 글로벌 혁신 환경에 영향을 미치려는 야심으로 요약할 수 있다. 다음에서 이러한 추세가 중국 및 그 밖의 지역에서 바이오의약품 혁신의 미래에 의미하는 바를 제시하고 있다.
중국 바이오 기업들은 계속적인 신약물 개발을 가속화하고 있다
중국에 기반을 둔 바이오제약은 해외에서 개척된 임상적으로 검증된 표적에 초점을 두고 위험 요소를 감수하며 신약 포트폴리오를 중점적으로 개발하는 패스트 팔로어 전략을 추구해 왔다. 최근에는 많은 플레이어들이 초기 단계의 비임상적으로 검증된 약물들에 대한 MoA 연구로 전환하면서 동일한 작용 메커니즘(MoA)을 목표로 하는 글로벌 리더들과 경쟁을 하며 개발에 걸리는 시간을 단축하고 있다. 2003년 AstraZeneca의 표피 성장 인자 수용체 억제제 Iressa가 2003년 FIC(First-in-class) 출시부터 중국에 Betta Pharmaceuticals의 Conmana가 출시되기까지 8년이 걸렸지만, 2014년 Merck의 PD-1 항암제인 Keytruda 및 Top Alliance(Shanghai Junshi Biosciences 로도 알려짐)에서 Tuoyi의 중국 시장 출시는 단 4년의 시간이 걸렸다.
현재 중국 플레이어가 글로벌 FIC 자산의 격차를 계속 좁힐 것으로 예상되고 있다. 예를 들어, BeiGene의 TIM-3 면역 관문 수용체를 표적으로 하는 약물은 임상 2상 시험 중이며, FIC 경쟁사는 3상 중이다. Abbisko Therapeutics의 FGFR4 표적 약물은 임상 1상 시험 중이며, Blueprint Medicines의 FIC 경쟁업체(Cstone Pharmaceuticals가 라이선스)는 FGFR4 가 유도하는 국소 진행성 또는 전이성 간세포 암종(HCC)을 표적으로 하는 임상 2상 시험을 수행하고 있다.
중국 바이오텍들은 차별화된 치료제 개발과 플랫폼으로 나아가고 있다
혁신과 차별화에 대한 중국 바이오텍사들의 투자가 결실을 맺고 있다. 예를 들어 Junshi Biosciences는 FIC 가능성이 있는 anti-BTLA mAb를 개발하고 있는 반면 I-Mab의 anti-CD47 mAb는 적혈구와의 결합을 낮추는 높은 안전성 프로필로 인해 동급 약물들 중 최고의 잠재력을 가지고 있다.
중국 플레이어들도 플랫폼 기술을 구축하고 새로운 방식에 투자하고 있다. 특히 Akeso Biopharma와 EpimAb Biotherapeutics는 독점 이중특이성 기술 플랫폼을 구축하고 있다. 예를 들어, 최신 보도 자료에 따르면 Gracell Biotechnologies의 FasTCAR은 긴 제조 시간, 차선의 제조 품질, 높은 치료 비용 및 열악한 T 세포 적합성을 포함하는 자가 치료의 문제를 해결하는 것을 목표로 하고 있다.
한편 RemeGen은 중국에서 조건부 위암 치료제로 출시해 요로상피암 치료제로 미국 식품의약국(FDA)로 부터 획기적인 치료제 지위를 획득한 리드 자산인 disitamab vedotin (RC48)을 기반으로 항체-약물 접합 플랫폼을 개발 중이다. RemeGen은 Seagen과 RC48에 대한 26억 달러 라이선스 및 공동 개발 계약을 체결했다(그림 5).

중국 혁신이 세계 시장에 진입하고 있다
중국 바이오 제약 회사는 글로벌화하고 혁신의 완전한 가치를 확보하기 위한 옵션을 모색하고 있다. 그 결과 해외 임상을 포함하는 더 많은 국제 파트너십을 기대할 수 있고, 중국에서 발견된 혁신적인 약물을 미국 및 유럽 시장에서 환자를 위해 개발 및 상업화하는 것을 목표로 하고 있다. 그 결과 중국의 바이오제약 혁신이 전 세계적으로 규제 승인을 얻고 있다. 지난 2년 동안 패스트 트랙(Fast Track, 미충족 의료 수요를 충족시키는 약물 경로)과 기존 치료법을 개선할 수 있는 획기적인 치료법을 포함하여 중국에서 시작된 치료제들에 대한 FDA 지정이 급증했다 (그림 6).
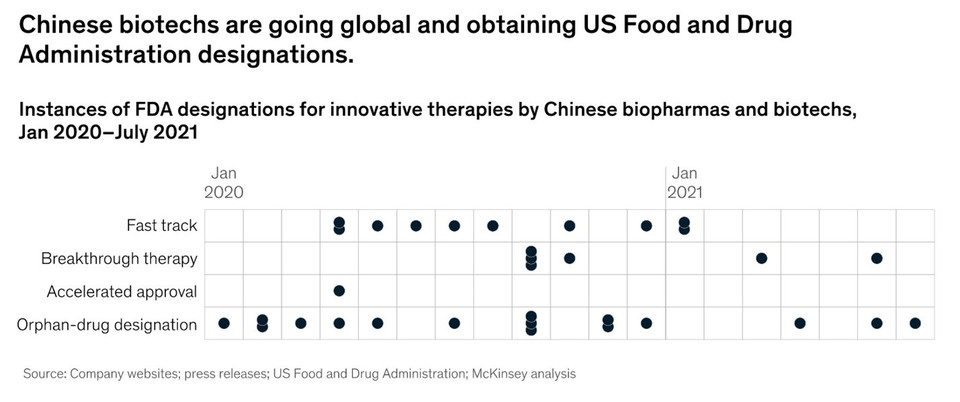
상업적 측면에서 중국 기업은 미국 및 유럽 시장을 위한 기존 개발 및 상업적 역량을 활용하기 위해 다국적 기업과 상당한 파트너십을 맺고 있다. 몇몇 중국 업체들도 중국 이외의 지역에서 상업적 입지를 구축하고 있다. 예를 들어 BeiGene은 본사를 베이징과 매사추세츠 주 케임브리지로 분할했다. HutchMed는 새로운 약물인 surufatinib에 대한 미국 NDA 절차를 시작하면서 중국, 유럽 및 미국 전역에서 R&D 및 상업적 진출을 확대하고 있다. 이러한 상업적 확장을 통해 이들 기업이 중국에서 시작된 혁신에서 더 많은 가치를 포착하고 미국과 중국에서 중요한 역할을 할 글로벌 바이오 제약 회사로 발전할지는 지켜볼 일이다.
다국적 기업의 참여를 유도하는 세 가지 전략을 통한 혁신
글로벌 바이오 제약 혁신 생태계에서 새로운 스타로 중국이 부상하는 것은 분명히 업계에 중요한 의미를 갖는다. 결과적으로 몇몇 다국적 기업은 중국의 혁신적인 자산 파이프라인을 활용하기 위해 움직이고 있으며 다음과 같은 세 가지 기본 모델을 중심으로 활동하고 있다.
현지 및 글로벌 시장을 위해 중국에서 자산 확보
AbbVie는 중국에서 자산을 적극적으로 확보해 왔다. I-Mab의 TJC4 라이선스 외에도 AbbVie는 Jacobio Pharmaceuticals과 제휴하여 잠재적인 1차 항암 단일요법인 SHP2 자산의 확보를 시도하고 있다. Johnson & Johnson과의 Legend Biotech의 CAR-T 세포 요법 거래와 다른 다국적 기업이 중국에서 조달한 PD-1 자산을 전 세계적으로 활용하기 위한 소수의 거래도 중국 바이오 기업들의 글로벌 진출을 보여주고 있다. 인바운드 활동과 관련하여 다국적 기업은 특허를 받지 않은 오리지널 의약품들에 대한 대량 구매가 가능하고 더 이상 상당한 가격의 프리미엄을 부과하지 않기 때문에 새로운 제품을 확보하려는 전략들을 적극적으로 활용하고 있다. 2020년 Bayer 가 이중 작용 글루코키나제 활성제 (glucokinase activator)인dorzagliatin의 라이선스를 취득한 것은 이러한 활동을 나타내는 것이며 Bayer의 항당뇨병 포트폴리오를 풍부하게 만들었다.
다방면에 걸친 전략적 파트너십
중국과의 전략적 파트너십은 현지 개발 및 상업화 기능에 대한 기회를 제공하고 있다. 또한 이러한 거래는 강력한 자본 시장을 활용할 수 있는 기회도 제공한다. 즉, 2021년 8월을 기준으로 Amgen는 BeiGene 지분 20.5%를 확보함으로 2019년 인수 가치는 약 15억 달러 증가했으며, 이는 약 27억 달러의 구매 초기 가치의 확보를 의미한다. 전략적 측면에서 이번 거래는 Amgen이 중국에서 종양학 포트폴리오를 개발하고 상업화하는 것을 지원하는 것이다. 또한 화이자는 Cstone에 2억 달러를 투자함으로 중국 본토에서 CStone의 후기 단계의 종양 자산인 sugemalimab에 접근할 수 있게 되었다.
중국 현지에서 혁신을 촉진시킨다
다국적 기업이 중국의 혁신을 포착하고 촉진하기 위해 다음과 같은 다양한 모델이 등장했다.
첫째, 지역 투자 펀드와의 제휴 또는 출시하는 방법이다. Sanofi는 2020년에 의료 기업가를 지원하기 위해 Cathay Innovation에 투자했다. 이는 AstraZeneca가 China International Capital Corporation과 함께 중국 의료 부문에 투자하기 위해 10억 달러 규모의 펀드를 출시한 이후에 실행되었다.
둘째, AstraZeneca가 중국의 의료 부문에 투자하기 위해 China International Capital Corporation과 함께 10억 달러 펀드를 출시한 후 의료 기업가를 지원하기 위한 혁신도 또 다른 좋은 예이다.
셋째, 초기 단계의 혁신을 촉진하기 위해 인큐베이터를 설립하는 것이다. 2021년에 출범한 스위스 최초의 글로벌 액셀러레이터인 로슈 액셀러레이터는 AI 및 디지털 솔루션을 포함한 제약, 진단 및 개인 맞춤형 의료 분야의 인재를 유치하는 것을 목표로 하고 있다. Johnson & Johnson의 JLABS 인큐베이터 네트워크 상하이 지점은 세계 최대 규모이며 중국과 아시아 태평양 지역 모두에 서비스를 제공하는 것을 목표로 하고 있다.
넷째, 중국 혁신가들에게 기술 플랫폼을 개방하고 있다. 2020년에 Innovent는 Roche의 범용 CAR-T 플랫폼과 특정 2:1 T 세포 이중특이성 항체의 발견 및 개발을 가능하게 하는 기술에 대한 액세스를 확보했다. Innovent가 제품을 개발, 제조 및 상업화하는 동안 Roche는 중국 외 개발 및 상업화를 위해 라이선스 옵션을 보유하게 되었다..
이러한 전략과 추세는 빠르게 성장하는 중국의 바이오제약 혁신 파이프라인을 초기 단계에 확보하려는 글로벌 기업들의 경향을 반영하고 있다. 중국 업체들이 계속해서 발전하고 글로벌 혁신 시장을 확대함에 따라 글로벌 진출의 기회는 더욱 넓어질 것으로 전망된다. 예를 들어 AI에 대한 중국의 투자는 의료를 위한 신약 개발 및 전달 모델을 통해 지역 및 국제 파트너 모두를 위한 기회를 확대하고 있다. 글로벌 야망, 상당한 자금 조달, 개혁의 규모와 속도, 인재 공급, 의료 기회가 중국에서 바이오 제약 혁신의 새로운 시대를 열었다.
그러나 생산적인 정책 환경을 육성하고 충분한 인재들의 확보를 포함하는 과제가 여전히 숙제로 남아 있다. 또한 산업 참가자는 역동적이고 초기 단계인 혁신 시장에 참여하는 위험을 효과적으로 대처해야 한다. 그러나 전반적으로 중국이 차별화된 혁신의 잠재적인 새로운 원천으로 부상한 것은 치열한 경쟁과 R&D 생산성에 대한 압박에 직면해 있는 글로벌 바이오 제약 산업에는 긍정적인 소식이다. 즉 중국 관련 혁신에 따르는 증가된 가치를 포착하고 그 기획을 확보하려는 전략은 점점 더 많은 글로벌 바이오제약 기업의 중요한 관심사가 되고 있다.
중국에는 “물이 깊으면 고기가 모여들고 숲이 깊으면 새가 모여든다 (有闺女不愁没有婆家)" 라는 속담이 있다. 이미 중국의 바이오 산업은 깊이 있는 물과 숲이 되어 가고 있다. 즉 급변하는 글로벌 바이오 산업에서 중국은 정책의 획기적인 변화와 과감한 투자가 맞물려 돌아가는 선순환 구조를 더욱 심화하여 글로벌 기업들을 모여들게 하고 있는 것이다.

