국내 환자 많은 정상안압 녹내장 환자 대상 2상, 통계적 유의성 달성
지난 5월 식약처로부터 3상 승인 받고 두 파트로 나눠 임상 준비 중
"방수구의 주요 배출구를 확장해서 안압을 낮추는 기전을 가진 약물은 아직 우리나라 환자에게 처방해 줄 약이 없는 상황입니다. 우리가 개발 중인 약이 3상을 마치고 승인을 받으면 국내 환자들도 ROCK 저해제 계열의 약물을 처방받을 수 있게 될 것입니다."
녹내장은 눈에서 받아들인 시각 정보를 뇌로 전달하는 데 중요한 역할을 하는 시신경에 병증이 생겨, 시야 결손 등 기능적 변화를 보이는 질환이다. 전 세계적으로 실명의 주요 원인이다. 이전에는 주로 안압 상승이 녹내장의 주 증상으로 꼽혔지만, 최근 정상 안압에서도 녹내장이 흔하게 발견된다. 특히 서양인과 달리 우리나라를 포함한 동양인은 60~70% 이상이 '정상안압' 녹내장을 앓고 있다.
피에이치파마(PH PHARMA)는 정상안압 녹내장 환자가 많은 국내 상황을 고려해 정상안압(치료전 안압 21mmHg 이하) 녹내장 환자 119명을 대상으로 녹내장 치료제 후보물질 소베수딜(Sovesudil) 개발을 위한 임상 2상을 진행했다. 이 임상은 △ Sovesudil 0.5% 투여군 △ Sovesudil 0.25% 투여군 △위약 군을 대상을 총 4주에 걸쳐 1일 3회 투여하는 방식으로 이뤄졌다.

임상 2상의 주요 평가 변수는 위약과 Sovesudil 투여 전과 비교해 4주 시점에서 평균 일 중 안압(diurnal IOP)의 변화를 본 것이다. 이와 함께 ROCK 저해제 계열의 주요 이상반응을 꼽히는 결막충혈 빈도도 살폈다.
연구 결과를 요약하자면 주요 평가 변수인 평균 일중 안압의 경우 Sovesudil 0.5% 투여군에서 베이스라인(Baseline) 15.38mmHg인 반면 4주 투여 시점에서는 13.88mmHg로 강하했다. Sovesudil 0.25% 투여군 역시 baseline 15.66mmHg에서 4주 투여 시점에서는 14.56mmHg로 통계적으로 유의미한 평균 일중 안압 강하 효과를 나타냈다.
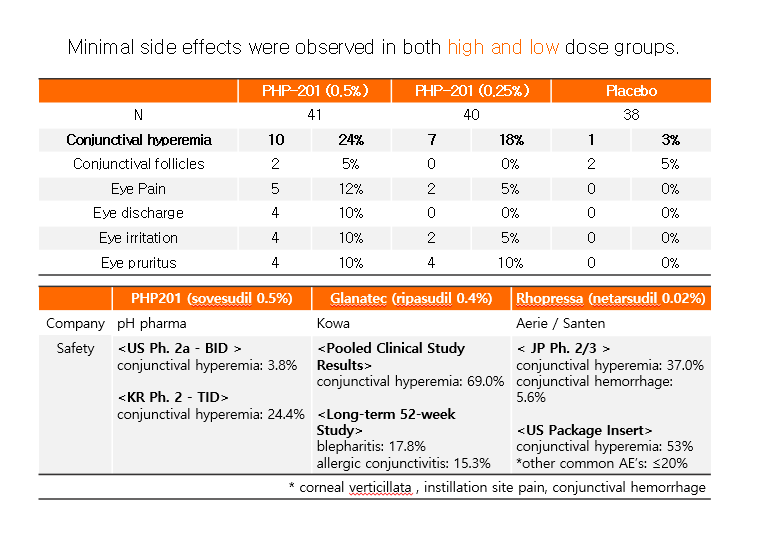
주요 이상 반응인 결막충혈(conjunctival hyperaemia) 역시 Sovesudil 0.5% 투여군 41명 중 10명(24.4%) 결막충혈을 겪었고, Sovesudil 0.25% 투여군 40명 중 7명만이 결막충혈을 겪었다.
피에이치파마는 이러한 2상 결과를 토대로 지난 5월 원발성 개방각 녹내장 환자를 대상으로 진행하는 임상시험 3상에 대해 식품의약품안전처로부터 임상계획승인(IND)을 받았다. 히트뉴스는 황윤영 피에이치파마 이사를 만나 녹내장 치료제 후보물질 소베수딜(Sovesudil)의 차별성과 임상 2상의 의미, 그리고 향후 3상 계획까지 들어봤다.
소베수딜(Sovesudil)은 녹내장 치료를 하는 ROCK 저해제 중 best in class라고 들었습니다.
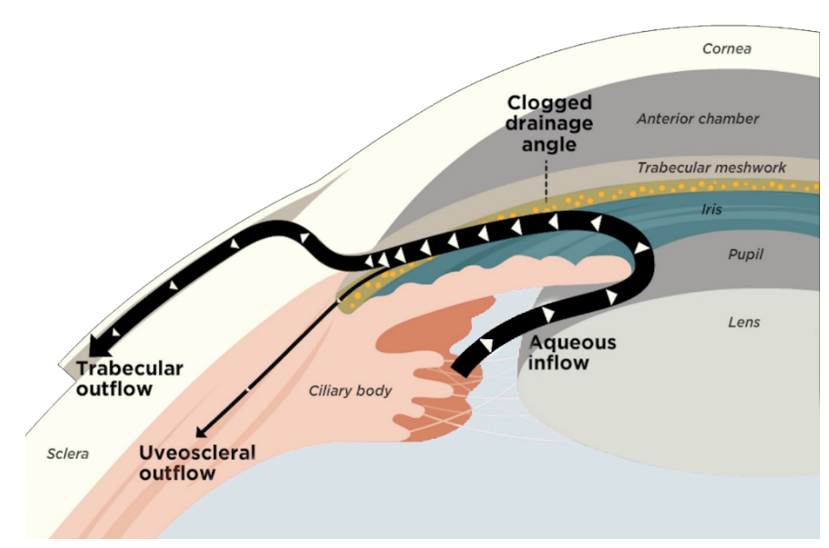
현재 녹내장 치료에 있어 1차 치료제로 처방되고 있는 프로스타글란딘(prostaglandin)은 안구의 포도막공막유출(uveoscleral outflow)을 원활하게 해 줘 안압을 낮추는 것입니다. 우리가 개발 중인 ROCK 저해제는 섬유주대(Trabecular meshwork)를 원활하게 빠져나갈 수 있도록 돕는 기전을 갖고 있는 것입니다.
프로스타글란딘과 ROCK 저해제를 함께 쓸 수 있다면 안압을 낮추고 녹내장을 치료하는 데 더 효과적일 것입니다. 현재 ROCK 저해제로 승인을 받은 약물은 미국 에어리 파마슈티컬스(Aerie Phamaceuticals)이 개발한 네타수딜(netarsudil)과 일본 코와제약이 개발한 리파수딜(Ripasudil)이 있습니다.
하지만 현재 한국에서는 두 약물이 모두 처방되지 못 하는 상황입니다. 리파수딜의 경우 한국에서 식약처로부터 승인은 받았지만, 시장에 출시되지 못 했습니다. 이런 상황에서 우리가 개발 중인 약물이 3상을 마치고, 승인을 받는다면 한국에서는 계열내 최초 약물이 될 것입니다.
정상안압 녹내장 환자를 대상으로 임상 2상을 진행한 이유는 무엇인가요?
현재까지 승인받은 녹내장 약물들은 모두 고안압 녹내장 환자를 대상으로 진행됐습니다. 서양인은 고안압 녹내장 비율이 높아 고안압 녹내장 환자를 대상으로 임상을 진행하는 것이 타당합니다.
그러나 일본을 비롯한 우리나라는 정상안압 범주의 녹내장 환자가 더 많습니다. 임상을 진행하기 위해 찾아간 교수님들이 말씀하는 바에 따르면 국내의 경우 최대 90%가 '정상안압' 녹내장 환자라고 합니다. 이런 국내 임상 상황에서 정상안압 녹내장 환자를 대상으로 2상 결과에서 통계적으로 유의미한 결과를 얻은 것은 매우 고무적이라고 생각합니다.
정상안압 녹내장 환자 119명을 대상으로 △위약 △저용량(0.25%) △고용량(0.5%) 투여군을 대상으로 4주 동안 하루에 세번 6시간 간격으로 sovesudil을 투여했습니다. 기존에 복용한 약이 빠져나갈 수 있는 wash out 기간을 거쳐 투여시점으로부터 4주 이후 평균값으로 안압 강하 효과를 살폈습니다.

Netarsudil과 Ripasudil 대비 Sovesudil만의 차별점은 무엇인가요?
ROCK 저해제는 기전 상으로 Trabecular meshwork 출구를 건드리기 때문에 결막충혈(conjunctival hyperaemia)이 주요 이상반응입니다. 이미 승인을 받은 ROCK 저해제는 눈에 투여가 되고, 다양한 효소(enzyme)에 의해 대사 과정을 거치면서 대사물질(metabolite)가 여전히 활성형(active)으로 남게 됩니다. Active metatbolite가 오랫동안 남아있어 결막충혈을 일으킬 것이라는 가설을 세웠습니다.
이런 가설 하에 우리는 sovesudil 물질을 디자인할 때부터 효소에 의해 분해되는 대사산물이 비활성형(inactive)이 되도록 했습니다. 이를 통해 결막충혈을 막고자 하는 목적이었고, 이는 우리가 개발 중인 신약후보물질의 차별점으로 내세웠습니다. 이러한 우리의 가설은 임상 2상까지는 충분히 입증됐습니다.

임상 2상 결과에서 각막충혈 효과가 적었나요?
물론 다른 약물과 직접비교임상(head to head)을 진행한 것은 아니기 때문에, 다른 약물 대비 우리의 각막충혈 효과가 더 적다라고 단정적으로 표현할 순 없습니다. 다만 다른 약물의 이상반응과 대비해 보며, 우리의 각막충혈 효과가 낮다는 경향성은 확인해 볼 수 있었습니다.
우리가 진행한 임상 2상 소베수딜 고용량군에서 각막충혈 빈도는 24.4%인 반면, 리파수딜 69%, 네타수딜 40% 정도가 생겼다는 보고가 있습니다. 처음부터 우리가 물질 디자인부터 고려했던 것처럼 각막충혈을 줄이면서 효과를 높이는 것을 입증해 나가고 있는 단계입니다.
지난 6월 sovesudil이 시신경보호에도 효과가 있을 수 있다는 동물실험 결과를 세계녹내장학회(World Glaucoma Congress)에서 발표했다고 들었습니다.
결국 녹내장의 궁극적 목표는 시신경 보호입니다. 안압이 떨어지면 시신경의 손상을 늦춘다는 결과가 속속 발표되면서, 현재 안압 강하만으로 약물들이 허가를 받고 있습니다. 하지만 안압이 낮아져도 시신경의 손상은 계속 진행될 수 있어, 녹내장의 증상은 계속 악화될 수 있습니다.
우리는 직접 안압을 낮추는 것고 동시에 시신경을 보호하는 데 우리가 개발 중인 약물이 특정한 역할을 할 수 있을지 입증해 보고 싶었습니다. 이런 가설 하에 시신경압착동물모델을 통해 sovesudil이 시신경을 보호하는 데 역할을 할 수 있는지 검증하는 실험을 진행했습니다.
시신경압착동물모델, 생소한 개념입니다.
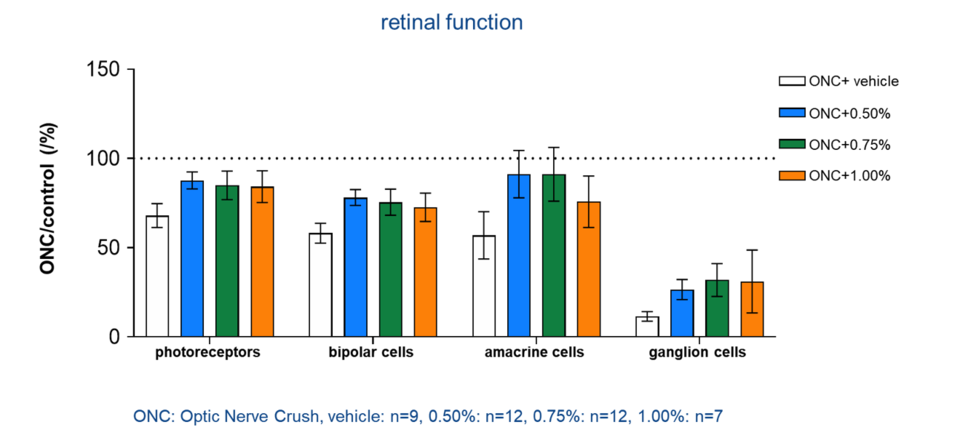
호주 맬버른 대학교와 공동연구를 한 것인데요, 쥐의 시신경 부위를 강제적으로 압력을 줘 시신경 세포를 망가뜨린 상태에서 약물을 주입한 실험입니다. 임상시험과 달리 동물실험은 sovesudil을 고용량(0.5%, 0.75%, 1%)으로 주입해 봤습니다. 용량 간의 통계적 차이는 없었지만, 위약대비 시신경 기능이 덜 망가지도록 보호한다는 실험 결과를 얻을 수 있었습니다.
기존 치료제 중 시신경을 보호하는 약물이 있나요?
실제 시신경을 보호한다는 적응증을 가진 약물은 없습니다. 다만 브리모니딘(brimonidine)이 시신경을 보호할 수 있다는 임상을 진행한다는 연구를 진행한 적은 있습니다. 이런 임상 결과를 바탕으로 약물의 차별성을 논하기도 하고요.
우리와 같은 계열의 약물 Netarsudil과 Ripasudil 역시 시신경 보호와 관려된 몇 가지 실험을 했습니다. 우리의 약물이 brimonidine과 같이 임상을 진행하려면 현재 진행한 실험 외에 몇 가지 실험을 더 진행해야 합니다. 현재 진행한 동물실험은 충분히 유의미하기 때문에, 후속 연구도 충분히 진행해 볼 만하다고 생각합니다.
국내에서 3상을 진행하고, 국내 시장에서 출시까지 생각하고 있는 것으로 알고 있습니다.
원발성 개방각 녹내장 환자를 대상으로 두 파트로 나눠 임상 3상을 진행할 계획입니다. 3A는 100명 내외, 3B는 200명 정도로 수행하면, ripasudil과 비슷한 규모의 임상입니다. 개발에 속도를 붙여 국내 환자들도 ROCK 저해제의 치료 혜택을 받을 수 있도록 할 것입니다.

