업계·정부, 디지털치료기기 임상·허가·수가 기준 마련 고심
정부와 업계가 국내 디지털치료기기(디지털치료제) 임상시험 기준 마련에 고심하고 있는 것으로 확인됐다.
업계에 따르면 임상시험 실시부터 실제 출시까지는 다소 시일이 걸릴 것으로 전망되나 개발부터 품목허가까지 한 싸이클이 원활하게 진행되는 것을 확인한다면 사업 확대 가능성은 충분하다는 의견이다.
업계에 따르면 현재 보건당국과 허가당국 및 업체들은 허가와 보험을 결정할 소위 '채점표' 만들기에 고심하고 있는 상황이다.
지난 4월 호흡질환 재활 프로그램 'Redpill 숨튼' 임상시험승인을 신청한 라이프시맨틱스 송승재 대표는 현재 정부 측과 품목허가·신의료기술평가에 필요한 디지털치료기기 안전성·성능 평가 기준 마련이 논의되고 있다고 밝혔다.
또한 해당 디지털치료기기는 허가·신의료기술 입증에 필요한 임상시험을 동시에 진행하는 범부처전주기의료기기연구개발사업단 트랙을 밟고 있어 승인 기준이 고도화 되고 있다고 덧붙였다.
송승재 대표는 "제품에 대한 치료기전은 물론 관련 임상시험 자료가 전무한 첫 단계인 만큼 기준을 마련하는 작업부터 진행하고 있다"며 "의료시장 출시 허들은 높아질 수 있으나 전체적인 과정이 간소화 되는 부분은 이를 상회하는 긍정적인 요소가 될 것"이라고 설명했다.
현재 임상시험 문턱에 닿은 레드필 숨튼은 폐암이나 만성폐쇄성폐질환자 재활 프로그램으로, 환자 호흡능력에 따른 맞춤형 운동프로그램과 일·월·주간 단위 리포트를 제공하는 형태의 디지털 치료기기다.
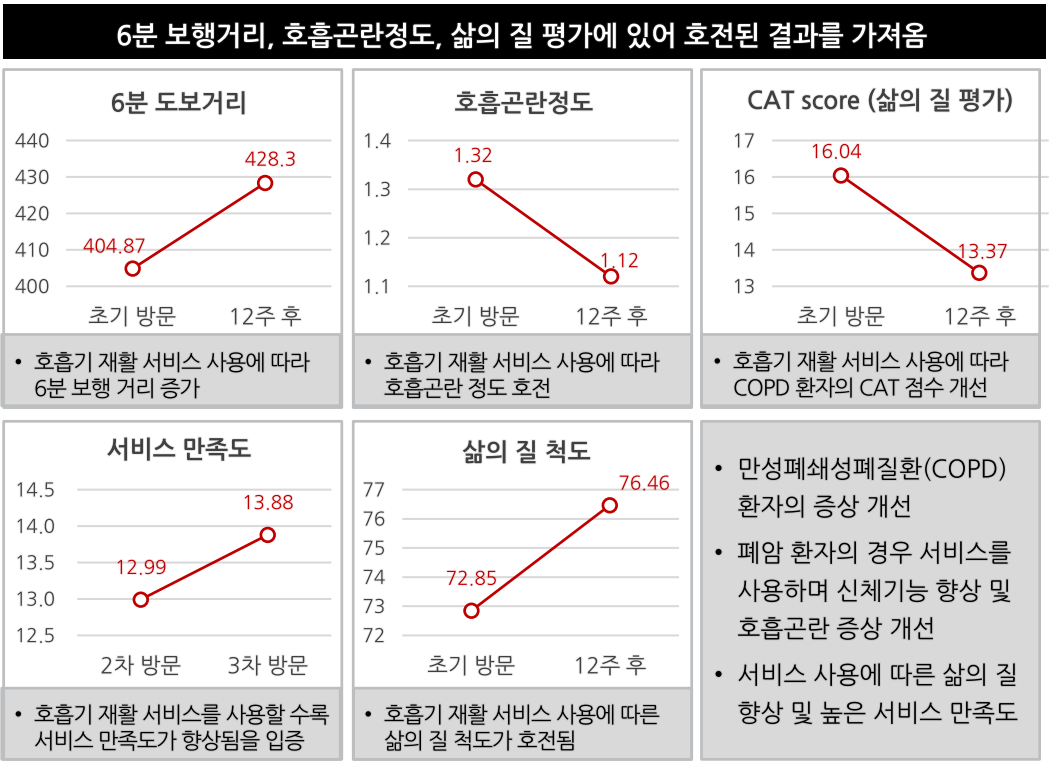
2021년 1분기 기업공개보고서에 따르면 2017년 4월부터 2017년 12월까지 서울아산병원, 서울보라배병원, 한양대구리병원, 원주세브란스기독병원, 경희대병원에서 호흡기질환 환자 243명(COPD 153명, 폐암 90명)을 대상으로 진행한 임상연구결과 6분 보행거리, 호흡곤란정도 등 삶의 질 평가에서 호전된 결과를 획득했다.
이밖에 디지털치료기기 임상시험 신청을 앞둔 다수의 디지털치료기기 개발사들은 임상시험 프로토콜 최종 점검 단계에 접어든 것으로 확인됐다.
알코올의존증 재활 디지털치료기기를 개발 중인 웰트는 현재 임상시험승인 신청을 위한 임상시험 프로토콜 개발 마무리 단계로 파악됐다.
강성지 대표는 "중독관련 디지털치료기기는 해외 개발·출시 사례가 있고 현장에서 사용되고 있는 만큼 임상시험 프로토콜 개발은 마무리 단계에 있다"며 "위약(僞藥)과 같은 형태의 대조군을 설정하는 등 효과를 입증할 여러 방안들이 논의되고 있다"라고 설명했다.
디지털치료기기 개발업체 에임메드(대표 신재원)는 최근 자체적인 임상시험 프로토콜 최종 점검을 마무리 하고 임상시험승인 신청을 완료했다.
에임메드 김수진 상무는 디지털 치료기기 특성상 발생하는 △임상시험 환자 모집 △연구수행 △평가결과 분석 등 기존 임상시험과 차별점을 반영한 ePRO(electronic Patient-reported outcome)시스템 적용에 주력했다고 밝혔다.
김 상무는 "디지털치료기기는 약물의 화학작용이 일어나지 않는다는 점과 치명적인 부작용을 야기하지 않는다는 강점이 있지만 임상시험 계획 수립에 있어서는 종전 임상환경과 차이가 분명해 연챡륙 시킬 프로토콜 개발이 필요했다"라고 설명했다.
TMI. (업계가 생각하는) 디지털 치료기기와 건강보험 간 고민
업계에 따르면 디지털 치료기기 급여에 관련해서는 기존 건강보험 시스템이 내포하고 있는 '사용자' 개념에 대한 고민이 있다.
기존 건강보험시스템 사용자가 의료진 중심이었다면 최근 개발되고 있는 모니터링·관리형 디지털치료기기나 전자약 등은 사용자가 환자 중심으로 옮겨가고 있기 때문이다.
업계는 건강보험 사용자 개념을 확장할 새로운 시스템 도입 혹은 최근 의료기기 개발 트렌드를 반영할 수 있는 별도 기준이 필요하다고 입을 모으고 있는 상황이다.

