
미국 연방정부가 사업에 대한 의견수렴과 세부내용 재검토를 이유로 FDA 승인을 받은 혁신 의료기기에 한해 4년간 수가를 지급하겠다는 MCIT 발효 연기를 결정했습니다.
관련기사 '혁신신의료기기면 수가 주겠다'는 미국 'MCIT' 제동
여기서 FDA의 혁신 의료기기 기준은 크게 보면 아래와 같습니다.
FDA의 혁신 의료기기(Breakthrough Divece) 기준
1. 획기적일 것
2. 승인된 치료적 대안이 없을 것
3. 기존 승인된 대안에 비해 상당한 이점을 제공할 것.
4. 가장 큰 이익은 환자에게 돌아갈 것.
미국 정부는 혁신적인 의료기술을 임상현장에 도입하고 효과를 확인할 기회를 제공하겠다는 결정을 내린 것입니다.
이는 안전성 유효성이 입증된 치료법에 가치를 매길 것인가, 가능성 있는 치료법에 투자해 유효성을 확인할 것인가 사이에서 하나를 선택했다는 점 만으로도 의미를 가집니다.
즉 '닭이 먼저냐, 달걀이 먼저냐'와 같은 고민에서 글로벌 규제에 큰 영향력을 행사하고 있는 미국이 내놓은 답이었다는 점에서 우리나라를 비롯한 많은 나라도 주목하고 있는 사업이었습니다.
3월 15일 발효 예정이었던 MCIT가 5월 15일로 유예됐다는 것은 사실입니다. 그렇지만 발효 계획에는 그것이 유예됐다는 사실보다 많은 의미가 담겨있습니다.
MCIT 시행을 결정할 수 있었던 이유
"치료제 개념 확장"
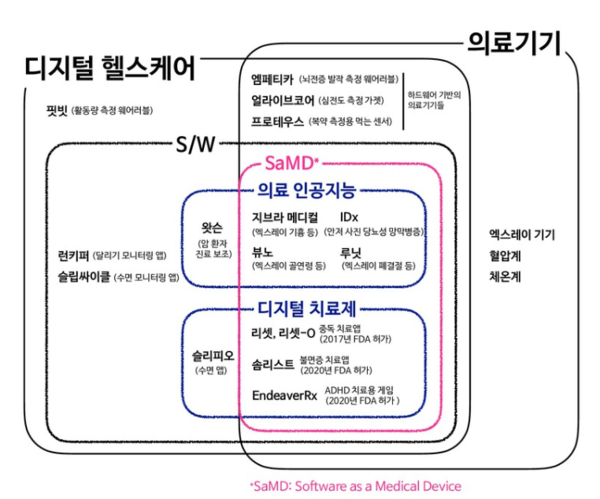
위 두 개 이미지는 각각 치료제의 변천사와 디지털 헬스케어 내 SaMD의 위치를 표현하고 있습니다. 디지털치료제(Software as Medical Device, SaMD) 관련 세션이나 세미나에 참석하신 경험이 있다면 몇 번이고 봤을 그림입니다.
눈이 번쩍 띄는 이미지였지만 최근 이 이미지들이 프레젠테이션 현장에 나타나면 '잠깐 다른 일을 해도 되겠구나' 싶을 정도로 익숙하게 다가오기도 합니다.
'Pear Therapeutics'의 약물중독 디지털 치료제 'reSET'이나 'Akili'의 ADHD 디지털치료제 'Endeavor'에 대한 이미지도 익숙합니다.


물론 이 익숙함은 새로운 기술들이 의료 현장에 깊숙이 자리하고 있다는 것은 아닙니다. 다만 새로운 치료제가 의미하는 바에 대한 공감대가 형성됐다는 의미입니다.
그러나 조금 달리 생각해보면 이 같은 공감대는 곧 치료제 개념이 '안전성과 유효성에 대한 임상적 근거를 확보할 수 있는 모든 것'으로 확장되고 있음을 의미합니다.
물론 MCIT가 추구하는 방향이 '게임형 치료제도 만들어 봅시다'는 아닐 것입니다.
'환자가 가장 안전하고 효과적으로 치료받을 수 있는 형식이 게임이라면 개발을 마다할 이유는 없습니다'가 보다 정확한 접근일 것입니다.
MCIT 시행을 결정해야 했던 이유
"개념이 바뀐다면 제도를 마련해야 한다"
형광 기술 기반으로 치과 진단을 보조하는 의료기기 개발업체 관계자를 만난 적 있습니다. 그는 오랜 기간 공을 들여 신의료기술평가 승인을 받았지만 새로운 수가코드 발급에 어려움을 겪고 있다는 말을 했습니다.
"결국에는 치과용 X-ray를 통해 의사 진단이 이뤄지는데 보조적 수단에 새로운 수가 코드를 발급하기는 어렵다고 합니다."
세계 어느 나라가 그렇듯 보험재정에는 한계가 있습니다. 몇 개의 보험체계를 어떤 방식으로 운영하고 있는가에 차이가 있을 뿐입니다.
재정의 한계가 있다는 전제 하에서 의료제품의 안전성·유효성 만큼이나 비용효과성은 재정 지출에 있어 중요한 지표가 됩니다.
그렇기 때문에 새로운 치료 가능성이 있는 혁신 의료기기임에도 수가 지급이 '닭과 달걀'의 문제가 될 수 있다는 것입니다.
MCIT 사업 내용은 파격적입니다.
우선 AI 등 혁신 의료제품의 선순환 구조는 아래와 같습니다.
제품 제공(사용)
↓
임상현장 데이터 확보
↓
제품 고도화
↓
고도화된 제품 제공(사용)
그렇지만 선순환 구조 첫번째 연결고리인 제품제공과 임상현장근거 확보 사이에서는 아래와 같은 이유로 선순환이 끊어집니다.
제품 제공(사용)
↓
사용할 근거를 찾지 못함
↓
임상현장 데이터를 확보하지 못함
↓
제품 고도화 실패 및 개발 지연
물론 사용할 근거를 찾지 못한다는 부분을 '설득'과 '부단한 노력'으로 극복하는 사례도 확인 가능합니다.
그렇지만 업계가 말하고자 하는 것은 선순환 구조를 설득보다 '시스템'으로 확보하자는 것이며, 그 시스템이 곧 '수가 진입'이라는 것입니다.
MCIT는 선순환 구조를 만들 재정을 파격적으로 지원하겠다는 미국 정부의 의지였기에 의미가 컸던 것이죠.
우리나라가 마중물 수가를 준비하는 이유
K-의료의 새 목표 : 글로벌 시장 선점
한국보건산업진흥원은 '보건산업정책연구 Perspective'를 통해 글로벌 시장 선점 가능성이 있는 AI 기반 진단보조 SW에 한시적인 수가 가산 시범사업을 시행할 필요가 있다고 밝혔습니다.
국내 의료시장의 구매요인을 충족해 실제 사용 데이터를 확보하고 이것이 글로벌 진출에 활용될 수 있다는 이유입니다.
글로벌 시장 진출과 선점을 안전성·유효성, 비용효과성에 상응하는 가치로 인정해야 한다는 것입니다.
업계 관계자들과 이야기를 나눠보면 '내수 시장 만으로는 (성장이)어렵다', '기술이 충분한 우리 기업이 제대로 성장하려면 해외로 나가야 한다'는 말을 종종 듣게 됩니다.
그렇지만 유망한 우리 기술이 외국 협상 테이블에 오르게 되면 가장 먼저 듣는 질문은 '자국 점유율은 어떤가'라는 것입니다.
최근 '디지털'이나 '스마트'라는 단어를 접하게 되면 종종 직전 세대를 관통했던 '웰빙(Well-being)'이라는 단어가 떠오릅니다.
디지털 뉴딜로 글로벌 시장을 선도하겠다는 선언이 흥행을 위해 우선 붙이고 보는 접두사가 아닌 행동으로 표출되려면 재정을 사이에 둔 고민에서 좀더 적극적인 선택지를 택할 필요가 있을 것입니다.

