미국 샌프란시스코에서 열린 IPF Summit 2018에서
NRDO (No Research Development Only) 모델의 바이오벤처 브릿지바이오(대표 이정규)는 8월 20일부터 미국 샌프란시스코에서 열린 IPF Summit 2018에서 특발성 폐섬유증 치료제 후보물질인 BBT-877의 전임상 효력시험 결과를 발표했다.
BBT-877은 2017년 레고켐 바이오사이언스로부터 도입한 오토택신 저해 신약 후보 물질로, 오토택신은 섬유증, 자가면역질환, 종양 등 다양한 질병에 관여하는 것으로 밝혀져 글로벌 제약·바이오 산업과 학계의 주목 받고 있는 신규 타깃이다. 최근 갈라파고스사의 오토택신 저해 신약 후보물질인 GLPG1690이 특발성 폐섬유증 환자를 대상으로 한 23명 규모의 소규모 2상 임상시험 (임상2a)에서의 우수한 효력을 FDA로부터 인정받아 추가 2상 임상시험 (임상2b)를 하지 않고 바로 임상 3상으로 가는 것을 승인받았다.
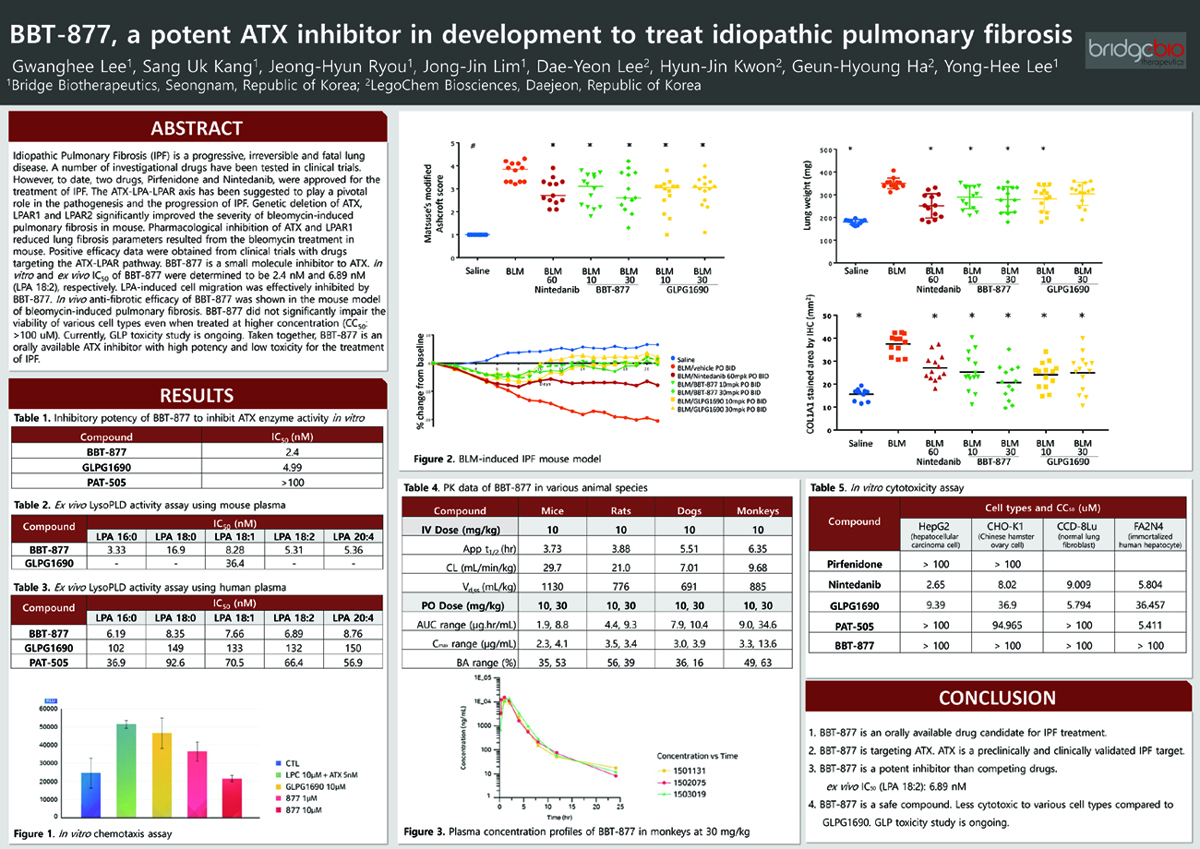
포스터 형식으로 진행된 이번 발표는 동물 모델에서의 BBT-877의 효력을 경쟁 약물들과 비교한 것을 중심으로 주요 전임상 시험 결과를 포함하고 있으며, 특히 블레오마이신 유도 폐질환 마우스 동물 모델에서 경쟁약물과 비교하여, 병리학적 지표 (애쉬크로프트 점수)와 바이오마커 (콜라겐 침착도)에서 우수한 결과를 보여 계열 내 최고 의약품 (Best-in-Class)의 가능성을 보여 줬다고 회사측은 밝혔다.
브릿지바이오는 2017년 5월, BBT-877에 대한 전세계 독점실시권 확보 이후 레고켐 바이오사이언스의 초기 연구 결과를 이어 받아 개발에 박차를 가하여, 금번 학회에서 주요 전임상 시험 결과를 발표하고 금년 말 미국 FDA에 임상 1상 IND를 신청할 계획이다.
브릿지바이오의 이정규 대표는 “레고켐 바이오사이언스로부터 도입한 BBT-877의 우수한 전임상 효력시험 결과를 공개할 수 있게 돼 기쁘다. NRDO로서의 강점을 바탕으로 정확하고 빠른 개발을 통해 올해 안에 갈라파고스사의 GLPG1690에 이어 두번째로 임상 시험을 진행하여 계열 내 최고 의약품으로 개발을 이어가겠다”고 밝혔다.
브릿지바이오는 성균관대학교와 한국화학연구원으로부터 전세계 독점실시권을 확보한 궤양성대장염 개발후보물질인 BBT-401의 미국 임상 1상을 진행 중에 있으며, 신규 면역 항암제 후보 물질인 BBT-931을 유한양행과 공동 개발 중에 있다.
<용어설명>
◆오토택신(Autotaxin)=900여 개의 아미노산으로 구성된 혈중 단백질로, 리소파티딜콜린 (LPC, lysophosphatidylcholine)을 가수분해하여, 리소포스파티드산 (LPA, lysophosphatidic acid)으로 전환하는 효소이다. 오토택신에 의해 생성된 인지질인 LPA는 수용체 (LPAR)에 결합해 세포증식, 세포사멸 방지, 세포이동, 사이토카인 및 케모카인 분비 등 다양한 신호전달과정에 관여하는 것으로 연구되어 있으며, 병리학적으로는 염증 및 섬유화 (Fibrosis)에 관여되어 있음이 밝혀지고 있어 최근 주목받고 있는 치료 타겟 물질이다.
◆특발성 폐섬유증(IPF, idiopathic pulmonary fibrosis)=특발성폐섬유증은 만성적으로 진행되는 폐섬유증의 하나로, 아직 정확한 원인이 밝혀지지 않고 있다. 폐의 아랫부분부터 섬유화로 인해 기능이 손상되는 질환으로 경과가 좋지 않고 증명된 치료 방법이 없는 희귀난치성질환으로 진단 2년 내에 50%의 환자가 사망하는 중증질환이다. 지금까지 단 2 종의 약물(오페브, 에스브리엣)만이 미국 FDA로부터 2014년 허가를 받고 출시되었다.

