연구자 주도 임상이 절반 이상
국가임상시험재단 “공익적 임상시험 정부와 협의할 것”
코로나19 백신과 치료제 개발이 활발하게 이뤄지고 있는 것으로 나타났다.
임상시험 레지스트리 미국국립보건원(NIH)의 클리니컬트라이얼닷고브(ClinicalTrials.gov)에 따르면, 코로나19 백신과 치료제 임상시험은 지난 3월 11일 기준 56건에서 466건으로 약 8.3배 증가했다. 특히 연구자 임상시험은 32건에서 314건으로 9.8배 증가해 공익적 목적의 연구자 임상시험이 임상연구 활발하게 일어나고 있는 것으로 보인다. 이 같은 내용은 국가임상시험지원재단이 지난 28일 발간한 KoNECT 브리프 보고서 2호를 통해 다뤄졌다.
국내 코로나19 관련 임상시험은 9건으로, 전 세계 임상시험의 1.9% 수준이다. 관련해 재단은 보고서를 통해 “(정부는) 방역 성공 모델 구축뿐만 아니라 백신·치료제 개발의 조기 성공을 돕기 위한 체계적인 구축이 필요한 시점”이라고 제언했다.
466건 중 백신 관련 임상은 14건이다. 이 중 연구자 임상 10건, 제약사 임상시험 3건, NIH 후원 임상 1건이다. 백신의 경우 연구자 주도 임상연구가 71.4%를 차지함을 알 수 있다.
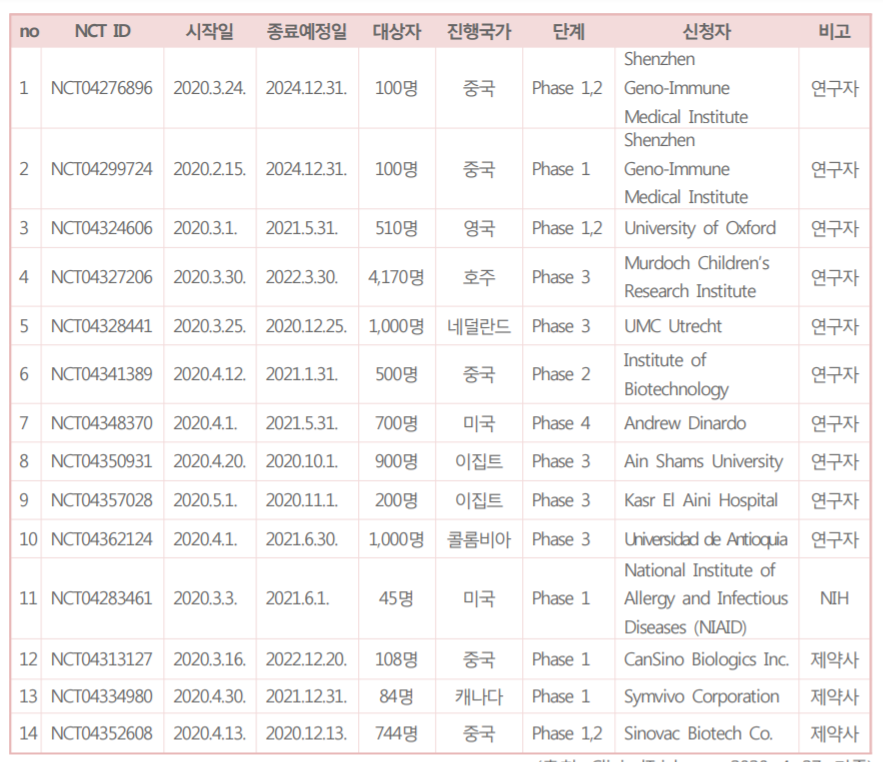
영국 과학저널 <네이처>에 따르면, 현재 개발 중인 코로나19 백신은 ▲바이러스 백신(불활화 백신, 약독화 백신) ▲바이러스벡터 백신(복제 가능, 복제 불가능) ▲핵산백신(DNA 백신, RNA 백신) ▲단백질기반 백신(단백질 서브유닛 백신, 바이러스유사입자(VLP) 백신)이 있다.
이중 세계보건기구(WHO)가 발표한 임상 개발 단계 백신 후보물질 7개는 ▲미국 모더나의 RNA 백신 ▲미국 이노비오의 DNA 백신 ▲중국 CanSino의 바이러스벡터 백신 ▲중국 시노백의 바이러스 백신(불활화) ▲중국 베이징생물의약품연구소의 바이러스 백신(불활화) ▲영국 옥스포드대와 제너연구소의 바이러스벡터백신 ▲독일 바이오엔텍의 RNA 백신이 있다.
국내에서는 국립보건연구원과 SK바이오사언스가 단백질기반 백신으로 각각 VLP와 단백질 서브유닛 백신을 개발 중이다.
미국 질병예방통제센터(CDC)에 근무 중인 문성실 박사는 자신의 페이스북을 통해 “현재 코로나19 백신으로 가장 많이 개발되고 있는 방법은 스파이크 단백질/서브유닛(protein/subunit) 백신”이라며 “민간 주도 백신 연구를 가장 많이 하는 지역으로는 북아메리카 비율이 높은 편”이라고 언급했다. 이어 “바이러스벡터 백신의 경우도 영국과 제너 연구소가 개발 중인 백신 후보물질이 주목 받고 있다”고 덧붙였다.
코로나19 치료제 관련 임상시험은 지난 27일 clinicaltrial.gov 등록 기준 452건으로, 연구자 임상시험 304건, 제약사 임상시험 141건, NIH와 미국 정부 주도 임상 7건으로 나타났다. 치료제 임상 역시 백신과 마찬가지로 연구자 임상시험이 67.3%로 활발하게 진행 중인 것으로 나타났다. 약제 유형별로 살펴보면, 화합물의약품이 382건, 바이오의약품 임상이 57건인 것으로 집계됐다.
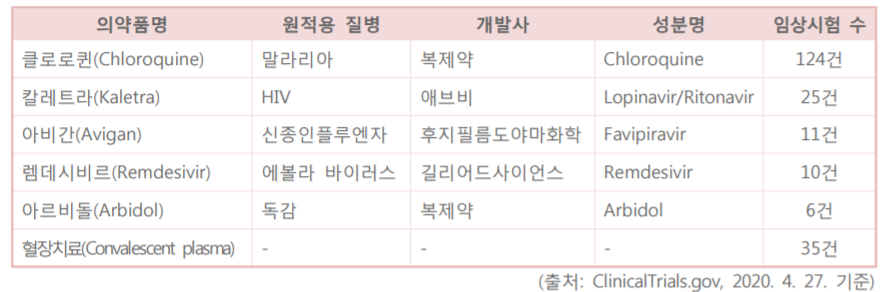
현재 가장 많이 진행되고 있는 임상시험은 말라리아 치료제 ‘하이드록시클로로퀸’(클로로퀸)이 124건으로 가장 많았고, 이어 HIV 치료제 ‘칼레트라’가 25건, 신종인플루엔자 치료제 ‘아비간’이 11건, 에볼라 바이러스 후보물질 ‘렘데시비르’ 10건, 독감 치료제 ‘아르비돌’이 6건, 혈장치료제가 35건이었다.
현재 국내에서는 코로나19 치료제 관련 연구자 임상시험 6건과 제약사 임상시험 3건 등 총 9건의 임상시험이 식품의약품안전처의 승인받아 진행 중이다. 이 중 4건의 임상시험이 ClinicalTrials.gov에도 등록돼 있다.
구체적으로 살펴보면 제약사 주도 임상시험 3건은 길리어드 사이언스의 렘데시비르 임상 2건과 부광약품의 클로로퀸과 레보비르 임상이다. 그 외 연구자 주도 임상으로는 렘데시비르, 클로로퀸과 칼레트라 병용임상, 클로로퀸 단독임상, 천식 치료제 알베스코 흡입제, 혈액응고방지제 후탄, 뇌경색 치료제 ‘페로딜’ 관련 임상이 있다.
재단은 보고서를 통해 “임상시험 책임자는 임상시험용 의약품의 관리, 무작위배정 및 눈가림해제,대상자의 동의, 임상시험의 안전성과 관련한 보고, 보험 가입, 임상시험의 품질보증 및 임상시험자료의 품질관리, 자료의 처리, 모니터링, 점검 등 필요한 모든 제반 활동에 대해 관리의무를 지닌다”며 “때문에 실질적으로 진료를 중심으로 움직이는 임상현장에서 임상의사가 임상연구에만 몰두하기 어려운 실정”이라고 지적했다.
그러면서 “재단은 현재 진행 중인 코로나19의 백신·치료제 개발을 위한 임상시험의 시험책임자(PI)와 관련 학회 등의 의견을 수렴해 공익적 임상시험의 선정 기준과 구체적인 지원 내용에 대해 정부와 협의할 예정”이라고 밝혔다.
관련기사
- 인류의 기다림!...렘데시비르·클로로퀸은 '반신반의' 상태
- 부광 레보비르 · SK케미칼 후탄… 코19 치료효과 낼까
- 코로나19로 의약품 임상시험 차질...원료약 수급도 불안
- '과학적 지식 없다'고 규제 당국만 탓하는 일부 연구자들
- "렘데시비르 연구 결과 다 나온 게 아냐… 아직 유보적"
- "렘데시비르 효과, 정확히 판단하려면 추가 자료 필요"
- 브리핑 | "희망보다 신중" 렘데시비르, 결과 더 지켜봐야
- 녹십자, 글로벌 혈액제제 기업과 코19 혈장치료제 개발 협력
- 코로나 치료제·백신, 끝을 보려면 "전략과 협력" 절실
- GC녹십자, 코19 혈장치료제 전면 무상 공급키로

