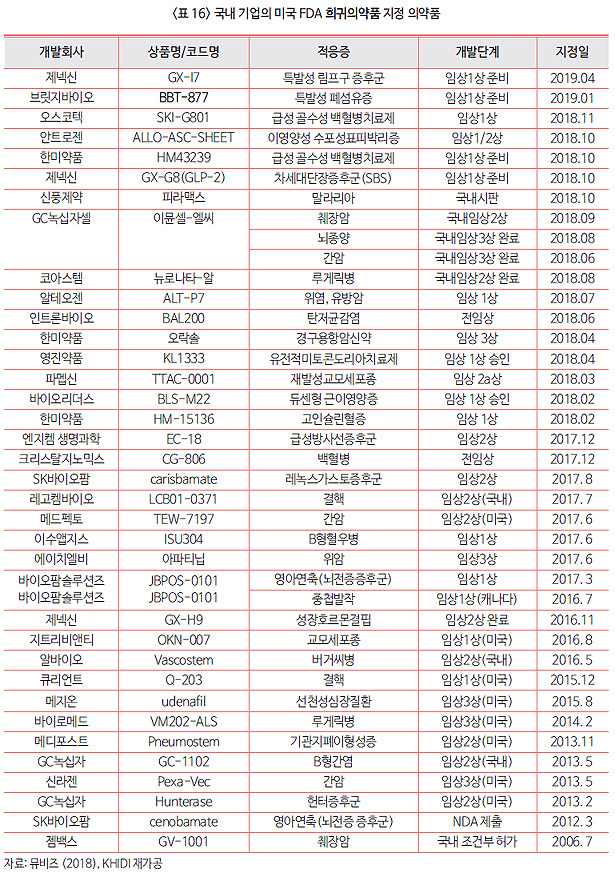
한미약품 4건 지정 최다… 매년 지정 건수 증가
대웅제약 특발성 폐섬유증치료 신약도 가세

국내 제약사의 신약 후보물질이 미국 FDA로부터 희귀의약품으로 지정받는 사례가 매년 증가하고 있다. 실제 2015년 2건, 2016년 3건, 2017년 9건, 2018년 16건으로 지정 건수는 크게 늘었다.
미국 FDA의 희귀의약품 지정(Orphan Drug Designation, ODD)은 희귀난치성 치료제 개발·허가가 신속하게 이뤄지도록 지원하는 제도다. 희귀의약품으로 지정되면 임상시험 승인·허가 기간 단축, 전문의약품 허가 신청비용 면제, 세금감면 등 다양한 혜택이 주어진다.
히트뉴스는 그동안 FDA로부터 희귀의약품으로 지정받은 국내 개발신약 현황을 정리해봤다.
대웅제약의 특발성 폐섬유증 합성신약 'DWN12088'도 지난 8일 미국 FDA로부터 희귀의약품으로 지정받았다. 특발성 폐섬유증은 폐가 서서히 굳어지면서 폐 기능을 상실하는 간질성 폐질환으로 5년 생존율이 40% 미만이다. 대웅제약 연구진은 PRS(Prolyl-tRNA Synthetase) 단백질이 콜라겐 및 섬유화 유발 인자 생성에 기여한다는 사실에 착안했고, PRS 단백질 활성만을 선택적으로 감소시켜 폐섬유증의 원인인 콜라겐의 과도한 생성을 억제하는 DWN12088을 발견했다.
DWN12088은 세상에 없던 신약(First-In-Class)을 목표로 개발되고 있다. 대웅제약에 따르면 DWN12088은 전임상에서 폐섬유증 동물모델을 통해 기존 약물 대비 우수한 효능·안전성이 입증됐다. 현재 호주 인간연구윤리위원회(Human Research Ethics Committee, HREC)에 임상1상 시험계획서를 제출한 상태이며, 올 3분기 글로벌 임상 1상 개시를 앞두고 있다.
한미약품의 단장증후군 바이오신약 '랩스 GLP-2 아날로그'(LAPS GLP-2 Analog, HM15912), 급성 골수성 백혈병 합성신약 'FLT3'(HM43239), 경구용 전이성 유방암 합성신약 '오락솔', 선천성 고인슐린혈증·비만 바이오신약 '랩스 글루카곤 아날로그'(LAPS Glucagon Analog, HM15136)도 지난해와 올해에 걸쳐 모두 희귀의약품으로 지정받았다.
랩스 GLP-2 아날로그는 지속형 GLP-2 유도체로 투약이 편리하며(주1회 투여) 체내 안정성 증가로 장세포 생성 효력도 뛰어나다. 계열 내 경쟁력 있는 신약(Best-In-Class)을 목표로 개발 중이며, 지난 7월 8일 국내 1상 임상시험 단계에 본격 돌입했다. 단장증후군은 선천성 또는 생후 수술적 절제로 전체 소장의 50% 이상이 소실돼 흡수장애·영양실조를 일으키는 희귀질환이다. 한미약품은 "HM15912는 자사의 독자적인 플랫폼 기술 '랩스커버리'가 적용됐다. 체내 지속성 및 융모세포 성장 촉진 효과로 단장증후군 환자의 삶의 질을 개선할 것으로 기대된다"고 했다.
FLT3는 급성 골수성 백혈병을 유발하는 FLT3(FMS-like tyrosine kinase 3) 돌연변이를 억제하면서 기존 FLT3 저해제의 약물 내성을 극복한 차세대 신약 후보물질이다. 현재 국내·미국에서 임상 1상을 각각 진행하고 있다. FLT3은 조혈모세포 및 조혈전구세포의 생존·증식·분화·세포자멸사 과정에서 중요한 역할을 하는 효소다. FLT3 돌연변이가 발생하면 하위 신호 전달이 과활성화되면서 세포가 비정상적으로 증식해 백혈병이 발병한다. 급성 골수성 백혈병 환자의 약 30%는 FLT3 돌연변이를 내포하는 것으로 알려져 있다.
오락솔은 정맥주사용 항암제 '파클리탁셀'을 경구용으로 전환한 혁신 항암신약으로 한미약품이 개발한 플랫폼 기술 '오라스커버리'(Orascovery)가 적용됐다. 오라스커버리는 경구흡수 증진 약물전달 기술인데, 한미약품은 2011년 미국 아테넥스(Athenex) 사에 이 기술을 라이선스 아웃했다. 지난 8일 아테넥스에 따르면, 글로벌 임상 3상에서 기존 정맥주사용 항암제보다 오락솔의 효능·편의성이 더 우수하게 나타났고, 주요 부작용인 신경병증 발생 빈도 또한 획기적으로 감소했다. 이를 토대로 아테넥스는 이른 시일 내 미국 FDA에 신약허가 사전미팅(Pre-NDA Meeting)을 신청할 예정이다.
비만 및 선천성 고인슐린증 치료제 랩스 글루카곤 아날로그는 주 1회 제형의 바이오신약 주사제로, 한미약품의 바이오신약 플랫폼 기술 '랩스커버리'(Lapscovery)가 적용됐다. 랩스커버리는 바이오의약품의 짧은 반감기를 늘려 투여 횟수·투여량을 감소시킴으로써 부작용은 줄이고 효능은 제고하는 기술이다. 한미약품에 따르면, 랩스 글루카곤 아날로그는 전임상에서 유의미한 약동학적 변화와 탁월한 체중 감소효과를 입증했으며 임상 1상을 마친 뒤 올 4분기 2상 임상시험에 착수할 예정이다.
신풍제약의 항말라리아 합성신약 '피라맥스'는 지난해 10월 미국 FDA로부터 희귀의약품으로 지정됐다. 지난해 아프리카 시장에 시판된 후 최근 아프리카 코트디부아르·콩고공화국·니제르에서 항말라리아 치료지침 1차 치료제로 등재됐으며, 기타 아프리카 10개국에도 진출했다. 지난 7월 3일과 4일에는 미국 대외원조기구 유세이드(USAID) 사 및 유니세프(UNICEF)와 피라맥스 조달을 위한 장기공급협정을 각각 체결했다. 신풍제약 관계자는 "피라맥스는 차세대 말라리아 치료제로, 약물 효능·효과에 대한 임상적 효용성이 이미 입증됐다. 기존 말라리아 치료의 임상적 문제점을 극복할 수 있을 것"이라고 했다.
영진약품의 미토콘드리아 이상 질환 신약 'KL1333'은 지난해 4월 미국 FDA의 희귀의약품 지정을 받았다. 현재 국내 임상1상과 글로벌 임상1a/b상을 진행하고 있다. KL1333은 미토콘드리아 질환 환자로부터 분리한 세포의 '아데노신 3인산'(ATP, 생명체의 주된 에너지원) 생산을 증가시키고, 젖산·활성산소종의 생성을 억제하는 물질이다.
KL1333은 활성산소종 억제 효과 위주인 기존 약물과는 달리 세포 에너지 대사 활성화를 유도하고, 미토콘드리아의 기능 및 생합성을 증가시켜 치료 효과를 나타내는 새로운 기전이다. 영진약품은 2017년 4월 스웨덴 뉴로바이브(NeuroVive) 사에 KL1333의 개발·판매 독점권을 부여하는 글로벌 라이센스 협약을 체결했다. 이재준 영진약품 사장은 "치료법이 거의 없거나 전혀 없는 심각한 유전적 미토콘드리아 질환 환자들을 위해 파트너사인 뉴로바이브와 함께 희망적인 치료제를 개발해 나갈 것"이라고 했다.